+3Li 1s 2 2s 1 1с 2с
Структура атома
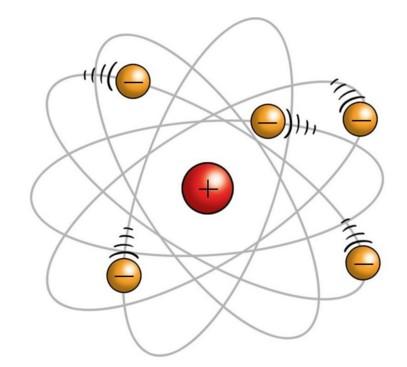
Одна из первых моделей структуры атома, ” модель пудинга “была разработана D. D. Thomson в 1904 году. Томсон открыл существование электронов, за что получил Нобелевскую премию. Однако наука того времени не могла объяснить существование этих особых электронов в пространстве. Томсон предположил, что атом состоит из отрицательных электронов, помещенных в равномерно положительно заряженный “суп”, который компенсирует заряд электронов (другая аналогия – кишмиш в пудинге). Модель, конечно, оригинальная, но ошибочная. Однако модель Томсона послужила отличной отправной точкой для дальнейшей работы в этой области.

И дальнейшая работа оказалась успешной. Ученик Томсона Эрнест Резерфорд, основываясь на экспериментах по рассеянию альфа-частиц на золотой фольге, предложил новую планетарную модель атомной структуры.
Согласно модели Резерфорда, атом состоит из массивного, положительно заряженного ядра и частиц малой массы – электронов, которые, подобно планетам вокруг Солнца, летают вокруг ядра и не падают на него.
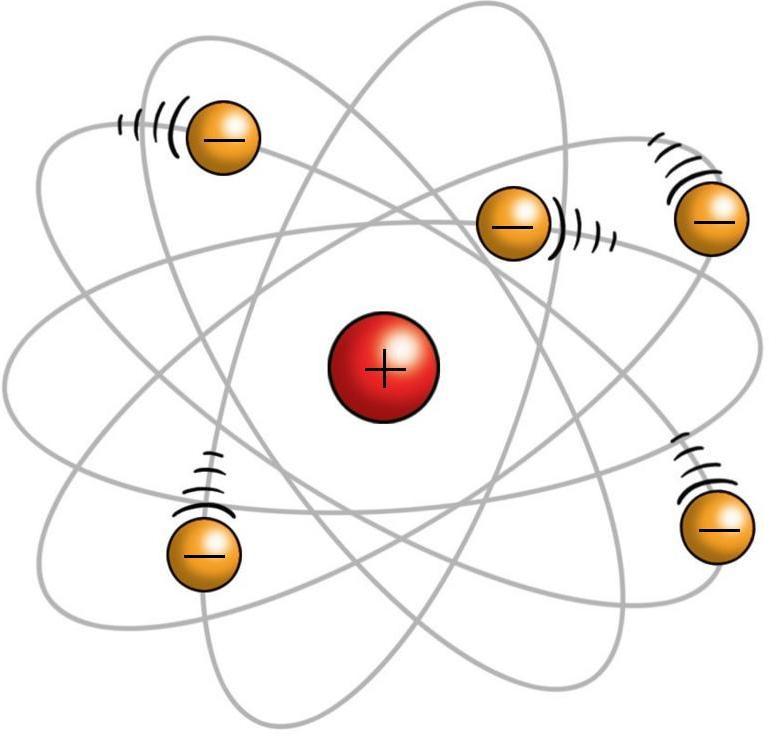
Модель Резерфорда оказалась еще одним шагом в изучении структуры атома. Однако современная наука использует более совершенную модель, предложенную Нильсом Бором в 1913 году. Об этом будет рассказано подробно.
Атом – это наименьшая электрически инертная, химически неделимая частица материи, состоящая из положительно заряженного ядра и отрицательно заряженной электронной оболочки.
Электроны движутся не по определенной орбите, как предполагал Резерфорд, а скорее хаотично. Набор электронов, которые движутся вокруг ядра, называется электронная оболочка .
А объем ядра.который является массивным и положительно заряженным, как доказал Резерфорд, расположен в центральной части атома. Структура ядра довольно сложна и изучается в ядерной физике. Основными частицами, составляющими атомное ядро, являются протоны и нейтроны . Они связаны друг с другом ядерными силами (сильное взаимодействие).
Давайте рассмотрим основные характеристики протоны, нейтроны и электроны:
| Протон | Нейтрон | Электрон | |
| Масса | 1.00728 а.е.м. | 1.00867 а.е.м. | 1/1960 a.u.m. |
| Зарядка | + 1 элементарный заряд | 0 | – 1 элементарный заряд |
1 а.е.м. (атомная единица массы) = 1,66054-10 -27 кг
1 элементарный заряд = 1,60219-10 -19 K
И – самое главное. Периодическая таблица химических элементов, построенная Дмитрием Ивановичем Менделеевым, следует простой и понятной логике: атомный номер – это количество протонов в ядре данного атома . А Дмитрий Иванович в 19 веке ни о каких протонах и слыхом не слыхивал. Тем более гениальным было его открытие, его способности и научное чутье, которые позволили ему продвинуть науку на полтора столетия вперед.
Следовательно, заряд ядра Z равен количество протоновэто количество атомов в периодической таблице химических элементов.
Атом – это электрически нейтральная молекула, поэтому количество протонов равно количеству электронов: Ne = Np = Z.
Масса атома ( массовое число A ) примерно равна суммарной массе крупных частиц, из которых состоит атом, – протонов и нейтронов. Поскольку масса протона и нейтрона приблизительно равна 1 атомной единице массы, можно использовать формулу:
Массовое число приводится в периодической таблице химических элементов в ячейке каждого элемента.
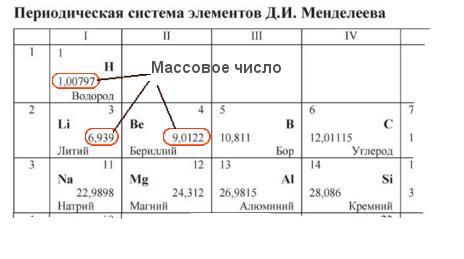
Пожалуйста, обратите внимание! При решении заданий ЕГЭ массовое число всех атомов, кроме хлора, округляется до целого числа по правилам математики. Предполагается, что массовое число атома хлора в ЕГЭ равно 35,5.
Поэтому количество нейтронов в атоме можно рассчитать, вычитая атомный номер из массового числа: Nn = M – Z.
В периодической таблице есть химические элементы – Атомы с одинаковым ядерным зарядом. Но может ли измениться количество других молекул в этих атомах? Довольно много. Например, атомы с разным числом нейтронов называются изотопы …данного химического элемента. Один и тот же элемент может иметь несколько изотопов.
Попробуйте ответить на вопросы. Ответы приведены в конце статьи:
- Имеют ли изотопы одного и того же элемента одинаковое или разное массовое число?
- Имеют ли изотопы одного и того же элемента одинаковое или разное количество протонов?
Химические свойства атомов определяются структурой электронной оболочки и зарядом ядра. Поэтому химические свойства изотопов одного и того же элемента практически одинаковы.
Поскольку атомы одного и того же элемента могут существовать в виде различных изотопов, массовое число часто указывается в названии, например, хлор-35, и такая форма написания атомов принята:

Еще несколько вопросов:
3. Определите число нейтронов, протонов и электронов в изотопе бром-81.
4. Определите число нейтронов в изотопе хлора-37.
Диаметр атома составляет 10 -10 м, диаметр ядра – 10 -14 – 10 -15 м. Масса атома водорода составляет 1,67 – 10 -24 г, атома углерода – 1,99 – 10 -23 г, а атома железа – 9,29 – 10 -23 г.
Из каких элементарных частиц состоит атом?
Ключевые слова: атомная структура, элементарные частицы, протоны и электроны в атомах, атомный номер, массовое число, нейтронное число, нуклид, изотопы, ионы, катионы, заряд иона.
Согласно модели Резерфорда, каждый атом состоит из ядра в центре и электронной оболочки. Весь положительный заряд и почти вся масса атома сосредоточены в ядре. Электроны движутся вокруг ядра. Число электронов в атоме равно положительному заряду ядра.
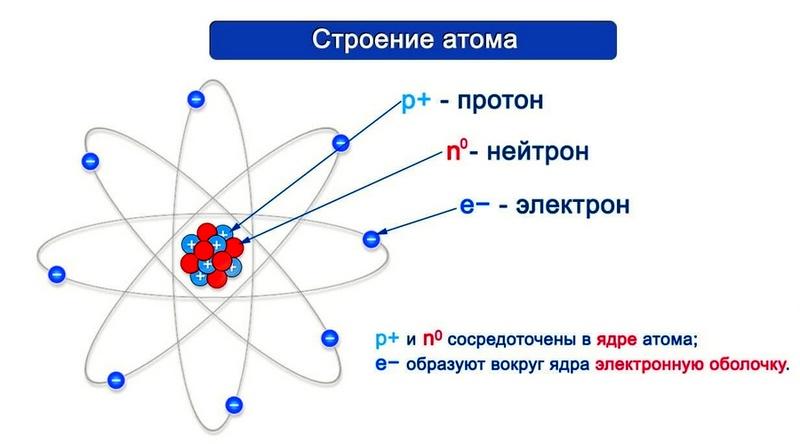
Диаметр атома составляет 10 -10 м, диаметр ядра – 10 -14 – 10 -15 м. Масса атома водорода составляет 1,67 – 10 -24 г, атома углерода – 1,99 – 10 -23 г, а атома железа – 9,29 – 10 -23 г.
Элементарные частицы – это протоны, электроны и нейтроны, из которых состоят все атомы.
Таблица 1: “Элементарные частицы атома”.
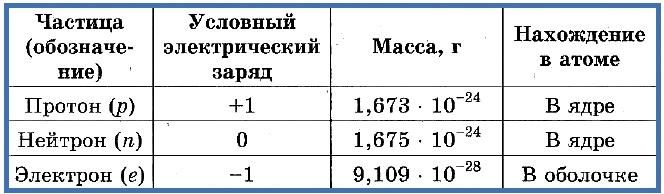
Число протонов различно для разных типов атомов, определяет заряд атомного ядра и равно атомному номеру элемента в таблице Менделеева. Поскольку атом является электрически нейтральной молекулой, число электронов в нем равно числу протонов.
Таблица 2: “Протоны и электроны в атомах”.
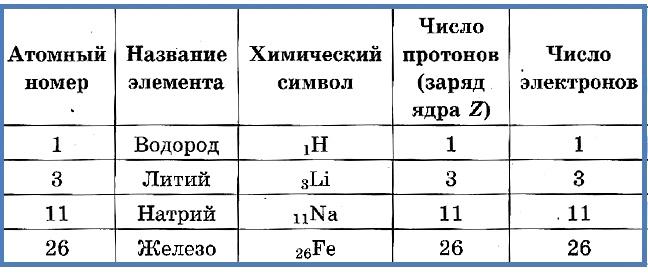
Атомный номер указывается слева внизу от символа элемента, например: 1Н, 26Fe. Атомный номер обозначается заглавной латинской буквой Z.
Атомный массовый номер A – это сумма чисел протонов и нейтронов в ядре. Массовый номер указывается в левом верхнем углу символа элемента или добавляется к названию элемента через дефис, например: 23 Na или натрий-23.
Массовое число кислорода, A( 16 O) = 16 = (8p + 8n).
Количество нейтронов N в ядре атома задается формулой: N = A – Z. Например, для атома натрия с массовым числом 23, 23 Na: A = 23, Z = 11, N = A – Z = 23 – 11 = 12.
Нуклид – это вид атома с определенным количеством протонов и нейтронов в ядре. Например, в природе существует три типа кислородных нуклидов: 16 O, 17 O и 18 O.
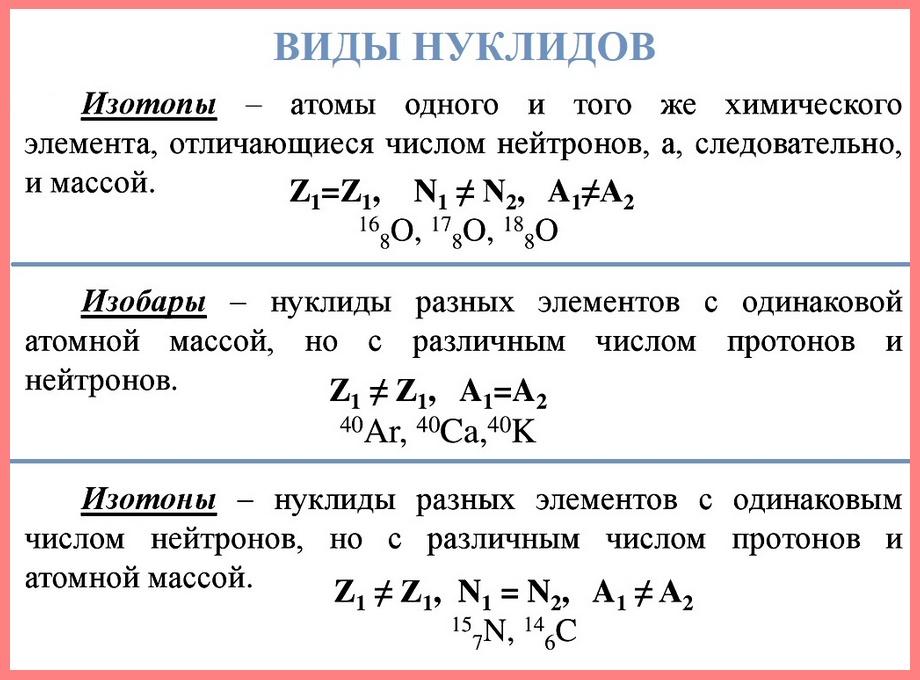
Изотопы – это атомы одного вида с одинаковым числом протонов, но разным числом нейтронов. Таким образом, атомы 16 O, 17 O и 18 O являются изотопами. Природными изотопами урана являются 234 U, 235 U и 238 U.
Ионы – это заряженные частицы, образующиеся при отщеплении или присоединении электронов к нейтральным атомам. Ионы также образуются из молекул путем присоединения протона H + (NH3 → NH4 + ) или в результате отщепления H + (HNO3 -> НЕТ3 – ).
Таблица 3 “Обозначение и название ионов”.

Катионы – положительно заряженные ионы (Na + , Al 3+ ), анионы – отрицательно заряженные ионы (Cl – , NO3 – ).
Заряд иона указывается в виде подстрочного знака в правом верхнем углу символа химического элемента: Li + , Ca 2+ . На первом месте пишется число, а на втором – знак заряда. Число 1 не написано.
Атомы состоят из электронов, протонов и нейтронов. Нейтроны были открыты после того, как физики разработали планетарную модель атома. Только в 1932 году в ходе серии экспериментов Джеймс Чедвик обнаружил частицы без заряда. Отсутствие заряда было подтверждено тем, что эти частицы никак не реагировали на электромагнитное поле.
Электроны внутри атома
Отрицательно заряженные электроны движутся вокруг ядра атома, образуя своего рода облако. Массивное ядро притягивает электроны, но энергия самих электронов позволяет им “убегать” дальше от ядра. Поэтому чем выше энергия электрона, тем дальше от ядра он находится.
Энергия электрона не может быть произвольной, она соответствует четко определенному набору энергетических уровней в атоме. Это означает, что энергия электрона ступенчато изменяется от одного уровня к другому. Соответственно, электрон может двигаться только в пределах ограниченной электронной оболочки, соответствующей тому или иному энергетическому уровню – таков смысл постулата Бора.

Набирая больше энергии, электрон “перепрыгивает” с ядра на более высокий слой, теряя энергию – наоборот, на более низкий. Таким образом, облако электронов вокруг ядра упорядочивается в виде нескольких “нарезанных” слоев.
Периодический характер изменения структуры, физических и химических свойств присущ также простым и сложным веществам. В качестве примера рассмотрим закономерности изменения некоторых свойств атомов и соединений элементов периода 3 (см. табл. 8).
Ядерная модель атомной структуры
В начале 20 века на основе исследований многих ученых, прежде всего английского физика Э. Резерфорда, была создана основная модель строения атома, которая получила название ядерная (планетарная) модель. Согласно этой модели, атом состоит из положительно заряженного ядра и движущихся вокруг него отрицательно заряженных электронов. Почти вся масса атома (более 99,96%) сосредоточена в ядре. Диаметр ядра примерно в 100 000 раз меньше диаметра атома в целом (порядка 1000). 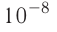
Атом – это наименьшая единица химического элемента, которую нельзя разложить химическим путем на другие, более мелкие и простые материальные частицы.
Структура атомов – элементарных частиц материи, электронов, протонов, нейтронов
 Все физические тела в природе состоят из разновидности материи, называемой веществом. Вещества делятся на две основные группы: простые и сложные.
Все физические тела в природе состоят из разновидности материи, называемой веществом. Вещества делятся на две основные группы: простые и сложные.
Сложные вещества – это те, которые могут быть разложены на другие, более простые вещества в результате химических реакций. В отличие от сложных веществ, простые вещества – это те, которые не могут быть химически разложены на еще более простые вещества.
Примером сложного вещества является вода, которая может быть химически разложена на два других, более простых вещества – водород и кислород. Что касается последних двух, то они уже не могут быть химически разложены на более простые вещества и поэтому являются простыми веществами, другими словами, химическими элементами.
В первой половине 19 века наука приняла предположение, что химические элементы являются неизменными веществами, не имеющими общей связи друг с другом. Однако российский ученый Д. I. Менделеев (1834-1907) в 1869 году первым раскрыл взаимосвязь химических элементов и показал, что качественная характеристика каждого элемента зависит от его количественной характеристики – атомной массы.
Изучая свойства химических элементов, Д. И. Менделеев заметил, что их свойства периодически повторяются в зависимости от атомной массы. Он представил эту периодичность в виде таблицы, которая стала известна в науке как Периодическая таблица элементов Менделеева.
Ниже приведена современная периодическая таблица химических элементов Менделеева.
Согласно современным представлениям науки, каждый химический элемент состоит из набора мельчайших материальных (осязаемых) частиц, называемых атомами.
Атом – это наименьшая часть химического элемента, которая не может быть разложена химическим путем на другие, более мелкие и простые материальные частицы.
Атомы различных химических элементов в природе отличаются по физическим и химическим свойствам, структуре, размеру, массе, атомному весу, внутренней энергии и некоторым другим свойствам. Например, атом водорода значительно отличается по своим свойствам и структуре от атома кислорода, а тот от атома урана и т.д.
Установлено, что атомы химических элементов имеют очень малые размеры. Если условно считать, что атомы имеют сферическую форму, то их поперечное сечение должно быть равно одной стомиллионной части сантиметра. Например, размер поперечного сечения атома водорода, самого маленького атома в природе, составляет сто миллионных долей сантиметра (10 – 8 см), а размер поперечного сечения самых крупных атомов, например, атома урана, не превышает трехсот миллионных долей сантиметра (3 – 10 – 8 см). Поэтому атом водорода меньше земного шара на радиус в один сантиметр.
Из-за очень маленького размера атомов их масса также очень мала. Например, масса атома водорода равна т = 1,67 – 10 -24 г. Это означает, что в одном грамме водорода содержится около 6 – 10 23 атомов.
Атомная масса химического элемента – это абстрактное число, которое показывает, во сколько раз его масса больше, чем 1/16 массы атома кислорода.
В периодической таблице элементов Д. Менделеева приведены атомные массы всех химических элементов (см. число под названием элемента). Из таблицы видно, что самым легким атомом является водород с атомной массой 1,008. Атомная масса углерода равна 12, кислорода – 16 и так далее.
Что касается более тяжелых химических элементов, то их атомные массы более чем в 200 раз превышают массу водорода. Например, атомная масса ртути составляет 200,6, радия – 226 и т.д. Чем выше порядок номера, занимаемого химическим элементом в периодической таблице элементов, тем больше его атомная масса.
Большинство атомных масс химических элементов выражаются в виде дробных чисел. Это в некоторой степени объясняется тем, что такие химические элементы состоят из совокупности многих разновидностей атомов с разными атомными массами, но схожими химическими свойствами.
Химические элементы, которые занимают одинаковый номер в периодической таблице элементов и поэтому имеют одинаковые химические свойства, но разные атомные массы, называются изотопами.
Изотопы встречаются у большинства химических элементов, у кальция два изотопа, у извести – четыре, у цинка – пять, у олова – одиннадцать и т.д. Многие изотопы получают искусственными методами, и среди них некоторые имеют большое практическое значение.
Элементарные частицы материи
Долгое время считалось, что именно атомы химических элементов составляют предел делимости материи, т.е. являются элементарными “строительными блоками” Вселенной. Современная наука отвергла эту гипотезу, установив, что атом каждого химического элемента представляет собой совокупность еще более мелких материальных частиц, чем сам атом.
Согласно электронной теории материи, атом любого химического элемента представляет собой систему, состоящую из центрального ядра, вокруг которого циркулируют “элементарные” частицы материи, называемые электронами. Ядра атомов, согласно общепринятому мнению, состоят из набора “элементарных” частиц материи – протонов и нейтронов.
Чтобы понять структуру атомов и происходящие в них физические и химические процессы, необходимо хотя бы смутно представлять себе основные характеристики элементарных частиц, из которых построены атомы.
Установлено, что электрон – это частица с наименьшим отрицательным электрическим зарядом, наблюдаемым в природе.
Если условно считать, что электрон как частица имеет сферическую форму, то его поперечное сечение должно быть 4 – 10 -13 см, т.е. оно в десятки тысяч раз меньше, чем поперечное сечение любого атома.
Электрон, как и любая другая реальная частица, имеет массу. Масса покоя” электрона, т.е. Его масса в состоянии относительного покоя равна m o = 9,1 – 10 -28 г.
Чрезвычайно малая “масса покоя” электрона показывает, что инерционные свойства электрона очень слабы, а это значит, что электрон может под воздействием изменяющейся электрической силы колебаться в пространстве с частотой многие миллиарды периодов в секунду.
Масса электрона настолько мала, что для получения одного грамма электронов необходимо взять 1027 штук. Чтобы иметь хоть какое-то физическое представление об этом колоссально огромном числе, приведем пример. Если один грамм электронов расположить по прямой линии близко друг к другу, они образуют цепочку длиной четыре миллиарда километров.
Масса электрона, как и масса любой другой частицы материи, зависит от скорости его движения. Электрон в состоянии относительного покоя имеет “массу покоя”, которая является механической по своей природе, как и масса любого физического тела. Что касается “массы движения” электрона, которая увеличивается со скоростью его движения, то она имеет электромагнитное происхождение. Это объясняется наличием электромагнитного поля у движущегося электрона как вида материи, обладающего массой и электромагнитной энергией.
Чем быстрее движется электрон, тем больше инерционные свойства его электромагнитного поля, тем больше его масса и, следовательно, его электромагнитная энергия. Поскольку электрон и его электромагнитное поле представляют собой единую органически связанную материальную систему, естественно, что масса движения электромагнитного поля электрона может быть непосредственно отнесена к самому электрону.
В дополнение к свойствам частицы, электрон также обладает волновыми свойствами. Эксперименты показали, что поток электронов, как и поток света, распространяется в виде волнового движения. Природа волнового движения потока электронов в пространстве подтверждается явлениями интерференции и дифракции электронных волн.
Интерференция электронов – это явление наложения электронных волн друг на друга, а дифракция электронов – это явление окружения электронными волнами краев узкой щели, через которую проходит поток электронов. Следовательно, электрон – это не просто частица, а “частица-волна”, длина которой зависит от массы и скорости электрона.
Установлено, что электрон, помимо поступательного движения, совершает также вращательное движение вокруг своей оси. Этот тип движения называется “вращение” (от английского слова “spin” – веретено). В результате этого движения электрон, помимо своих электрических свойств, обусловленных электрическим зарядом, приобретает также магнитные свойства, напоминающие элементарный магнит.
Протон – это реальная частица с положительным электрическим зарядом, равным по абсолютной величине электрическому заряду электрона.
Масса протона составляет 1,67 – 10 -24 г, что примерно в 1840 раз больше “массы покоя” электрона.
В отличие от электрона и протона, нейтрон не имеет электрического заряда, т.е. является электрически инертной “элементарной” частицей материи. Масса нейтрона почти равна массе протона.
Электроны, протоны и нейтроны, из которых состоят атомы, взаимодействуют друг с другом. В частности, электроны и протоны, как частицы, имеющие противоположные электрические заряды, притягиваются друг к другу. В то же время электрон от электрона и протон от протона отталкиваются как частицы с одинаковыми электрическими зарядами.
Взаимодействие всех этих электрически заряженных частиц происходит через их электрические поля. Эти поля представляют собой особый вид материи, состоящий из набора элементарных материальных частиц, называемых фотонами. Каждый фотон имеет четко определенное присущее ему количество энергии (квант энергии).
Взаимодействие электрически заряженных материальных частиц происходит путем обмена фотонами друг с другом. Силу взаимодействия электрически заряженных частиц обычно называют электрической силой.
Нейтроны и протоны в ядрах атомов также взаимодействуют друг с другом. Однако это взаимодействие происходит уже не через электрическое поле, поскольку нейтрон является электрически инертной частицей материи, а через так называемое ядерное поле.
Это поле также является особым видом материи, состоящим из набора элементарных материальных частиц, называемых мезонами. Взаимодействие нейтронов и протонов происходит путем обмена мезонами друг с другом. Сила взаимодействия нейтронов и протонов друг с другом называется ядерной силой.
Установлено, что ядерные силы действуют в ядрах атомов на очень малых расстояниях, порядка 10 – 13 см.
Ядерная сила намного больше, чем электрическая сила взаимного отталкивания протонов в атомном ядре. Это приводит к тому, что они не только способны преодолевать внутри атомных ядер силы взаимного отталкивания протонов, но и образовывать очень прочные ядерные системы из комбинации протонов и нейтронов.
Стабильность ядра каждого атома зависит от соотношения двух противоборствующих сил – ядерной (взаимное притяжение протонов и нейтронов) и электрической (взаимное отталкивание протонов).
Сильные ядерные силы, действующие в ядрах атомов, способствуют превращению нейтронов и протонов друг в друга. Эти взаимопревращения нейтронов и протонов происходят за счет поглощения или поглощения более легкими элементарными частицами, такими как мезоны.
Рассмотренные нами частицы называются элементарными, потому что они не состоят из совокупности других, более простых частиц материи. Но в то же время нельзя забывать, что они способны превращаться друг в друга, появляться на свет за счет друг друга. Поэтому эти частицы являются своего рода сложными образованиями, т.е. их элементарность условна.
Химическая структура атомов
Простейший по своей структуре атом – атом водорода. Она состоит из набора всего двух элементарных частиц – протона и электрона. Протон в системе атомов водорода действует как центральное ядро, вокруг которого электрон вращается по определенной орбите. Схематическое изображение атома водорода показано на рис.1.
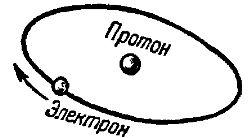
Рис.1 Схематическое изображение структуры атома водорода
Эта модель является лишь приближением к реальности. Дело в том, что электрон как “волна-частица” не имеет резко отграниченного от внешней среды объема. Это означает, что следует говорить не о точной линейной орбите электрона, а о своего рода электронном облаке. В этом случае электрон обычно занимает некоторую среднюю линию облака как одну из возможных орбит электрона в атоме.
Надо сказать, что сама электронная орбита не является строго фиксированной и неподвижной в атоме – она также, за счет изменения массы электрона, совершает определенное вращательное движение. Следовательно, движение электрона в атоме относительно сложное. Поскольку ядро атома водорода (протон) и вращающийся вокруг него электрон имеют противоположные электрические заряды, они притягиваются друг к другу.
В то же время электрон, вращаясь вокруг ядра атома, создает центробежную силу, которая стремится оторвать его от ядра. Следовательно, электрическая сила взаимного притяжения между ядром атома и электроном и центробежная сила, действующая на электрон, являются противоположными силами.
При равновесии электрон занимает относительно стабильное положение на определенной орбите в атоме. Поскольку масса электрона очень мала, чтобы уравновесить притяжение к ядру атома, он должен вращаться с огромной скоростью около 6 – 10 15 оборотов в секунду. Это означает, что электрон в системе атомов водорода, как и в любом другом атоме, движется по своей орбите с линейной скоростью более тысячи километров в секунду.
В нормальных условиях электрон вращается в атоме данного типа по орбите, ближайшей к ядру. В этом случае он обладает минимально возможным количеством энергии. Если же по той или иной причине, например, под воздействием какой-то другой материальной частицы, проникшей в атомную систему, электрон перемещается на орбиту, более удаленную от атома, то он обладает несколько большей энергией.
Однако электрон остается на этой новой орбите в течение очень короткого периода времени, а затем он снова поворачивается на орбиту, ближайшую к атомному ядру. Во время этого движения электрон отдает свою избыточную энергию в виде кванта электронно-магнитного излучения – лучистой энергии (рис.2).
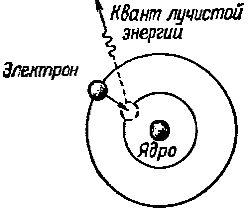
Рис. 2: Электрон, переходя с дальней орбиты на более близкую к атомному ядру, испускает квант лучистой энергии
Чем больше энергии получает электрон извне, тем дальше от атомного ядра он выходит на орбиту и тем больше электромагнитной энергии он излучает при вращении на орбиту, ближайшую к ядру.
Измеряя количество энергии, отдаваемой электроном при движении с различных орбит на орбиту, ближайшую к ядру атома, было установлено, что электрон в системе атома водорода, как и в системе любого другого атома, не может двигаться по любой орбите, кроме вполне определенной, в зависимости от энергии, которую он получает под действием внешней силы. Орбитали, которые электрон может занимать в атоме, называются орбиталями проницаемости.
Поскольку положительный заряд ядра атома водорода (заряд протона) и отрицательный заряд электрона численно равны, их суммарный заряд равен нулю. Это означает, что атом водорода в нормальном состоянии является электрически нейтральной частицей.
Это справедливо для атомов всех химических элементов: атом любого химического элемента в нормальном состоянии является электрически нейтральной частицей из-за численного равенства его положительных и отрицательных зарядов.
Поскольку ядро атома водорода содержит только одну “элементарную” частицу – протон, так называемое массовое число ядра равно единице. Массовое число ядра любого химического элемента – это общее число протонов и нейтронов в составе ядра.
Природный водород состоит в основном из набора атомов с массовым числом, равным единице. Однако он содержит другой тип атома водорода, с массовым числом два. Атомные ядра этого тяжелого водорода, называемые дейтронами, состоят из двух частиц – протона и нейтрона. Этот изотоп водорода называется дейтерием.
Природный водород содержит очень небольшое количество дейтерия. На каждые шесть тысяч атомов легкого водорода (массовое число равно единице) приходится только один атом дейтерия (тяжелого водорода). Существует еще один изотоп водорода, сверхтяжелый водород, называемый тритием. Этот изотоп водорода имеет в своем атомном ядре три частицы: протон и два нейтрона, которые связаны между собой ядерными силами. Массовое число ядра атома трития равно трем, т.е. атом трития в три раза тяжелее легкого атома водорода.
Хотя атомы изотопов водорода имеют разную массу, они обладают одинаковыми химическими свойствами, например, легкий водород вступает в химическую реакцию с кислородом, образуя сложное вещество – воду. Подобным образом изотоп водорода дейтерий соединяется с кислородом и образует воду, которая, в отличие от обычной воды, называется тяжелой водой. Тяжелая вода очень полезна при производстве ядерной энергии.
Поэтому химические свойства атомов не зависят от массы их ядер, а только от структуры электронной оболочки атома. Поскольку атомы легкого водорода, дейтерия и трития имеют одинаковое количество электронов (по одному на атом), эти изотопы обладают одинаковыми химическими свойствами.
Не случайно химический элемент водород занимает первое место в периодической таблице элементов. Факт, что между номером любого элемента в периодической таблице и величиной заряда ядра атома этого элемента существует определенная связь. Его можно сформулировать следующим образом: порядковый номер любого химического элемента в периодической таблице элементов численно равен положительному заряду его ядра и, следовательно, числу электронов, вращающихся вокруг него.
Поскольку водород занимает первое место в периодической таблице элементов, это означает, что положительный заряд ядра его атома равен единице и что вокруг ядра вращается один электрон.
Химический элемент гелий – номер два в периодической таблице элементов. Это означает, что он имеет положительный электрический заряд, равный двум, т.е. имеет два протона в ядре и два электрона в электронной оболочке атома.
Природный гелий состоит из двух изотопов – тяжелого и легкого гелия. Массовое число тяжелого гелия равно четырем. Это означает, что ядро тяжелого атома гелия должно содержать два нейтрона в дополнение к двум протонам, упомянутым выше. Что касается легкого гелия, то его массовое число равно трем, что означает, что помимо двух протонов его ядро должно содержать один нейтрон.
Было установлено, что в природном гелии количество легких атомов гелия составляет примерно одну миллионную часть от количества тяжелых атомов гелия. На рисунке 3 показана схематическая модель атома гелия. На рисунке 3 показана схематическая модель атома гелия.
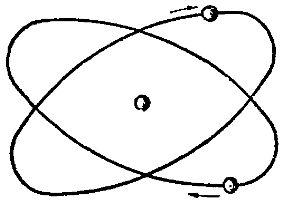
Рис.3. Схематическая модель строения атома гелия
Дальнейшее усложнение структуры атомов химических элементов заключается в увеличении числа протонов и нейтронов в ядрах атомов и одновременно в увеличении числа электронов, вращающихся вокруг ядер (рис.4). Используя периодическую таблицу элементов, можно легко определить количество электронов, протонов и нейтронов в отдельных атомах.
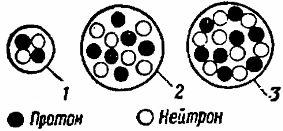
Рисунок 4: Схематические диаграммы структуры атомных ядер: 1 – гелий, 2 – углерод, 3 – кислород.
Порядковый номер химического элемента равен числу протонов в ядре атома и, одновременно, числу электронов, вращающихся вокруг ядра. Что касается атомной массы, то она приблизительно равна массовому числу атома, то есть числу протонов и нейтронов в ядре вместе взятых. Поэтому, вычитая из атомной массы элемента число, равное его порядковому номеру, можно определить, сколько нейтронов находится в ядре.
Было установлено, что ядра легких химических элементов, которые имеют в своем составе равное количество протонов и нейтронов, очень прочны, поскольку ядерные силы в них относительно велики. Ядро тяжелого атома гелия, например, необычайно прочно, потому что состоит из двух протонов и двух нейтронов, связанных между собой сильными ядерными силами.
Ядра атомов более тяжелых химических элементов содержат неравное количество протонов и нейтронов в своем составе, поэтому их связь в ядре слабее, чем в ядрах более легких химических элементов. Ядра этих элементов могут относительно легко расщепляться при бомбардировке атомными “снарядами” (нейтронами, ядрами атомов гелия и т.д.).
В случае самых тяжелых химических элементов, особенно радиоактивных, их ядра настолько слабы, что они самопроизвольно распадаются на составные части. Например, атомы радиоактивного элемента радия, который имеет 88 протонов и 138 нейтронов, распадаются на атомы радиоактивного элемента радона. В свою очередь, атомы последних распадаются на составные части, превращаясь в атомы других элементов.
После краткого знакомства с составными частями ядер атомов химических элементов рассмотрим строение электронных оболочек атомов. Как мы знаем, электроны могут вращаться вокруг атомных ядер только по четко определенным орбитам. В этом случае они настолько сгруппированы в электронной оболочке каждого атома, что можно различить отдельные слои электронов.
Каждый слой может содержать определенное количество электронов, не превышающее строго определенного числа. Например, первый электронный слой, ближайший к ядру атома, может содержать максимум два электрона, второй слой может содержать максимум восемь электронов и так далее.
Те атомы, у которых внешние электронные слои полностью заполнены, имеют наиболее стабильную электронную оболочку. Это означает, что атом прочно удерживает все свои электроны и не нуждается в получении дополнительных электронов извне. Например, у атома гелия два электрона полностью заполняют первый электронный слой, а у атома неона – десять электронов, причем первые два полностью заполняют первый электронный слой, а остальные – второй (рис. 5).
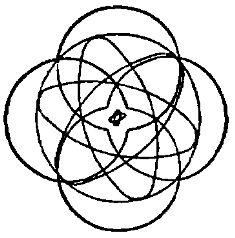
Рисунок 5: Схематическая диаграмма структуры атома неона
Поэтому атомы гелия и неона имеют достаточно стабильные электронные оболочки и не стремятся к их количественному изменению. Такие элементы химически инертны, то есть они не вступают в химическое взаимодействие с другими элементами.
Однако большинство химических элементов имеют атомы, в которых внешние электронные слои не полностью заполнены электронами. Например, атом калия имеет девятнадцать электронов, восемнадцать из которых полностью заполнены в первых трех слоях, а девятнадцатый электрон находится в следующем, незаполненном электронном слое. Плохое заполнение электронами четвертого электронного слоя приводит к тому, что атомное ядро очень непрочно удерживает самый крайний – девятнадцатый – электрон, и поэтому последний может быть легко вырван из атома.
Или, например, атом кислорода имеет восемь электронов, два из которых полностью заполняют первый слой, а остальные шесть располагаются во втором слое. Таким образом, для завершения второго электронного слоя в атоме кислорода не хватает только двух электронов. Вот почему атом кислорода не только удерживает свои шесть электронов во втором слое, но и способен привлечь два электрона, которых ему не хватает для завершения второго электронного слоя. Это достигается за счет химической связи с атомами элементов, внешние электроны которых слабо связаны с их ядрами.
Химические элементы, атомы которых, как правило, не имеют внешних электронных слоев, полностью заполненных электронами, химически активны, т.е. легко вступают в химические взаимодействия.
Так, электроны в атомах химических элементов расположены в строго определенном порядке, и любое изменение их пространственного расположения или количества в электронной оболочке атома приводит к изменению его физических и химических свойств.
Равенство числа электронов и протонов в расположении атома является причиной того, что его общий электрический заряд равен нулю. Если равенство числа электронов и протонов в атомной системе нарушается, атом становится электрически заряженной системой.
Атом, в котором система противоположных электрических зарядов находится вне равновесия, поскольку он потерял часть своих электронов или, наоборот, приобрел их избыток, называется ионом.
Способность противоположных ионов притягиваться друг к другу является причиной того, что они химически соединяются, образуя более сложные молекулы, молекулы.
В заключение следует отметить, что размер атома очень велик по сравнению с размером молекул вещества, из которого он состоит. Ядро самого сложного атома со всеми его электронами занимает миллиардную часть объема атома. Простой расчет показывает, что если кубический метр платины сжать настолько плотно, что исчезнут внутри- и межатомные пространства, то объем составит около одного кубического миллиметра.
Если вам понравилась эта статья, пожалуйста, поделитесь ею в социальных сетях. Это поможет нашему сайту сильно вырасти!
Чтобы закрепить все эти понятия, давайте рассмотрим структуру атома теллура и некоторые его свойства (см. рис. 13). Этот рисунок показывает, что теллур – неметалл, потому что, во-первых, он имеет шесть электронов на внешнем уровне, и, во-вторых, его символ находится в строке главной подгруппы над линией B – At. Поэтому его атом может и взять (пока не будет завершен внешний уровень, и отдать электроны. В результате, в отличие от металлов, неметаллический теллур может находиться в более низкой степени окисления (–2) и образуют летучие соединения с водородом (Н2Te). Высшее состояние окисления атома теллура (+6), как и в случае с металлами, соответствует номеру группы, и в этом состоянии окисления теллур образует высший оксид TeO3.
Структура атома и свойства элементов
Мы получили краткую электронную формулу атома марганца, которая отражает расположение его валентных электронов. Что мы можем определить из этой формулы?
1. Какие свойства, металлические или неметаллические, преобладают у этого элемента? Ответ: Марганец является металлом, поскольку имеет 2 электрона на внешнем (четвертом) уровне.
2. Какой процесс характерен для металла? Ответ: Всегда только пожертвование электронов.
3. Какие электроны и сколько электронов отдаст атом марганца? Ответы:
- Два внешних электроны (они находятся дальше всего от ядра и меньше притягиваются к нему);
- семь (2+5) валентность электронов (поскольку в этом случае на третьем уровне атома останется восемь электронов, т.е. a полный уже внешний уровень).
Все эти рассуждения и выводы можно отразить на диаграмме (рис. 12).
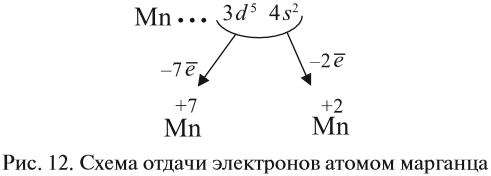
Результирующие условные заряды атома называются
Принимая структуру атомов кислорода и водорода и проводя аналогичные рассуждения, можно показать, что типичными состояниями окисления для кислорода являются -2, а для водорода +1.
Вопрос. С какими из этих химических элементов марганец может образовывать соединения, если учитывать его степени окисления, полученные выше?
Только с кислородом, поскольку его атом имеет противоположную степень окисления. В этом случае нетрудно придумать формулы для соответствующих Оксиды марганца (Здесь состояния окисления соответствуют валентностям химических элементов):
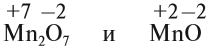
Структура атома марганца предполагает, что более высокой степени окисления, чем +7, в марганце быть не может, так как в этом случае пришлось бы затрагивать стабильный, уже завершенный существующий уровень. Поэтому состояние окисления +7 самый высокийи соответствующий оксид Mn2О7 — самый высокий уровень оксида марганца.
Чтобы закрепить все эти понятия, давайте рассмотрим структуру атома теллура и некоторые его свойства (см. рис. 13). Этот рисунок показывает, что теллур – неметалл, потому что, во-первых, он имеет шесть электронов на внешнем уровне, и, во-вторых, его символ находится внутри главная подгруппа над линией B – At. Поэтому его атом может и взять (пока не будет завершен внешний уровень, и отдать электроны. В результате, в отличие от металлов, неметаллический теллур может находиться в более низкой степени окисления (–2) и образуют летучие соединения с водородом (Н2Te). Высшее состояние окисления атома теллура (+6), как и в случае с металлами, соответствует номеру группы, и в этом состоянии окисления теллур образует высший оксид TeO3.

Задача 3.11. Нарисовать электронные конфигурации атомов Nа, Rb, СІ, I, Si, Sn. Определите свойства этих химических элементов, формулы их простейших соединений (с кислородом и с водородом).
- В химических реакциях принимают участие только только валентные электроныкоторые могут располагаться только на двух последних уровнях.
- Атомы металлов могут отдать эти электроны (все или некоторые), только приняв положительное состояние окисления.
- Атомы неметаллы можно принять (не хватает до восьми) электронов, в то время как он набирает отрицательный состояние окисления и отдает валентные электроны (все или некоторые), а принимает позитивный степень окисления.
Возникает вопрос: как сразу создать короткую электронную схему (валентное расположение электронов), не создавая длинных электронных конфигураций? Для этого необходимо помнить несколько простых правил.
1. Номер период соответствует числу энергетических уровней атомов химических элементов того же периода.
2. Номер группыобычно совпадает с числом валентность электроны (исключение составляют лишь подгруппы меди и железа).
3. подгруппа (главная или второстепенная) включает химические элементы, которые имеют одинаковое валентное распределение электронов Одинаковое распределение валентных электроновВ главных и второстепенных подгруппах элементов распределение электронов различно.
3.1. В элементах главной подгруппы все валентные электроны расположены за пределами например:
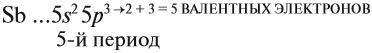
V группа, основная сторона → 5 валентность электроны
Поэтому для все химических элементов главной подгруппы пятой группы (пять валентных электронов) распределение этих электронов следующее:
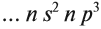
3.2. Для элементов вторичных подгрупп число внешних электронов не более двух.Например:
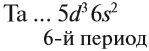
5 валентность электроны ← V группа, партия → 2 электроны на внешнем уровне*.
* Из-за “электронного сбоя” количество внешний электронов может быть ниже. Но количество валентность электронов не меняется, поэтому свойства элемента останутся прежними. Эти случаи обсуждаются на Уровне 2 Самоучителя, часть 1.
Для большинства химических элементов меньших подгрупп, имеющих два электрона на внешнем энергетическом уровне, оставшиеся (N – 2) валентных электрона будут находиться на d-подуровень внешнего энергетического уровня (N – номер группы), например:
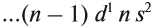
Вопрос. Для элементов, чьи группа для чего составлена эта запись?
Задача 3.12. Составьте короткие электронные схемы для атомов химических элементов под номерами 35 и 42, а затем расположите распределение электронов в этих атомах в соответствии с алгоритмом. Убедитесь, что ваше “предсказание” сбылось.
Теперь сравните свойства химических элементов, которые принадлежат к одной и той же подгруппе, например:
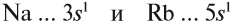
Что общего между атомами этих элементов? На внешнем уровне каждого атома находится один электрон, и они являются активными металлами. Металлическая активность имеет отношение к способности … отдавать Чем легче атом отдает электроны, тем сильнее его металлические свойства.
Что удерживает электроны в атоме? Их притяжение к ядру. Сайт ближе к электронов к ядру, чем сильнее они притягиваются ядром атома, тем труднее их “оторвать”.
Из этого мы делаем вывод: какой элемент – На сайте или Rb – какой из них легче отдает внешний электрон? Какой металл более активен? Очевидно, рубидий, потому что его валентные электроны находятся дальше от ядра (и более слабо удерживается ядром).
Заключение. В главных подгруппах Сверху вниз металлические свойства усиливаютсяПо мере увеличения радиуса атома валентные электроны меньше притягиваются к ядру.
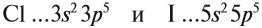
Оба химических элемента являются неметаллами, потому что им не хватает одного электрона для завершения внешнего уровня, и эти атомы будут активно привлекать недостающий электрон. В то же время, чем больше атом неметалла притягивает недостающий электрон, тем больше проявляются его неметаллические свойства (способность принимать электроны).
Что вызывает притяжение электрона? Из-за положительного заряда атомного ядра. Но в данном случае, чем ближе к ядру, тем сильнее их взаимное притяжение, тем активнее неметалл..
Давайте пойдем в заключениеКакой элемент обладает более сильными неметаллическими свойствами: хлор или йод? Хлор, конечно, потому что его свойства сильнее, чем у йода. валентные электроны ближе в ядро..
Выводы. Активность неметаллов в подгруппах уменьшается сверху внизпо мере увеличения радиуса атома, атому становится все труднее притягивать недостающие электроны.
Давайте сравним свойства кремния и олова:

На внешних уровнях обоих атомов находится по четыре электрона. Однако эти элементы находятся на противоположных сторонах периодической таблицы. На противоположных сторонах линии, соединяющей бор и астат (см. правило в уроке 2.1). Поэтому:
- кремний, символом которого является выше В – В строке, есть более сильное выражение неметаллические свойства;
- Олово, символом которого является ниже В – На линии, чем больше металлических металлик свойства;
Почему? Это происходит потому, что в атоме олова четыре валентных электрона находятся так далеко от ядра, что добавить недостающие четыре электрона сложно, в то время как пожертвовать электроны с пятого энергетического уровня довольно легко. В случае с кремнием возможны оба процесса, с преобладанием первого (перенос электронов).
- чем больше меньше электроны в атоме и далее металлик свойства;
- сайт больше внешние электроны в атоме, т.е. ближе к ядру, тем сильнее неметаллический неметаллические свойства.
Сравнить атомную структуру и свойства химических элементов одного периода:
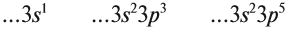
Вопрос. О каком периоде и о каких элементах идет речь?
Мы видим, что металлические свойства уменьшаются по мере увеличения числа внешних электронов, а неметаллические свойства увеличиваются. Если речь идет о большом периоде, где большинство элементов имеют 2 электрона на внешнем уровне (элементы более мелких подгрупп), то основная причина снижения металлических свойств в период это уменьшение атомного радиуса. Дело в том, что при увеличении заряда ядра в периоде, сила притяжения электронов к нему увеличивается, а радиус атома уменьшается:
Сравните: r (Ca) = 0,197 нм и r (Zn) = 0,139 нм
Вопрос. Какой металл более активен?
Для любого химического элемента периодической таблицы, основываясь на этих и других соображениях, приведенных в этой главе, можно построить Описывать свойства химического элемента в зависимости от его положения в периодической таблице.
1. Нарисовать схему строения атома, т.е. определить состав ядра, расположение электронов на энергетических уровнях и подуровнях
- Определите общее число электронов в атоме (по порядковому номеру);
- определить количество энергетических уровней (по номеру периода);
- определить количество внешний электроны (по типу подгруппы и номеру группы);
- указывают на количество электронов в целом уровень энергии, кроме предпоследнего;
- Рассчитать число электронов на предпоследнем уровне.
2. Определите число валентных электронов и число внешний электроны.
3. Определите, является ли данный химический элемент (в соответствии с его положением в PCCE) более сильным металлом или неметаллом.
4. Определите количество пожертвованных (отобранных) электронов.
5. Определите высшую и низшую степень окисления химического элемента.
6. Напишите химические формулы простейших соединений с кислородом и водородом для этих состояний окисления.
7. Определите природу оксида (см. урок 2.1) и напишите уравнения его реакции с водой.
8. Приведите уравнения реакций, характерных для данных веществ (п. 6) (см. урок 2).
Задача 3.13. Опишите атомы на следующей схеме сера, селен, кальций и стронций и свойства этих химических элементов. Каковы общие свойства их оксидов? Гидроксиды?
Если вы выполняли упражнения 3.11 и 3.12, то легко заметите, что не только атомы элементов одной подгруппы, но и их соединения имеют общие свойства и схожий состав. Это отражено в Периодический закон МенделееваСвойства химических элементов, а также свойства простых и сложных веществ, которые они образуют, находятся в периодической зависимости от заряда ядер их атомов.
Физический смысл периодического закона ясно: свойства химических элементов периодически повторяются, потому что конфигурации валентных электронов (расположение электронов на внешнем и предпоследнем уровнях) периодически повторяются.
Таким образом, химические элементы одной подгруппы имеют иметь одинаковые распределение валентных электронов и, следовательно аналогичный свойства.

- Многоликий протон.
- Определение количества нейтронов, протонов и электронов в атоме.
- Заряд атомного ядра, теория и примеры.
- Как работают атомы.
- Свойства атомов и их периодичность – ЗФТШ, МФТИ.
- Строение атома водорода (H), схема и примеры.
- Как определить число нейтронов, протонов и электронов в изотопе?.