Явление растворения металлов в электролитах используется в химических источниках энергии. Металлическая пластина, опущенная в раствор собственной соли, стремится раствориться в нем до некоторой степени. Эту тенденцию иногда называют упругостью растворения металла.
Что такое электродный потенциал
Электродный потенциал или электродный потенциал металла – это разность потенциалов, возникающая на границе раздела металл-раствор при погружении металла в раствор электролита, вследствие взаимодействия поверхностных ионов атомов металла, расположенных в узлах кристаллической решетки, с полярными молекулами воды, ориентированными на поверхности электрода. Это происходит в результате образования двойного электрического слоя, т.е. асимметричного распределения заряженных частиц на границе раздела.

Явление растворения металлов в электролитах используется в химических источниках энергии. Металлическая пластина, опущенная в раствор собственной соли, стремится раствориться в нем до некоторой степени. Эту тенденцию иногда называют упругостью растворения металла.
Цинковая пластина, помещенная в раствор сульфида цинка Zn SO4 Это растворяет молекулы цинка в виде положительно заряженных ионов. Поскольку атомы цинка выходят в виде положительно заряженных ионов, на цинковой пластине образуется избыток свободных электронов, и она заряжается отрицательно, а в слое жидкости у поверхности цинка образуется избыток положительных ионов, и поэтому этот слой заряжен положительно. Таким образом, на границе раздела жидкость-металл образуется двойной электрический слой, состоящий из пространственно разделенных зарядов противоположного знака.
Эти заряды будут противодействовать дальнейшему переносу металла в раствор – отрицательные пластины задерживают положительный ион металла, а положительный заряд электролита выталкивает ион металла обратно на пластину. Другими словами, электрическое поле двойного слоя на границе раздела металл-жидкость противодействует дальнейшему переносу ионов металла в раствор. Устанавливается баланс между химическими силами, присущими стремлению металла перейти в раствор, и противодействующими им электрическими силами.
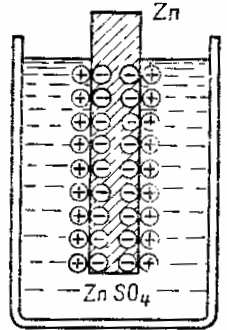
Диаграмма образования двойного электрического слоя на границе раздела металл/электролит
Таким образом, в результате растворения в электролите металлический электрод приобретает определенный электродный потенциал (или электрохимический потенциал) по отношению к электролиту, который зависит от материала электрода и состава электролита.
Однако электродные потенциалы могут иметь положительное значение. Это происходит, когда положительные ионы раствора переходят на электрод, заряжая его положительно, а слой электролита отрицательно, например, когда медная пластина погружается в достаточно концентрированный раствор сульфата меди (CuSO4).
Электрический двойной слой можно сравнить с конденсатором, одной из обкладок которого является поверхность металла, а другой – слой ионов в растворе на поверхности металла. Между противоположно заряженными клеммами возникает разность, или скачок потенциала.
Скачок потенциала на границе раздела электрод-раствор может служить мерой окислительно-восстановительной способности системы. Однако измерить такую разность потенциалов или, аналогично, разность потенциалов между двумя фазами не представляется возможным. Однако возможно измерение э.д.с. элементов, состоящих из интересующих электродов и одного электрода (одного и того же во всех случаях), потенциал которого условно принимается равным нулю.
Измеренный ток характеризует окислительно-восстановительный потенциал электрода по отношению к некоторому условному нулю. Полученное таким образом значение называется внутренним потенциалом металла.
Для измерения электродного потенциала любого металла необходимо поместить в электролит второй электрод, который, в свою очередь, будет иметь определенный электродный потенциал, зависящий от его материала. Следовательно, непосредственно можно измерить только алгебраическую сумму потенциалов двух электродов.
По этой причине электродные потенциалы различных материалов определяются относительно стандартного электрода (водородного электрода, потенциал которого условно принимается равным нулю).
Для измерения можно использовать и другие эталонные электроды, потенциал которых известен по отношению к стандартному водородному электроду. Этот потенциал также должен быть найден путем измерения э.д.с. цепь, состоящая из выбранного электрода сравнения и стандартного водородного электрода.
Если испытательный электрод сопряжен со стандартным водородным электродом и является отрицательным, внутреннему потенциалу присваивается знак “-“, в противном случае – знак “+”.
Например, измеренный таким образом электродный потенциал в растворе соответствующей соли металла составляет -0,76 В для цинка, +0,34 В для меди и +0,8 В для серебра. Значение э.ф.с. для данного элемента определяется путем вычитания более отрицательного потенциала из более положительного.
Если две металлические пластины с разными электродными потенциалами поместить в подходящий электролит, например, в раствор серной кислоты (H2SO4), вольтметр, приложенный к этим пластинам, покажет напряжение между ними чуть более 1 В.
Это напряжение, называемое в данном случае электродвижущим потенциалом гальванической пары, возникает в результате разности потенциалов между электродами из меди, имеющей небольшой положительный потенциал, и цинка, имеющего значительный отрицательный потенциал. Таким устройством является простейший гальванический элемент – вольтов элемент.
В гальваническом элементе химическая энергия преобразуется в электрическую, и электрическая работа может быть выполнена за счет использования энергии химической реакции.

Измерение энергии в гальванических элементах должно производиться при отсутствии тока в цепи элемента. В противном случае измеренная ЭДС будет меньше значения, определяемого как разница между равновесными потенциалами двух электродов. Действительно, определенная концентрация электронов на электродах соответствует равновесному потенциалу: она ниже на более положительном электроде и выше на более отрицательном. Соответственно меняется и структура части двойного слоя в растворе.
Измерение эффективности элемента без протекания тока обычно выполняется методом компенсации. Для этого необходимо иметь стандарт ЭДС. Этот стандарт является так называемым нормальным элементом. Обычно используемым стандартом является простой ртутно-кадмиевый элемент Вестона, выходное напряжение которого составляет 1,01830 В при 20 °C.
Если вам понравилась эта статья, пожалуйста, поделитесь ею в социальных сетях. Это поможет нашему сайту развиваться!
решетки, специфическая (некулоновская) адсорбция полярных молекул на электроде и др. Эти два последних явления приводят к тому, что электродный потенциал становится ненулевым даже в условиях, когда поверхностный заряд металла равен нулю (см. зарядный потенциал).Abs.
Расчет стандартных электродных потенциалов
Электродный потенциал не может быть определен эмпирически.
Потенциал гальванического элемента определяется “парой” электродов. Поэтому невозможно определить значение для каждого электрода в паре, используя эмпирически выведенные потенциалы гальванических элементов. Для этого водородный электрод, для которого потенциал точно определен и составляет 0,00 В, и любой электрод, для которого электронный потенциал еще не известен, можно соотнести со стандартным водородным электродом для образования гальванического элемента – и в этом случае потенциал гальванического элемента дает потенциал неизвестного электрода.
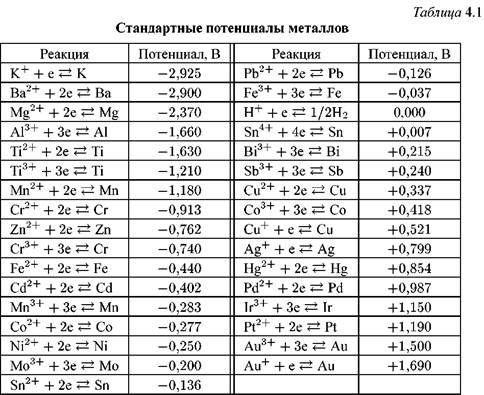
Поскольку электродные потенциалы традиционно определяются как потенциалы восстановления, при расчете общего потенциала ячейки знак окисляющего металлического электрода должен быть обратным. Обратите также внимание, что потенциалы не зависят от числа электронов, переданных в полуреакции (даже если оно варьируется), поскольку они рассчитаны для 1 моль переданных электронов. Поэтому необходимо соблюдать осторожность при расчете любого электродного потенциала на основе двух других.
Fe3++ 3e-→ Fe(твердый) -0.036 В

Fe2++ 2e-→ Fe(dw) -0.44 В
Чтобы получить третье уравнение:
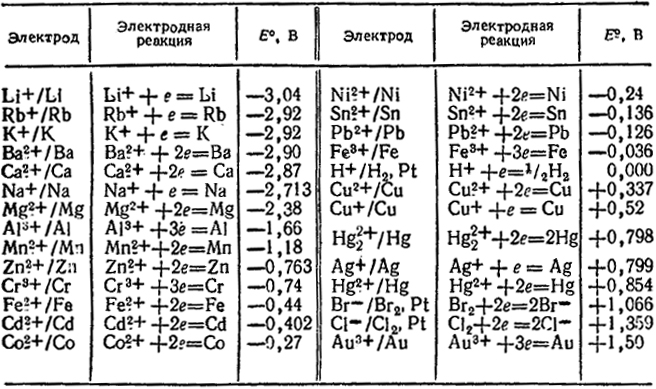
Умножьте потенциал первого уравнения на 3, переверните второе уравнение (поменяйте знак) и умножьте его потенциал на 2. Сложение этих двух потенциалов дает стандартный потенциал из третьего уравнения.
Abs. Электродный потенциал отдельного электрода определить невозможно, поэтому всегда измеряется разность потенциалов между исследуемым электродом и стандартным эталонным электродом. Электродный потенциал равен электромагнитному потенциалу электрохимической цепи, состоящей из испытуемого электрода и стандартного электрода (диффузионный потенциал между различными электролитами, обусловленный различной скоростью движения ионов, в данном случае должен быть исключен). Для водных растворов используется водородный электрод (Pt, H2В качестве электрода сравнения в водных растворах принят водородный потенциал (Pt [0,101 МПа] | H+ [a=1]), потенциал которого при давлении водорода 0,101 МПа и термодинамической активности ионов H+ в растворе, равной 1, равен нулю (водородная шкала электродных потенциалов). На схемах водородный электрод всегда пишется слева; например, потенциал медного электрода в растворе соли меди равен ЭДС цепи Pt, H2|HClCuCl2|Cu|Pt (две пунктирные линии означают, что потенциал диффузии на HC1 и CuC12 была удалена).
Если испытываемый электрод находится в стандартных условиях, когда активности всех ионов, определяющих электродный потенциал, равны 1, а давление газа (для газовых электродов) составляет 0,101 МПа, то значение электродного потенциала называется стандартным (обозначается E°).
Она связана с нормированным изменением энергии Гиббса и константой равновесия Kр константа равновесия K r электрохимической реакции, связана с константой равновесия K r: где F – число Фарадея, n – число электронов на реакцию, R – газовая постоянная и T – абсолютная температура. Значения E° электрохимических систем относительно водородного электрода и взаимодействий r, происходящих на электродах, приведены в специальных таблицах (подробнее см. Стандартный потенциал).
Зависимость электродного потенциала от термодинамической активности ai участников электрохимической реакции выражается уравнением Нернста:
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛЭлектродный потенциал – это электростатическая разность потенциалов между электродом и контактирующим с ним электролитом. Возникновение электродного потенциала обусловлено пространственным разделением зарядов противоположного знака на границе фаз и образованием двойного электрического слоя. Пространственное разделение зарядов на границе между металлическим электродом и раствором электролита обусловлено следующими явлениями: перенос ионов из металла в раствор при установлении электрохимического равновесия, кулоновская адсорбция ионов из раствора на поверхности металла, вытеснение электронного газа из рамки положительно заряженных ионов кристаллической решетки, специфическая (некулоновская) адсорбция ионов или полярных молекул р-ра на электроде и др. Последние два явления приводят к тому, что электродный потенциал не равен нулю, даже если поверхностный заряд металла равен нулю (см. Потенциал нулевого точечного заряда).
Abs. Электродный потенциал отдельного электрода определить невозможно, поэтому всегда измеряется разность потенциалов между исследуемым электродом и стандартным эталонным электродом. Электродный потенциал равен электромагнитному потенциалу электрохимической цепи, состоящей из тестируемого электрода и стандартного электрода (диффузионный потенциал между различными электролитами, обусловленный различием ионных скоростей, в данном случае должен быть исключен). Для водных растворов используется водородный электрод (Pt, H2Водородный потенциал (Pt [0,101 МПа] | H+ [a= 1]) в водных растворах, потенциал которого при давлении водорода 0,101 МПа и термодинамической активности ионов H+ в растворе, равной 1, принят за эталонный равен нулю (водородная шкала электродных потенциалов). На схемах водородный электрод всегда пишется слева; например, потенциал медного электрода в растворе соли меди равен эдс цепи Pt, H2|HCl CuCl2|Cu|Pt (две пунктирные линии означают, что потенциал диффузии на HC1 и CuC12 были удалены).
CuCl2|Cu|Pt (две пунктирные линии означают, что потенциал диффузии на HC1 и CuC12 были удалены).
Если испытываемый электрод находится в стандартных условиях, когда активности всех ионов, определяющих электродный потенциал, равны 1, а давление газа (для газовых электродов) составляет 0,101 МПа, то значение электродного потенциала называется стандартным потенциалом (обозначается E°).
Она связана с нормированным изменением энергии Гиббса 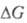 и константа равновесия Kр константа равновесия K r электрохимической реакции, связана с константой равновесия K r:
и константа равновесия Kр константа равновесия K r электрохимической реакции, связана с константой равновесия K r: 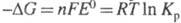 где F – число Фарадея, n – число электронов на реакцию, R – газовая постоянная и T – абсолютная температура. Значения E° электрохимических систем относительно водородного электрода и взаимодействий r, происходящих на электродах, приведены в специальных таблицах (подробнее см. Стандартный потенциал).
где F – число Фарадея, n – число электронов на реакцию, R – газовая постоянная и T – абсолютная температура. Значения E° электрохимических систем относительно водородного электрода и взаимодействий r, происходящих на электродах, приведены в специальных таблицах (подробнее см. Стандартный потенциал).
Зависимость электродного потенциала от термодинамической активности ai участников электрохимической реакции выражается уравнением Нернста:
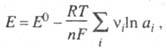
где vi – стехиометрический коэффициент. Электродный потенциал отрицателен для исходных веществ и положителен для продуктов реакции.
Если через электрод протекает ток, электродный потенциал отклоняется от своего равновесного значения из-за конечной скорости процессов, происходящих непосредственно на границе раздела электрод-электролит (см. Поляризация).
Или в качестве альтернативы,
Значительные условности.
Исторически сложилось, что существуют две конвенции для определения электродного потенциала:
- Конвенция “Нернст – Льюис – Латимер” (иногда называемая “американской” конвенцией),
- Конвенция Гиббса-Оствальда-Стокгольма (иногда называемая “европейской” конвенцией).
В Стокгольме в 1953 году ИЮПАК признал каждую из этих конвенций приемлемой, но единогласно рекомендовал называть “электродным потенциалом” только величину, выраженную в соответствии с соглашением (2). Чтобы избежать возможной двусмысленности, определенный таким образом электродный потенциал может также называться Электродный потенциал Гиббса-Стокгольма . В обоих соглашениях стандартный водородный электрод определяется как имеющий потенциал 0 В. В обоих соглашениях также оговорено, что знак E для реакции в полуэлементе, когда она записана как восстановление.
Основное различие между двумя конвенциями заключается в том, когда реакция полуэлемента обращается вспять, согласно написанному в соответствии с системой (1), знак E также переключается, тогда как в соглашении (2) этого не происходит. Логика, лежащая в основе изменения знака E является сохранение правильной знаковой связи с изменением свободной энергии Гиббса, задаваемой Δ G = – nFE, где n – число электронов, участвующих в реакции, и F – постоянная Фарадея. Предполагается, что полуреакция уравновешивается соответствующей полуреакцией SHE. Поскольку Δ G меняет знак при обратной записи реакции, аналогично сторонники конвенции (1) утверждают, что знак Е . Сторонники соглашения (2) утверждают, что все регистрируемые электродные потенциалы должны соответствовать электростатическому знаку относительной разности потенциалов.
Запишем значения стандартных электродных потенциалов металлов из таблицы 9.1: φ 0 = -0,44 В, φ 0 = -0,25 В. Поскольку φ 0 < φ 0 , железо будет действовать как анод, а никель как катод.
Понятие электродного потенциала
Электроды– Электрохимические системы, состоящие из металла или полупроводника, погруженного в раствор электролита или расплавленный электролит. Они фактически представляют собой металлические или графитовые изделия (проводники первого рода) в электропроводящей среде (проводники второго рода). Носителями свободных зарядов в проводниках первого рода являются электроны, а в проводниках второго рода – ионы обоих знаков.
Металлы, как правило, имеют кристаллическую структуру. Положительные ионы (катионы), которые находятся в равновесии с электронным газом, расположены в узлах кристаллической решетки:
Когда металл погружается в раствор, начинается сложное взаимодействие между металлом и компонентами раствора. Катионы металла выходят в электролит, а катионы из электролита встраиваются в кристаллическую решетку металла. Со временем между электродом и электролитом устанавливается равновесие. В зависимости от того, куда смещается это равновесие, поверхность металла приобретает более высокий или более низкий потенциал.
Перераспределение заряда на границе раздела металл-раствор приводит к образованию двойного электрического слоя (рис. 9.1) и скачку потенциала между металлом и раствором.
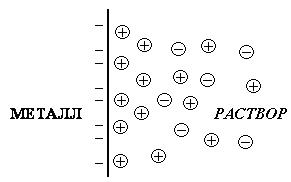 |
| Рисунок 9.1: Двойной электрический слой на границе раздела металл-раствор |
Потенциал электрода, погруженного в электролит, называется электродным потенциалом. Его значения зависят от многих факторов: материала электрода, состава электролита, температуры, давления и т.д. Электродный потенциал измеряется относительно выбранного эталонного электрода, потенциал которого принимается за ноль. В качестве электрода сравнения обычно используется стандартный водородный электрод.
Стандартный электродный потенциал (j 0 )это потенциал металла, погруженного в раствор собственной соли и измеренный относительно водородного электрода в стандартных условиях. Стандартные условия: концентрация ионов в растворе 1 моль/л, температура Т = 298 K, давление Р = 1.01325∙10 5 Па.
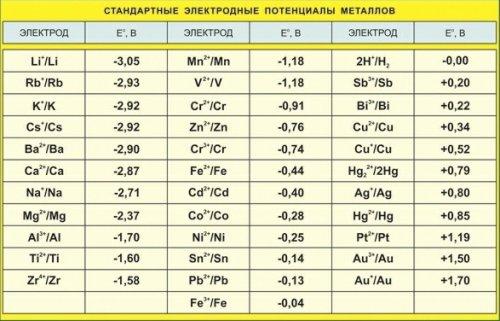
Был получен ряд стандартных электродных потенциалов (табл. 9.1), что позволяет количественно характеризовать электрохимическую активность металлов. Чем меньше значение φ 0 , тем более выражены восстановительные свойства металла, т.е. он легче отдает электроны и легче окисляется. Чем выше значение φ 0 , тем сильнее окислительные свойства катиона металла в растворе.
Стандартные электродные потенциалы φ 0 некоторых металлов
| Электрод | Электродный потенциал, V | Электрод | Электродный потенциал, V |
| Li + /Li | –3,05 | Cd 2+ /Cd | –0,40 |
| Rb + /Rb | –2,93 | Co 2+ /Co | –0,28 |
| K + /K | –2,92 | Ni 2+ /Ni | –0,25 |
| Ba 2+ /Ba | –2.90 | Sn 2+ /Sn | –0,136 |
| Ca 2+ /Ca | –2,87 | Pb 2+ /Pb | –0,127 |
| Na + /Na | –2,71 | 2H + /H | 0,00 |
| Mg 2+ /Mg | –2,37 | Sb 3+ /Sb | +0,20 |
| Al 3+ /Al | –1,70 | Bi 3+ /Bi | +0,22 |
| Ti 2+ /Ti | –1,60 | Cu 2+ /Cu | +0,34 |
| V 2+ /V | –1,18 | Ag + /Ag | +0,85 |
| Mn 2+ /Mn | –1,18 | Hg 2+ /Hg | +0,85 |
| Zn 2+ /Zn | –0,76 | Pt 2+ /Pt | +1,19 |
| Cr 3+ /Cr | –0,74 | Au 3+ /Au | +1,5 |
| Fe 2+ /Fe | –0,44 |
Уравнение Нернста используется для расчета электродных потенциалов в условиях, отличных от стандартных:
Где T – температура, K;
F – число Фарадея, равное 96 500 Cl/моль;
R – универсальная газовая постоянная, 8,314 Дж/(моль.К);
n – число электронов, участвующих в элементарном акте окислительно-восстановительного процесса;
– концентрация ионов металла в растворе, моль/л.
На стр. T = 298 K формула Нернста принимает вид:
Гальванический элемент
Гальванический элемент – это химический источник тока, в котором энергия, выделяемая в результате окислительно-восстановительной реакции на электродах, преобразуется непосредственно в электрическую энергию..
Типичный гальванический элемент можно представить на примере элемента Даниэля-Якоби (рисунок 9.2).
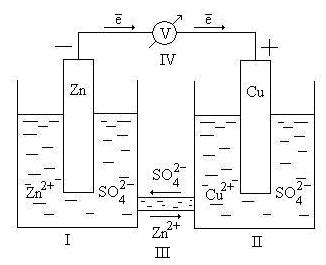
Рисунок 9.2: Схема гальванического элемента Даниэля-Якоби
Имеется мензурка, содержащая раствор ZnSO4 в воде с погруженной в нее цинковой пластиной; II – стакан, содержащий CuSO4 в воде с погруженной в нее медной пластиной; III – солевой мостик (электролитический ключ), который обеспечивает поток катионов и анионов между растворами; IV – вольтметр (необходим для измерения электромагнитного поля, но не является частью гальванического элемента).
Стандартный электродный потенциал цинкового электрода . Стандартный электродный потенциал медного электрода . Поскольку атомы цинка будут окислены:
| Zn – 2ē = Zn 2+ . | (а) |
Электрод, на котором происходит реакция окисления или который отправляет катионы в электролит, называется электродом анод. В рассматриваемом гальваническом элементе роль анода заключается в следующем цинк электрод. Поскольку стандартный потенциал цинкового электрода ниже потенциала медного электрода, цинковому электроду присваивается заряд “-“, а медному электроду – заряд “+”.
Электроны, высвобождаемые в процессе окисления, передаются меди через внешнюю цепь (электрический ток).
На медьэлектрода процесс восстановления катионов электролита Cu 2+ :
| Cu 2+ +2ē = Cu. | (б) |
Электрод, на котором происходит реакция восстановления или который принимает катионы из электролита, называется электродом катод.
Через электролитический ключ ионы в растворе перемещаются: анионы SO4 2- к аноду, катионы Zn 2+ к катоду. Движение ионов в растворе замыкает электрическую цепь гальванического элемента.
Реакции (a) и (b) называются электродными реакциями.
Сложив уравнения процессов, происходящих на электродах, мы получим общее уравнение окислительно-восстановительной реакции, происходящей в гальваническом элементе:
| Zn + Cu 2+ = Zn 2+ + Cu | (в) |
или, с учетом анионов в растворе:
| Zn + CuSO4= ZnSO4+ Cu. | (г) |
В общем случае полное уравнение окислительно-восстановительной реакции, происходящей в любом гальваническом элементе, может быть представлено как
| IА + ЯК n+ Á MeА n+ + MeК, | (д) |
где подстрочные индексы A и K означают анодный и катодный металлы, соответственно.
Реакции c) – e) называются проводящие реакцииреакции.
Символическое обозначение (схема) гальванического элемента выглядит следующим образом:
Часто вместо растворов обозначают только катионы, содержащиеся в растворе:
Схема гальванического элемента Даниэля-Якоби выглядит следующим образом:
Максимальная разность потенциалов между электродами, которая может быть получена при работе гальванического элемента, называется электродвижущая сила (ЭМП) клетки Е. Этот показатель рассчитывается по формуле;
| Е= φк – φа, | (9.4) |
где φк и φа – электродные потенциалы катода и анода, соответственно.
Значение ЭДС элемента Даниэля-Якоби при стандартных условиях составляет:
Е = +0,34 – (-0,76) = 1,10 В.
Электродвижущая сила Е это мера способности гальванического элемента производить электрическую работу во внешней цепи.
Электрическая работа определяется максимальной полезной работой, совершаемой в химической реакции, которая равна изменению изобарно-изотермического потенциала ∆G процесса. Соотношение между ∆G а ЭДС описывается уравнением:
| ∆G = –nFE, | (9.5) |
где n – число электронов в элементарном окислительно-восстановительном акте, F – является числом Фарадея.
Величина изменения изобарно-изотермического потенциала токогенерирующей реакции при стандартных условиях ∆G 0 связана с константой равновесия этой реакции Кконстанта равновесия по соотношению
Гальванические элементы являются первичными (одноразовыми) химическими источниками энергии (ХИЭ). Вторичные (многоразовые) CIC представляют собой батареи. Процессы, происходящие при разрядке и зарядке батарей, являются взаимными.
Гальванические элементы, в которых электроды изготовлены из одного и того же металла и помещены в растворы с различной концентрацией их солей, называются концентрационными элементами. Концентрация. Функцию анода в таких элементах выполняет металл, погруженный, например, в солевой раствор более низкой концентрации:
Пример 1. Составьте схему гальванического элемента, в котором происходит реакция: Mg + ZnSO4 = MgSO4 + Zn. Что является катодом и анодом в этом элементе? Напишите уравнения для процессов, происходящих на этих электродах. Рассчитайте ЭДС этого элемента при стандартных условиях. Рассчитайте константу равновесия для реакции образования тока.
Решение
В таблице приведены значения стандартных электродных потенциалов для систем Zn/Zn 2+ и Mg/Mg 2+. :
Потому что магниевый электрод действует как анод, а цинковый электрод – как катод. Схема гальванического элемента выглядит следующим образом:
На аноде происходит процесс окисления:
На катоде происходит восстановление катионов окружающей среды:
Стандартная ЭДС гальванического элемента
Используя уравнения (9.5) и (9.6), рассчитаем константу равновесия реакции, генерирующей ток:
Потенцируя, мы находим Кравно = 3,5 ∙10 54 .
С сайта К >>1, то реакция создания тока практически необратима.
Пример 2. Составьте схему гальванического элемента, состоящего из цинкового и серебряного электродов, погруженных в растворы их солей. Концентрации ионов в растворах: CZn 2+ = 0,1 моль/л, CAg + = 0,01 моль/л. Определите, какой электрод является катодом, а какой – анодом. Напишите уравнения для реакций, происходящих на электродах, и суммарное уравнение для реакции генерирования тока в гальваническом элементе. Рассчитайте ЭДС ячейки.
Решение
Поскольку концентрации ионов не равны единице, сначала рассчитаем электродные потенциалы по формуле Нернста. Если в описании задачи не указано значение температуры, ее следует принять за стандартную. Т = 298 К. Поэтому мы будем использовать уравнение (9.2):
Численное значение концентрации определим по формуле Нернста, используя данные таблицы 9.1:
Расчет показывает, что . Поэтому цинковый электрод действует как анод, а серебряный электрод – как катод.
Диаграмма гальванического элемента:
Давайте рассчитаем ЭДС ячейки, используя уравнение (9.4):
Теперь запишите электродные реакции. На аноде происходит процесс окисления:
а на катоде происходит процесс восстановления:
Суммируя уравнения электродных процессов (с учетом равенства числа принятых и отданных электронов), получаем общее уравнение реакции генерации тока: Zn + 2Ag + = Zn 2+ + 2Ag.
Задачи
221–226 Напишите уравнения катодного и анодного процессов и составьте схему гальванического элемента, в котором протекает следующая реакция (см. таблицу). Рассчитайте константу равновесия для реакции и ЭДС ячейки, используя стандартные электродные потенциалы.
| Номер задания | Реакция | Ответить |
| Sn + PbCl2 = SnCl2 + Pb | Кр = 2,0; E = 9∙10 – 3 B | |
| Zn + Pb(NO3)2 = Zn(NO3)2 + Pb | Кр = 3,5∙10 21 ; E = 0,633 B | |
| Zn + 2AgNO3 = Zn(NO3)2 + 2Ag | Кр = 8,7∙10 52 ; E = 1,56 B | |
| Ni + 2AgNO3 = Ni(NO3)2 + 2Ag | Кр = 3,8∙10 35 ; E = 1,05 B | |
| Zn + CdSO4 = ZnSO4 + Cd | Кр = 1,56∙10 12 ; E = 0,36 B | |
| Mg + Ni(NO3) 2 = Mg(NO3)2 + Ni | Кр = 1,7∙10 8 ; E = 8,23 B |
227–233Рассчитайте значения электродных потенциалов металла, который является анодом, при различных концентрациях раствора: 10; 0,1; 0,01; 0,001 моль/л. Концентрация раствора, в который погружен катод, постоянна и равна 1 моль/л. Определите ЭДС.
Постройте график зависимости ЭДС гальванического элемента от логарифма концентрации раствора, в который погружен анод. Напишите уравнение реакции генерирования тока в гальваническом элементе.
| задачи нет. | Гальванический элемент |
| Ni |Ni 2+ || 2Ag + |2Ag | |
| Zn | Zn 2+ || Cr 3+ | | | Cr | |
| H2|2H + |Cu 2+ |Cu | |
| Mg | Mg 2+ ||Ni 2+ |Ni | |
| Al|Al 3+ ||Fe 2+ |Fe | |
| Zn | Zn 2+ || Pb 2+ | Pb | |
| Mg| Mg 2+ ||Bi 3+ |Bi |
234–236 Одним электродом гальванического элемента является металл (см. таблицу), погруженный в раствор своей соли с концентрацией ионов 0,01 моль/л, а другим – водородный электрод. ЭДС этой ячейки составляет ЕНапишите уравнения катодной и анодной реакций, составьте схему гальванического элемента. Рассчитайте потенциал водородного электрода и концентрацию ионов водорода в растворе. Т = 298 K.
| Проблемы нет. | металл | Е, В | Ответить |
| Zn | 0,701 | 0,01 | |
| Cu | 0,371 | 0,03 | |
| Ni | 0,250 |
237–240 Запишите уравнения электродных реакций и составьте схему гальванического элемента, работа которого выражается уравнением, приведенным в таблице. Определите, какой электрод является катодом, а какой – анодом. Рассчитайте значения электродных потенциалов при концентрациях анодных растворов С1 и катод С2 (см. таблицу). Определите ЭДС этого элемента.
| Проблемы нет. | Реакция | С1, моль/л | С2, моль/л | Ответы |
| Fe + 2Ag +2 Á Ag + Fe 2+ | 0,01 | 0,1 | 1,24 | |
| Ni + Cu 2+ Á Ni 2+ + Cu | 0,1 | 0,1 | 0,59 | |
| Mg + Pb 2+ Á Mg 2+ + Pb | 0,01 | 2,184 | ||
| Zn + Ni 2+ Á Ni + Zn 2+ | 0,01 | 0,01 | 0,513 |
241–244 Составьте схему гальванического элемента, состоящего из двух металлов Me1 и я2погруженные в раствор собственных солей ионной концентрации С1 и С2 (см. таблицу). Определите, какой электрод является катодом, а какой – анодом. Напишите уравнения реакций, происходящих на этих электродах, а также суммарное уравнение реакции, генерирующей ток в гальваническом элементе. Рассчитайте ЭДС ячейки.
| Проблемы нет. | Я1 | Я2 | С1, моль/л | С2, моль/л | Ответы |
| Zn | Ni | 0,01 | 0,01 | 0,51 В | |
| Fe | Cu | 0,1 | 0,01 | 0,75 В | |
| Fe | Ag | 0,001 | 0,01 | 1,21 В | |
| Mg | Fe | 0,01 | 1,99 В |
245–247 Рассчитайте значения электродных потенциалов металлов, перечисленных в тексте задачи, при концентрациях следующих растворов С1 (для 1 металла) и С2 (для 2-го металла). Определите анод и катод. Рассчитайте ЭДС этого элемента.
Выполните те же расчеты для концентраций растворов, уменьшенных в 10 раз. Изменится ли ЭДС?
Приведите уравнения электродных реакций.
| НОМЕР ЗАДАЧИ | Ме1 | Ме2 | С1, моль/л | С2 , моль/л | Ответы |
| Zn | Cu | 0, 1 | 0, 1 | 1,10 В | |
| Аль | Ni | 0,1 | 0,01 | 1,41 В | |
| Mg | Ni | 0,01 | 0,1 | 2,15 В |
248 Какой гальванический элемент называется концентрационным? Составьте его схему. Напишите уравнения анодного и катодного процессов, рассчитайте ЭДС. Гальванический элемент состоит из серебряных электродов, помещенных: первый в 0,01 М, а второй в 0,1 М раствор AgNO.3.
249 Нарисуйте схему двух гальванических элементов, в одном из которых анодом будет никель, а катодом – никель. Напишите уравнения реакций для каждого из них на аноде и катоде и рассчитайте ЭДС гальванического элемента при стандартных условиях. Если концентрацию каждого иона уменьшить в 10 раз, изменится ли ЭДС этого элемента?
250 Железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему гальванического элемента и напишите электронные уравнения процессов, происходящих на катоде и аноде.
КОРРОЗИЯ МЕТАЛЛОВ
Коррозия – Самопроизвольное разрушение металлов в результате их взаимодействия с окислителями в окружающей среде.
Это окислительно-восстановительный процесс, в котором металл выступает в качестве восстановителя. Основной причиной коррозии является термодинамическая нестабильность металла в окружающей среде и его способность переходить в более стабильное (окисленное) состояние.
Коррозию иногда называют ржавчиной. Ржавление – это коррозия железа и его сплавов с образованием продуктов коррозии, состоящих в основном из гидроксидов железа различной степени гидратации, желто-коричневого цвета. Цветные металлы корродируют, но не ржавеют. Коррозия классифицируется в зависимости от характера повреждения селективный, непрерывный (равномерные и неравномерные) локально (изъязвление, обесцвечивание или изъязвление), коррозионное растрескивание под напряжением и межкристаллическая коррозия. Коррозия может быть почвенной коррозией, атмосферной коррозией, электролитической коррозией, газовой коррозией и коррозией блуждающих токов, в зависимости от среды, в которой происходит процесс. В зависимости от механизма протекания и условий окружающей среды коррозия подразделяется на химическую и электрохимическую.
Химическая коррозия происходит в газовой среде при повышенных температурах (в отсутствие влаги) или в неэлектролитических жидкостях. Суть этого типа коррозионного процесса сводится к окислительно-восстановительной реакции, осуществляемой путем прямого переноса электронов металла на окислитель. Окислителем могут быть газы, такие как O , SO , Cl , HCl и т.д. Коррозии также благоприятствует H2S, CO . В результате реакции на поверхности металла образуются слои оксидов, сульфидов, хлоридов и т.д.
Развитие коррозии происходит путем переноса катионов металла, молекул окислителя или электронов через образовавшийся слой. Если слой плотный, непрерывный и хорошо сцеплен с металлом, дальнейшее окисление металла происходит очень медленно. Такие пленки можно использовать для защиты металлов от коррозии. Напротив, рыхлый слой не может защитить металл от дальнейших окислительно-восстановительных взаимодействий с окружающей средой. Защитные свойства образующихся продуктов коррозии определяются путем расчета коэффициента охрупчивания F:
где V – молярный объем продуктов коррозии (оксид, хлорид, сульфид и т.д.);
V – молярный объем металла, используемого для образования оксида;
М – молярная масса продуктов коррозии;
r – плотность металла;
n – число атомов металла в продукте коррозии;
А – атомный вес металла;
r – плотность продукта коррозии.
Если F < 1, образуется пленка, которая частично покрывает поверхность металла (рыхлая пленка). Непрерывная пленка с защитным эффектом образуется только в том случае, если 1 < F < 2,5. Если коэффициент хрупкости F > 2,5, в пленке возникают напряжения, которые разрушают ее и нарушают непрерывность (пленка набухает и трескается).
Пример 1. При химической коррозии железа в сухом воздухе, содержащем газообразную H2S и O2образуют слои FeS и FeO. Напишите уравнения образования этих соединений. Рассчитайте коэффициент охрупчивания F и сделайте вывод о защитных свойствах пленок. Плотность r = 7,87; r = 4,7; r = 5,7 г/см .
Решение
Пленки образуются при взаимодействии металла с агрессивной средой в результате следующих реакций:
Подставив численные значения в (10.1), получим коэффициент хрупкости:
Поскольку для сульфидной пленки F > 2,5, возможно растрескивание и разрыв пленки.
Критерий F для оксидной пленки лежит в диапазоне 1 < F < 2,5. Поэтому слой FeO является твердым и обладает хорошими защитными свойствами.
Электрохимическая коррозия – Самопроизвольное разложение металлов в присутствии электролита вследствие образования гальванических паров при контакте различных металлов, например, запорной арматуры и трубопроводов или множества гальванических микроэлементов на поверхности металлического сплава. Наиболее важные виды электрохимической коррозии включают атмосферную коррозию, подземную коррозию, коррозию в морской и пресной воде, сероводородную коррозию, кислотную коррозию, щелочную коррозию, коррозию в расплавленных солях, в водно-органических и органических средах. Основное различие между электрохимической и химической коррозией заключается в пространственном разделении реакций окисления металла и восстановления окислителя, происходящих на катодном и анодном участках. При электрохимической коррозии процессы окисления и восстановления происходят в областях с различной химической структурой или физическими условиями поверхности, т.е. химическая и энергетическая неоднородность. Эта неоднородность может возникать при различных фазовых и химических составах металла и сплава, при наличии примесей в металле, при различной химической обработке, при различной концентрации окружающего электролита, при неоднородности и различной толщине слоев продуктов коррозии и т.д.
Количественно различная поверхностная активность может быть охарактеризована величиной электродного потенциала φ, возникающего на границе раздела металл-раствор (табл. 9.1). Более активные поверхности имеют более низкое значение электродного потенциала (более отрицательное) и называются анодные участки. Области с меньшей активностью называются области катода.
На анодных участках происходит окисление металла, т.е. его разложение:
где Me обозначает катионы металла, переходящие в раствор;
Электроны остаются внутри металла и перемещаются от анодных участков к катодным, с которыми они находятся в непосредственном контакте и где происходит восстановление ионы и молекулы окислителя в коррозионной среде. В зависимости от состава среды происходят следующие процессы:
– в нейтральной или слабощелочной среде:
Наиболее вероятный катодный процесс в нейтральной среде в присутствии растворенного воздуха (атмосферная коррозия, почвенная коррозия, влажный воздух) выглядит следующим образом:
Пример 2. Нарисуйте электронные уравнения для катодного и анодного процессов коррозии железо-никелевого сплава в соляной кислоте и во влажном воздухе. Каков состав продукта коррозии?
Решение
Запишите значения стандартных электродных потенциалов металлов из таблицы 9.1: φ 0 = -0,44 В и φ 0 = -0,25 В. Поскольку φ 0 < φ 0 , железо будет действовать как анод, а никель как катод.
В кислой среде электронные уравнения процессов выглядят следующим образом:
– анодная реакция: Fe 0 – 2ē = Fe 2+ ;
– катодная реакция: 2H + + 2ē = H 0 2.
Продуктами коррозии являются хлорид железа FeCl и водород.
Во влажном воздухев катодной и анодной областях происходят следующие реакции:
– анодная реакция: Fe – 2ē = Fe ;
– катодная реакция: 2H O + O + 4ē = 4OH .
Продукты коррозии Fe + 2OH = Fe(OH) .
В присутствии влаги и кислорода железо дополнительно окисляется до трехвалентного состояния:
4Fe(OH) + 2H O + O = 4Fe(OH) .
Для количественной оценки коррозионной стойкости металлов используется масса (j) и значения глубины (D) используются для количественной оценки коррозионной стойкости металлов.
Скорость химической реакции определяется соотношением:
| г/м 2. ч (или г/м 2. год) , | (10.2) |
где ∆m – изменение массы образца, g
– время коррозии, ч или год;
S – площадь коррозии, м 2 .
Индекс глубины коррозии P равен:
| P = , мм/год, | (10.3) |
где ∆h – толщина разрушенного металла в момент времени t.
Значения P i j связаны родственными отношениями:
если j измеряется в г/м 2,
если j измеряется в г/м 2. h,
где r – плотность металла, г/см 3 .
Общая коррозия системы обычно оценивается с использованием вышеуказанных данных.
Защита от коррозии
Поскольку, как отмечалось выше, процесс электрохимической коррозии состоит из взаимосвязанных катодной и анодной реакций, замедление одной из них приводит к снижению скорости коррозии в целом.
Методы защиты от коррозии можно разделить на три группы:
– Воздействие металла;
– воздействие агрессивных средств массовой информации;
– комбинированные методы защиты.
К первая группа являются:
(a) сплавление металлов – образование защитного поверхностного слоя или введение элементов, снижающих катодную или анодную активность сплава;
(b) обработка поверхности металла – термическая обработка, напыление, механическая обработка (клепка и т.д.), модификация ржавчины на поверхности;
(c) нанесение защитных покрытий
(d) выбор коррозионностойких материалов;
д) рациональное проектирование – вывод отдельных структурных единиц из агрессивной среды.
Вторая группа Методы защиты включают:
(a) применение ингибиторов коррозии;
б) дегазация среды;
в) создание искусственных сред (обработка водных сред, использование нейтральных сред, сушка на воздухе).
Третья группа Методы защиты используют комбинацию вышеперечисленных методов.
Защитные покрытия можно разделить на органический (битум, краска, эмаль, лак) неорганический (оксидные, фосфатные, нитридные и другие слои), и гальванический (металлические, электролитические).
Неорганические (Химические) покрытия производятся путем обработки металла определенным химическим веществом. Когда этот химикат вступает в реакцию с поверхностью металла, образуется твердый слой неорганических соединений, который защищает металл от разрушения.
Гальваническое покрытие Покрытия делятся на катодные и анодные (рис. 10.1) в зависимости от соотношения стандартных электродных потенциалов защищаемого материала j 0 и покрытия j 0 . Если j 0 > j 0 , металл покрытия будет анодом, когда целостность защитного покрытия нарушена (анодное покрытие), а защищенный металл будет катодом.
Анодное покрытие очень эффективно, поскольку оно защищает защищаемый металл от деградации при разрушении. Примерами анодных покрытий по отношению к железу являются цинковые и магниевые покрытия на стали. Если j 0 < j 0 , то при разрушении покрытия металл, подлежащий защите, будет анодом, а металл покрытия - катодом (катодное покрытие). Катодные покрытия защищают металл до тех пор, пока эти покрытия являются непрерывными.
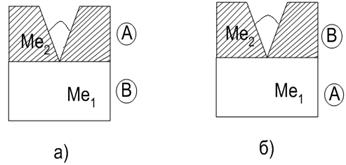
Рисунок 10.1. Гальванические покрытия: a) анодное покрытие j 0 1 > j 0 2; b) катодное покрытие j 0 1 < j 0 2. Я1 – металл, подлежащий защите, Me2 – металлическое покрытие (А – анод, В – катод)
Электрохимическая защита подразделяется на катодный, жертвенный и анодный. Первые два типа электрохимической защиты достигаются путем создания гальванического элемента, в котором защищаемый металл выступает в качестве катода. Это достигается путем контакта более активного металла с жертвенным металлом (который имеет более низкий стандартный электродный потенциал) или путем подключения изделия к отрицательному полюсу внешнего источника тока (катодная защита).
Анодная защита достигается путем подключения металла к положительному полюсу источника тока и формирования на его поверхности прочного оксидного слоя в результате анодного окисления путем электролиза (и смещения электродного потенциала в пассивное состояние).
Ингибиторы Ингибиторы – это вещества, которые добавляются в небольших количествах в коррозионную среду, накапливаются на границе раздела металл-электролит и замедляют скорость коррозии. Эффективность ингибиторов оценивается по значению коэффициента ингибирования К и степень защиты Z:
где ј – скорость коррозии в растворе без ингибитора;
ј – скорость коррозии в растворе с ингибитором.
Значение К это количество, на которое снизится скорость коррозии металла после добавления ингибитора. Значение Z является мерой относительного снижения скорости коррозии. На защитное действие ингибиторов существенно влияет ряд внешних и внутренних факторов коррозии: кислотность среды, температура, тип кислоты и защищаемого материала, тип растворителя и самого ингибитора, концентрация ингибитора, смешивание и т.д.
Пример 3.Можно ли использовать цинковое покрытие для защиты стальных изделий от коррозии во влажном воздухе? Нарисуйте электронные уравнения для катодного и анодного процессов коррозии, наблюдаемых при разрушении этого покрытия. Каков состав продуктов коррозии? Какой должна быть толщина покрытия, чтобы оно прослужило 5 лет, если величина P его глубины составляет 0,16 мм/год? Покрытие считается неработоспособным, если его остаточная толщина составляет 18% от первоначального значения.
Решение
Сравнение электродных потенциалов j 0 Zn/Zn 2+ = -0,76 В и j 0 Fe/Fe 2+ = -0,44 В, мы видим, что j 0 Zn < j 0 Fe Поэтому цинк по отношению к железу является анодом. Цинковое покрытие является анодным покрытием. На аноде происходит процесс окисления:
На катоде (Fe) происходит процесс восстановления молекул агента (во влажном воздухе это кислород и вода):
2H O + O + 4ē = 4OH .
Продукты коррозии: Zn 2+ + 2OH – = Zn(OH)2.
Если покрытие разрушится, сталь не растворится, поэтому можно использовать цинковое покрытие.
Толщина покрытия ∆h можно считать из уравнения:
где ∆h = P×t = 0.16 . 5 = 0,8 мм.
Но 82% первоначальной толщины подверглись коррозии. Тогда вся толщина покрытия должна составлять 100%:
K – константа равновесия
Окислительно-восстановительный потенциал
Значения окислительно-восстановительного потенциала используются, когда это необходимо для определения направления реакции в водных или других растворах.
2Fe 3+ + 2I – = 2Fe 2+ + I2
так что иодид-ионы и ионы железа обмениваются своими электронами через проводник..
В сосуды с растворами Fe 3+ и I – помещают инертный (платина или углерод) электроды и соедините внутренний и внешний контуры. В цепи возникает электрический ток.
Йодид-ионы отдают свои электроны, которые будут течь по проводнику к инертному электроду, погруженному в раствор соли Fe 3+:
2I – – 2e – = I2
2Fe 3+ + 2e – = 2Fe 2+
Окислительно-восстановительные процессы происходят на поверхности инертных электродов. Потенциал, возникающий на границе раздела между инертным электродом и раствором, содержащим как окисленную, так и восстановленную форму вещества, называется потенциалом равновесие окислительно-восстановительный потенциал.
Факторы, влияющие на величину окислительно-восстановительного потенциала
Значение окислительно-восстановительного потенциала зависит от многих факторов факторынапример
1) Природа вещества (окислитель и восстановитель)
2) Концентрация окисленных и восстановленных форм.
При температуре 25°C и давлении 1 атм окислительно-восстановительный потенциал рассчитывается по формуле уравнение Нернста:
E – окислительно-восстановительный потенциал данной пары;
Стандартный потенциал E° (измеряется при Cо = Cувеличение);
R – газовая постоянная (R = 8,314 Дж)
T – абсолютная температура, K
n – количество отданных или принятых электронов в окислительно-восстановительном процессе;
F – постоянная Фарадея (F = 96484,56 Кл/моль);
Cхорошо – концентрация (активность) окисленной формы;
Cуменьшенная форма– концентрация (активность) восстановленной формы.
Подставив известные данные в уравнение и перейдя к десятичному логарифму, мы получим следующую форму уравнения:
3) Кислотность раствора
Для пар, окисленная форма которых содержит кислород (например, Cr2O7 2- , CrO4 2- , MnO4 – ) окислительно-восстановительный потенциал увеличивается с уменьшением pH раствора, т.е. потенциал увеличивается с увеличением H + . И наоборот, окислительно-восстановительный потенциал уменьшается с уменьшением H + .
4) Температура
При повышении температуры окислительно-восстановительный потенциал данной пары также увеличивается.
Стандартные окислительно-восстановительные потенциалы можно найти в таблицах в специальных справочниках. Обратите внимание, что рассматриваются только реакции, протекающие в водных растворах при температуре ≈25 °C.
Эти таблицы позволяют рисовать некоторые выводы:
Что можно определить по значениям окислительно-восстановительного потенциала
- Величина и знак стандартного окислительно-восстановительного потенциалаНиже приведены некоторые из наиболее важных свойств, которые можно предсказать в химических реакциях, напр.
E°(F2/2F – ) = +2,87 В – сильнейший окислитель
E°(K + /K) = – 2,924 В – сильнейший восстановитель
Окислительно-восстановительная пара будет иметь чем больше восстановительная способностьчем больше его числовое значение отрицательный потенциали тем выше окислительная способность вышечем выше тем больше его положительный потенциал.
- Можно определить, какое соединение одного элемента будет обладать наиболее сильными окислительными или восстановительными свойствами.
- Можно предсказать направление ЭПР. Известно, что работа гальванического элемента происходит при положительной разности потенциалов. Также можно предсказать направление OR возможноесли разность потенциалов есть позитивный. ОВП течет в направлении слабых окислителей и восстановителей от более сильных, например, реакция
Sn 2+ + 2Fe 3+ = Sn 4+ + 2Fe 2+
практически течет в в прямом направлениив качестве
E° (Sn 4+ /Sn 2+ ) = +0,15 В,
E° (Fe 3+ /Fe 2+ ) = +0,77 В,
Cu + Fe 2+ = Cu 2+ + Fe
невозможно в прямом направлении и течет только справа налево, потому что
В процессе ОВС количество исходных веществ уменьшается, вызывая уменьшение Е окислителя и увеличение Е восстановителя. В конце реакции, т.е. при достижении химического равновесия, потенциалы двух процессов уравниваются.
- При определенных условиях может возникнуть несколько ОВД, реакция с наибольшей разностью окислительно-восстановительных потенциалов будет проведена первой.
- Используя справочные данные, мы можем определить ЭДС реакции.
Как определить электродвижущую силу (ЭДС) реакции?
Давайте рассмотрим некоторые примеры реакций и определим ЭМП:
- Mg + Fe 2+ = Mg 2+ + Fe
- Mg + 2H + = Mg 2+ + H2
- Mg + Cu 2+ = Mg 2+ + Cu
E° (Mg 2+ /Mg) = – 2,36 В
E° (Fe 2+ /Fe) = – 0,44 В
Для определения ЭДС реакции, найти разницу между окислительным и восстановительным потенциалом.
ЭДС = E 0 хорошо – Е 0 восстановить
- ЭДС = – 0,44 – (- 2,36) = 1,92 В
- ЭДС = 0,00 – (- 2,36) = 2,36 В
- ЭДС = + 0,34 – (- 2,36) = 2,70 В
Все вышеперечисленные реакции могут происходить в прямом направлениипотому что их ЭДС > 0.
Взаимосвязь между константой равновесия и окислительно-восстановительным потенциалом
Если необходимо определить степень реакции, то можно использовать константа равновесия.
Например, для реакции
Zn + Cu 2+ = Zn 2+ + Cu
Применение закон действующих массможно записать
Здесь константа равновесия K представляет собой равновесное соотношение между концентрациями ионов цинка и меди.
Значение константы равновесия можно рассчитать, используя уравнение Нернста
Подставляя в уравнение стандартные потенциалы пар Zn/Zn 2+ и Cu/Cu 2+, получаем
В равновесном состоянии E 0 Zn/Zn2+ = E 0 Cu/Cu2+, это
-0,76 + (0,59/2)lgCZn2+ = +0,34 + (0,59/2)lgCCu2+, из которого получаем
Значение константы равновесия показывает, что реакция протекает почти до конца, т.е. до тех пор, пока концентрация ионов меди не станет в 10,7 раз меньше концентрации ионов цинка.
Константа равновесия и окислительно-восстановительный потенциал связаны общей формулой
lgK = (E1 0 -E2 0 )n/0,059где
K – константа равновесия
E1 0 и E2 0 – стандартные потенциалы окислителя и восстановителя, соответственно
n – число электронов, отданных восстановителем или принятых окислителем.
Если E1 0 > E2 0 , тогда lgK > 0 и K > 1.
Реакция протекает в прямом направлении (слева направо), и если разница (E1 0 – E2 0 ) достаточно велик, он проходит почти до конца.
Напротив, если E1 0 < E2 0 , то K будет очень мал..
Реакция протекает в обратном направлении, так как равновесие сильно смещено влево. Если разница (E1 0 – E2 0 ) пренебрежимо мала, K ≈ 1, и реакция не будет протекать, если она не происходит в соответствующих условиях.
Знание стороны значение константы равновесия.без использования эмпирических данных может дать представление о глубине химической реакции. Важно помнить, что данные стандартного потенциала не дают представления о скорости, с которой реакция достигает равновесия.
Используя таблицы окислительно-восстановительных потенциалов, можно найти значения констант равновесия примерно для 85000 реакций.
Как составить схему гальванического элемента?
Пожалуйста, следуйте рекомендациям ИЮПАК по правильной нотации Диаграммы гальванического элемента и происходящих в нем реакций:
- ЭМП клетки – является положительным значением, поскольку в гальваническом элементе совершается работа.
- Значение ЭДС в гальванической цепи – это сумма скачков потенциала на контактах всех фаз, но поскольку окисление происходит на аноде, значение анодного потенциала должно быть вычтено из значения катодного потенциала.
Поэтому, когда вы рисуете схему гальванического элемента. слева электрод, на котором происходит окисление процесса окисления (анод), а справа – электрод, на котором происходит процесс восстановления (катод). процесс восстановления (катод).
- Интерфейс обозначается одной линией – |
- Электролитический мост на стыке двух проводников представлена двумя линиями – -. ||
- Растворы, в которые погружается электролитический мост записаны слева и справа от моста (при необходимости здесь же записывается концентрация растворов). Компоненты одной фазы, в данном случае, пишутся через запятую.
Например, сделайте диаграмма гальванического элементав котором происходит следующая реакция
Fe 0 + Cd 2+ = Fe 2+ + Cd 0
В гальваническом элементе анодом является железный электрод, а катодом – кадмиевый электрод.
Анод – это Fe 0 |Fe 2+ || Cd 2+ |Cd 0 Катод
Типовые задачи на составление схем гальванических элементов и расчет электродвижущей силы реакции вместе с их решениями можно найти здесь.
Читайте далее:- Типы эмиссии электронов.
- Как работает pH-электрод.
- Электролит (химия) – это. Что такое электролит (химия)?.
- Значение слова 'потенциал' в 9 словарях.
- Гальванические элементы – устройство, принцип действия, виды и основные характеристики; Сайт для электриков – статьи, советы, примеры, схемы.
- Топливные элементы/.
- Триод: конструкция и работа трехэлектродной лампы.