На рисунке 9.11 показана схема электролитического рафинирования меди.
Что представляет собой ток в электролитах
Электролиты обычно рассматриваются как проводящие среды, в которых протекание электрического тока сопровождается переносом веществ. Носителями свободного заряда в электролитах являются положительно и отрицательно заряженные ионы.
Основными представителями электролитов, широко используемых в технике, являются водные растворы неорганических кислот, солей и оснований. Прохождение электрического тока через электролит сопровождается выделением веществ на электродах. Это явление известно как электролиз (рис. 9.10).
Электрический ток в электролитах основан на движении ионов обоих знаков в противоположных направлениях. Положительные ионы движутся к отрицательному электроду (катод), а отрицательные ионы движутся к положительному электроду (анод). Ионы обоих знаков появляются в водных растворах солей, кислот и оснований в результате расщепления частей нейтральных молекул. Это явление называется электролитическая диссоциация.
Закон электролиза был экспериментально установлен английским физиком М. Фарадеем в 1833 году.
Первый закон Фарадея определяет количество первичных продуктов, осаждаемых на электродах при электролизе: масса m вещества, выделяющегося на электроде, прямо пропорциональна заряду q, прошедшему через электролит:
m = kq = kIt,
где k – электрохимическая эквивалентность вещества:
F = eNA = 96485 Кт/моль. – Постоянная Фарадея.
Второй закон Фарадея Электрохимические эквиваленты различных веществ соотносятся с их химическими эквивалентами :
Комбинированный закон Фарадея к электролизу:
Электролитические процессы классифицируются следующим образом:
Производство неорганических веществ (водорода, кислорода, хлора, оснований и т.д.)
производство металлов (литий, натрий, калий, бериллий, магний, цинк, алюминий, медь и т.д.)
рафинирование металлов (медь, серебро, …);
производство металлических сплавов;
гальваническое покрытие;
обработка поверхности металлов (азотирование, борирование, электрополировка, очистка);
производство органических веществ;
электродиализ и опреснение воды;
осаждение пленки с помощью электрофореза.
Практическое применение электролиза
Электрохимические процессы широко используются в различных областях современной техники, аналитической химии, биохимии и т.д. В химической промышленности путем электролиза получают хлор и фтор, щелочи, хлораты и перхлораты, серную кислоту и персульфаты, химически чистые водород и кислород и т.д. Некоторые вещества образуются при восстановлении на катоде (альдегиды, пара-аминофенол и т.д.), другие – при электроокислении на аноде (хлораты, перхлораты, перманганат калия и т.д.).
Электролиз в гидрометаллургии является одним из этапов переработки металлосодержащего сырья для получения товарных металлов. Электролиз может проводиться с растворимыми анодами – процесс электрорафинирования – или с нерастворимыми анодами – процесс электроэкстракции. Основной проблемой при электрорафинировании металлов является достижение требуемой катодной чистоты металла при приемлемых энергетических затратах. В цветной металлургии электролиз используется для извлечения металлов из руд и их рафинирования.
Электролиз расплавленных металлов позволяет получить алюминий, магний, титан, цирконий, уран, бериллий и т.д. Для рафинирования (очистки) металла электролизом из него отливают пластины и помещают их в качестве анодов 1 в электролизер 3 (рис. 9.11). При протекании тока рафинированный металл 1 подвергается анодному растворению, т.е. переходит в раствор в виде катионов. Затем эти катионы металла разряжаются на катоде 2, в результате чего образуется компактный осадок уже чистого металла. Примеси на аноде либо остаются нерастворимыми 4, либо переходят в электролит и удаляются.
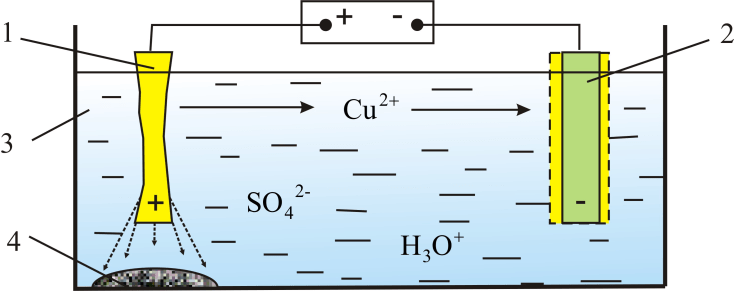
На рисунке 9.11 показана схема электролитического рафинирования меди.
Гальваническое покрытие – Отрасль прикладной электрохимии, занимающаяся процессом нанесения металлических покрытий на поверхность металлических и неметаллических объектов путем пропускания постоянного электрического тока через растворы их солей. Гальваническая технология подразделяется на гальваническое покрытие.
Гальваническое покрытие (от греческого слова “мантия”) Гальваника – это осаждение другого металла на поверхность металла.Это метод нанесения гальванического покрытия, которое прочно связывается с покрываемым металлом (объектом), служащим катодом электролизера (рис. 9.12).
Гальваника может использоваться для покрытия деталей тонким слоем золота или серебра, хрома или никеля. Электролиз можно использовать для нанесения тонких металлических покрытий на различные металлические поверхности. В этом методе нанесения покрытия деталь используется как катод, помещенный в солевой раствор металла, на который наносится покрытие. В качестве анода используется пластина из того же металла.
| Рисунок 9.12 | Рисунок 9.13 |
Рекомендуем посмотреть демонстрацию “Гальваника”.
Электроформование – Изготовление методом электролиза точных, легко снимаемых металлических копий значительной толщины из различных неметаллических и металлических предметов, называемых штампами (рис. 9.13).
Бюсты, статуэтки и т.д. изготавливаются методом гальванопластики. Гальванопластика используется для нанесения относительно толстых металлических покрытий на другие металлы (например, создание “накладки” из никеля, серебра, золота и т.д.).
$m = k ■ I ■ t$
Лабораторная работа “Определение элементарного заряда методом электролиза”.
Технические применения электролиза
Гальванизация – Покрытие металлических предметов тонким слоем другого металла (никелирование, хромирование, серебрение, золочение и т.д.) для защиты от окисления и придания им привлекательного внешнего вида. Объект для нанесения покрытия тщательно очищают, хорошо обезжиривают и помещают в качестве катода в электролитическую ванну, содержащую раствор соли металла, которым объект должен быть покрыт. Анодом служит пластина из того же металла. Для получения более равномерного покрытия часто используют две пластины в качестве анода, а объект помещают между ними.
Гальваническое покрытие – Электролитическое изготовление копий рельефных объектов (медалей, гравюр, барельефов и т.д.). С рельефного объекта делается восковая или другая отливка. Затем поверхность оттиска покрывается тонким слоем графита, чтобы сделать его проводящим. В этой форме отливка используется в качестве катода, который опускается в электролитическую ванну с раствором сульфата меди. Анодом является медная пластина. Когда на отливке вырастает достаточно толстый слой меди, электролиз прерывают и осторожно удаляют воск. Получается точная медная копия оригинала.
В полиграфической промышленности такие копии (стереотипы) изготавливаются с оттиска набора на пластиковом материале (матрице) путем нанесения на матрицу толстого слоя железа или другого материала. Это позволяет размножить набор в необходимом количестве экземпляров. Если раньше тираж книги был ограничен количеством оттисков, которые можно было получить из одного набора (набор стирается во время печати), то использование стереотипов позволяет значительно увеличить тираж.
Правда, в настоящее время электролиз используется для изготовления стереотипов только для книг высокого качества и с большим количеством иллюстраций.
Путем осаждения металла на длинный цилиндр производятся бесшовные трубы.
Процесс получения чешуйчатых покрытий был разработан русским ученым Якоби Б.С., который использовал этот метод в 1836 году для изготовления вогнутых фигур для Исаакиевского собора (в Санкт-Петербурге).
Рафинирование меди
Медь – лучший материал для проводников, но для этого она должна быть очищена от всех примесей. Удаление примесей из меди называется рафинированием (очисткой) меди. Сплошные куски (толстые листы) сырой меди, полученные при выплавке из руды, являются анодом, а тонкие пластины чистой меди – катодом. Этот процесс происходит в больших ваннах с водным раствором сульфата меди. В процессе электролиза медь в аноде растворяется, примеси, содержащие ценные и редкие металлы, выпадают на дно в виде осадка, а чистая медь осаждается на катоде. Аналогичным образом очищаются и некоторые другие металлы.
Производство алюминия
Алюминий добывается с помощью электролиза. Вместо солевых растворов этого металла они электролизуют его в расплавленных оксидах.
Глинозем (оксид алюминия Al2O3), получаемый при переработке бокситовых руд, содержащих алюминий, засыпают в угольные тигли. Тигель служит катодом. Анод состоит из углеродных стержней, вставленных в тигель. Угольные стержни сначала опускают в тигель и пропускают через них сильный ток. При прохождении тока глинозем нагревается и плавится. Затем карбонаты поднимаются, ток проходит через жидкость и вызывает электролиз. Расплавленный алюминий, образующийся при электролизе, падает на дно тигля (катода), откуда через специальное отверстие попадает в литейные формы.
Описанный способ производства алюминия сделал его самым дешевым и, наряду с железом, самым распространенным металлом в технике и быту.
При электролизе расплавленных солей получают также натрий, калий, магний, кальций и другие металлы.
Электролиз используется для гальванизации, нанесения гальванических покрытий, рафинирования меди, производства алюминия и других целей.
Рисунок 1 . 15 . 1 . Электролиз водного раствора хлорида меди.
Закон электролиза
В 1833 году М. Фарадей установил закон электролиза.
Закон Фарадея определяет количество первичных продуктов, которые выделяются при электролизе на электродах. Масса m вещества, выделяющегося на электроде, прямо пропорциональна заряду Q, протекающему через электролит:
m = k Q = k I t , где k – электрохимический эквивалент.
Масса вещества, выделившегося на электроде, равна массе всех ионов, достигших электрода, и записывается n = m 0 N = m 0 Q q 0 = m 0 q 0 I t .
Значения m 0 и q 0 представляют собой массу и заряд одного иона, соответственно, а N = Q q 0 – число ионов, достигших электрода при прохождении через электролит с зарядом Q . Отсюда следует, что электрохимический эквивалент k равен отношению массы m 0 иона вещества к его заряду q 0 .
Заряд иона является произведением валентности вещества n и элементарного заряда e ( q 0 = n e ), тогда выражение для k становится равным
k = m 0 q 0 = m 0 N A n e N A = 1 F M n .
N A – постоянная Авогадро, M = m 0 N A – молярная масса вещества, F = e N A – постоянная Фарадея.
F = e N A = 96485 K л / м о л .
Постоянная Фарадея равен заряду, который необходимо пропустить через электролит, чтобы высвободить один моль моновалентного вещества на электроде.
Закон Фарадея для электролиза обозначается следующим образом
Явление электролиза широко используется в современном промышленном производстве.
1. положительные ионы, образованные из атомов металла или водорода.
Электролиз .
Положительные и отрицательные ионы, будучи свободными носителями заряда, также являются молекулами материи. Поэтому наиболее важное различие между током в электролитах и током в металлах заключается в том, что Электрический ток в электролите сопровождается переносом вещества.
Явление переноса вещества при прохождении электрического тока через электролит называется электролизом электролиз. Законы электролиза были экспериментально изучены Фарадеем.
При электролизе растворенный раствор распадается на составные части и разделяется на электроде. Например, в растворе сульфата меди положительные ионы меди переходят на катод, в результате чего катод покрывается медью. На аноде выделяется кислотный остаток.
Естественно, возникает вопрос о нахождении массы вещества, выделившегося на электроде за определенное время. Эта масса, очевидно, совпадает с массой данного вещества, перемещаемого током через электролит с течением времени.
Пусть – обозначает массу одного иона вещества, – обозначает заряд иона (- валентность вещества). Предположим, что во время прохождения через электролит заряд . Число ионов, достигших электрода, равно . Масса вещества, осаждающегося на электроде, равна общей массе ионов:
Это количество является характеристикой вещества и называется его электрохимический эквивалент вещества. Значения электрохимических эквивалентов различных веществ приведены в таблицах.
Когда постоянный ток проходит через электролит, через него протекает заряд. Подставив это в уравнение (1), мы получим первый закон Фарадея:
Первый закон Фарадея. Масса вещества, выделяющегося на электроде, пропорциональна силе тока, протекающего через электролит, и времени протекания тока.
Теперь преобразуем выражение для электрохимического эквивалента, введя молярную массу вещества:
Подставляя это выражение в (2), получаем вторую формулу Фарадея:
Второй закон Фарадея. Масса вещества, выделяющегося на электроде, прямо пропорциональна молярной массе вещества и обратно пропорциональна его валентности..
В формуле (3) мы видим произведение двух констант и . Это также является константой и называется постоянная Фарадея:
Ионы, образующиеся в результате диссоциации, делятся на два типа:
Закон Фарадея
Процесс электролиза был экспериментально изучен английским физиком и химиком Майклом Фарадеем в 1833 году. Он сформулировал закон, согласно которому масса вещества, выделяющегося на электроде, прямо пропорциональна заряду, протекающему через электролит. Этот закон известен в науке как первый закон Фарадея.

Рисунок 3: Майкл Фарадей.
- m – масса вещества;
- Q – зарядка;
- k – электрохимический эквивалент;
- I – сила тока;
- t – время текущего действия.
Согласно второму закону Фарадея, масса вещества, высвобождаемого на электродах, прямо пропорциональна отношению молярной массы к валентной и равна электрохимическому эквиваленту.
- m – масса выделившегося вещества;
- k – электрохимический эквивалент;
- М – молярная масса;
- z – валентность вещества.
Электролиз используется в щелочных и кислотных аккумуляторах. Электролиз можно использовать для защиты изделия с металлическим покрытием.
Очевидно, что отрицательные ионы (SO4) пойдет к аноду, а положительный (Cu) к катоду, т.е. в электролите начинается упорядоченное движение ионов. Это упорядоченное движение ионов в электролите под воздействием электрического поля называется ионный электрический ток. Ионный электрический ток существует до тех пор, пока между электродами существует разность потенциалов.
Электрический ток в электролитах
В жидких проводниках (электролиты) спонтанное расщепление молекул на составляющие происходит непрерывно. Этот процесс иногда называют диссоциация молекул. Например, молекула медного купороса CuS04 диссоциирует на положительный ион меди Cu и отрицательный ион S04 (так называемый кислотный остаток). В электролите происходит неупорядоченное тепловое движение ионов и молекул. Ионы соединяются, образуют молекулы, снова распадаются и так далее. В целом, раствор является электрически нейтральным, поскольку количество положительных и отрицательных ионов в нем одинаково.
Давайте проведем следующий эксперимент. В стеклянную пробирку с раствором медного купороса (CuS04) слить две медные пластины (электроды) и подключить их к источнику электричества (рис. 1). Пластина, соединенная с положительным полюсом источника, называется анод (эта пластина положительная), а другая, соединенная с отрицательным полюсом, называется катод (эта пластина имеет отрицательный потенциал).
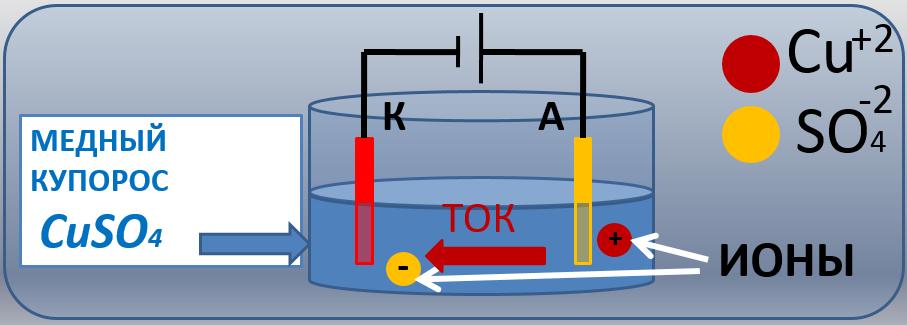
Рисунок 1. Протекание электрического тока через раствор сульфата меди.
Как только мы подключаем пластины к источнику электричества, между ними создается электрическое поле. Положительные и отрицательные ионы в растворе начнут взаимодействовать друг с другом под действием электрических сил.
Очевидно, что отрицательные ионы (SO4) будет двигаться к аноду, а положительные ионы (Cu) будет двигаться к катоду, т.е. в электролите начнется упорядоченное движение ионов. Это упорядоченное движение ионов в электролите под воздействием электрического поля называется ионный электрический ток. Ионный электрический ток существует до тех пор, пока между электродами существует разность потенциалов.
Мы видим фундаментальное различие между электрическим током в электролите и электрическим током в металлическом проводнике: первый возникает в результате движения ионов, а второй – в результате движения свободных электронов.
Что происходит в электролите, когда положительные ионы приближаются к катоду, а отрицательные ионы – к аноду?
Положительные ионы (Cu) присоединяют недостающие электроны и превращаются в молекулы чистой меди. Частицы меди осаждаются на катоде в виде очень тонкого слоя. Отрицательные ионы отдают дополнительные электроны аноду и вступают в химическую реакцию с материалом анода, т.е. с медью. меди, образуя частицы сульфата меди (CuSO4). Эти молекулы попадают в электролит.
Таким образом, при протекании электрического тока в электролите происходит следующий процесс: катод покрывается слоем меди, выделяющейся из электролита, а анод растворяется и восполняет потери меди в электролите.
Определение: Процесс пропускания ионного электрического тока через электролит, сопровождающийся химическим превращением вещества и его выделением, называется электролизом
Честь открытия явления электролиза принадлежит русскому ученому Б.С. Якоби. С. Якоби. Сегодня явление электролиза широко используется в промышленности (очистка металлов, копирование различных предметов, никелирование, золочение, серебрение и т.д.).
ПОНРАВИЛАСЬ ЛИ ВАМ СТАТЬЯ? ПОДЕЛИТЕСЬ ИМ СО СВОИМИ ДРУЗЬЯМИ В СОЦИАЛЬНЫХ СЕТЯХ!
Читайте далее:- Что такое электродный потенциал; Школа для инженеров-электриков: электротехника и электроника.
- Гальванические элементы – устройство, принцип действия, виды и основные характеристики; Сайт для электриков – статьи, советы, примеры, схемы.
- Электролит (химия) – это. Что такое электролит (химия)?.
- Типы эмиссии электронов.
- Электролиз.
- Тонкости электропроводности.
- Гальваника для начинающих. Что это такое и для чего он используется?.