Тип электролитического конденсатора, в котором в качестве одной из обмоток используется электролит. Конденсаторы этого типа, в отличие от других типов, имеют несколько характерных особенностей
Все электролиты делятся на две группы в зависимости от степени диссоциации
- сильные электролиты – электролиты, степень диссоциации которых в растворах равна единице (т.е. диссоциирует полностью) и не зависит от концентрации раствора. Подавляющее большинство солей, оснований и некоторые кислоты относятся к этой группе.
- Слабые электролиты – Степень диссоциации меньше единицы (т.е. не диссоциирует полностью) и уменьшается с увеличением концентрации. К ним относятся вода, ряд кислот и оснований из элементов p-, d- и f-.
Между этими двумя группами нет четкой границы; одно и то же вещество может быть сильным электролитом в одном растворителе и слабым электролитом в другом.
Применяется для изготовления электродов химических источников тока с твердыми электролит.
Значение слова “электролит”

ЭЛЕКТРОЛИ’Т., а, м. [от слова электрический и греческого lytos – растворенный] (физ.). Раствор какого-либо вещества, который может быть разложен на составные части путем электролиза.
Источник: “Толковый словарь русского языка” под редакцией Д. Н. Ушакова (1935-1940); (электронная версия): Фундаментальная электронная библиотека
электролит
1. физико-химическое вещество (обычно раствор или сплав), в котором протекание электрического тока происходит за счет движения ионов ◆ С другой стороны, макрогол не влияет на водный баланс и не вызывает абсорбции или экскреции электролиты в кишечнике. Под редакцией С. Маркуччи, Н.А. Коэн, Д.Г. Метро, Дж.Р. Кирш, Анестезиология, 2011.
Совместное совершенствование карты слов
/> Привет, меня зовут Lampbot, я компьютерная программа, которая поможет вам создать карту Word. Я хорошо разбираюсь в математике, но пока не понимаю, как устроен ваш мир. Пожалуйста, помогите мне понять!
Спасибо! Я обязательно научусь отличать общеупотребительные слова от узкоспециализированных.
Когда речь идет о понимании значения слова кантон (существительное):
Условные обозначения слова “электролит»
Синонимы к слову “электролит»
Предложения со словом “электролит»
- Радиатор все еще в порядке, кардан тоже в порядке, но сниженный уровень электролит – закончилась!
Сочетание слова “электролит
Термины со словом “электролит”
Опубликовать комментарий
Читать далее
Предложения со словом “электролит»
Радиатор в порядке, кардан в порядке, но сниженный уровень электролит – это просто завершающий штрих!
Батареи также различаются по следующим параметрам электролит – Например, это не кислота, а щелочь.
Он используется для изготовления электродов для химических источников тока с твердым электролитом. Электролит.
Синонимы к слову “электролит»
- аммиак
- мочевина
- хлор
- фенол
- перманганат
ассоциации со словом электролит
- электричество
- физика
- текущий
- химия
- аккумулятор
Сочетание слова “электролит»
Морфология
Карта русских слов и фраз
Онлайн тезаурус с возможностью поиска ассоциаций, синонимов, контекстуальных ассоциаций и примеров предложений для русских слов и фраз.
Основная информация о склонении существительных и прилагательных, спряжении глаголов и морфемной структуре слов.
Концентрированный раствор, с другой стороны, имеет структуру, подобную ионному сплаву или кристаллосольвату, характеризующуюся высокой упорядоченностью и однородностью ионных структур. Такие ионные структуры соединяются друг с другом и с молекулами воды посредством сложных взаимодействий.
Что такое электролит
Вещества, в которых электрический ток обусловлен движением ионов, т.е. ионной проводимостью, называются электролитами. Электролиты являются проводниками второго класса, поскольку ток в них связан с химическими процессами, а не просто с движением электронов, как в металлах.
Их молекулы в растворе способны к электролитической диссоциации, т.е. они растворяются на положительно заряженные (катионы) и отрицательно заряженные (анионы) ионы. В природе встречаются твердые электролиты, ионные сплавы и растворы электролитов. В зависимости от типа растворителя электролиты могут быть водными или неводными, а также особого типа – полиэлектролиты.

В зависимости от типа ионов, на которые вещество растворяется в воде, различают электролиты без ионов H+ и OH- (солевые электролиты), электролиты с большим количеством ионов H+ (кислоты) и электролиты с преобладанием ионов OH- (основания).
Если в результате диссоциации молекул электролита образуется одинаковое количество положительных и отрицательных ионов, электролит называется симметричным. Или же он является асимметричным, если количество положительных и отрицательных ионов в растворе не одинаково. Примерами симметричных электролитов являются валентный электролит KCL-1.1 и CaSO4 – 2,2-валентный электролит. Представителем асимметричного электролита является, например, H2SO4 – 1,2-валентный электролит.

Все электролиты можно условно разделить на сильные и слабые, в зависимости от их способности к диссоциации. Сильные электролиты почти полностью диссоциируют на ионы в разбавленных растворах. К ним относятся многие неорганические соли, некоторые кислоты и основания в водных растворах или растворители с высокой способностью к диссоциации, такие как спирты, кетоны или амиды.
Слабые электролиты диссоциируют лишь частично и остаются в динамическом равновесии с недиссоциированными молекулами. К ним относятся большое количество органических кислот, а также многие основания в растворителях.
Степень диссоциации зависит от нескольких факторов: от температуры, от концентрации и от типа растворителя. Таким образом, один и тот же электролит при разных температурах или при одной и той же температуре, но в разных растворителях, будет диссоциировать в разной степени.
Поскольку электролитическая диссоциация, по определению, порождает больше молекул в растворе, это приводит к значительным различиям в физических свойствах растворов электролитов и веществ других типов: увеличивается осмотическое давление, изменяется точка замерзания относительно чистого растворителя и т.д.
Ионы электролита часто участвуют в электрохимических процессах и химических реакциях как самостоятельные кинетические единицы, не зависящие от других ионов, присутствующих в растворе: окислительно-восстановительные реакции происходят на электродах, погруженных в электролит, продукты которых добавляются к электролиту при протекании тока через электролит.
Таким образом, электролиты представляют собой сложные системы веществ, включающие ионы, молекулы растворителя, недиссоциированные молекулы растворителя, ионные пары и более крупные соединения. Поэтому свойства электролитов определяются рядом факторов: характером взаимодействий ион-молекула и ион-ион, изменениями в структуре растворителя в присутствии молекул растворителя и т.д.
Ионы и молекулы полярных электролитов взаимодействуют очень активно, что приводит к образованию сольватационных структур, роль которых возрастает с уменьшением размера ионов и увеличением их валентности. Энергия сольватации – это мера взаимодействия ионов электролита с молекулами растворителя.

Электролиты, в зависимости от их концентрации, могут быть: разбавленными растворами, переходными растворами и концентрированными растворами. Разбавленные растворы имеют структуру, подобную структуре чистого растворителя, но присутствующие ионы нарушают эту структуру своим взаимодействием. Эти слабые растворы сильных электролитов отличаются от идеальных растворов по своим свойствам из-за электростатического взаимодействия между ионами.
Область концентрационного перехода характеризуется значительным изменением структуры растворителя вследствие взаимодействия ионов. При еще более высоких концентрациях большинство молекул растворителя участвуют в сольватационных структурах с ионами, создавая тем самым дефицит растворителя.
Концентрированный раствор имеет структуру, подобную ионному сплаву или кристаллосольвату, характеризующуюся высокой степенью упорядоченности и однородности ионных структур. Эти ионные структуры вступают друг с другом и с молекулами воды в сложные взаимодействия.
Электролиты характеризуются высоко- и низкотемпературными областями своих свойств, а также областями высокого и нормального давления. С увеличением давления или температуры молярное упорядочение растворителя уменьшается, и влияние ассоциативных и сольватационных эффектов на свойства раствора ослабевает. А когда температура опускается ниже точки плавления – некоторые электролиты переходят в стеклообразное состояние. Примером такого электролита является водный раствор LiCl.

Сегодня электролиты играют особенно важную роль в мире техники и биологии. В биологических процессах электролиты являются средой для неорганического и органического синтеза, а в технике – основой для электрохимического производства.
Электролиз, электрокатализ, коррозия металлов, электрокристаллизация – эти явления занимают важное место во многих современных отраслях промышленности, особенно в связи с энергетикой и охраной окружающей среды.
Поскольку для осаждения или нейтрализации 1 эквивалента требуется такое же количество электроэнергии. любого вещества требуется одинаковое количество электричества, то очевидно, что заряд, переносимый ионами, содержащимися в 1 экв. ионов, одинаков для всех веществ. Число эквивалентов в одном моле иона равно валентности иона, поэтому число единичных зарядов (электронов), переносимых ионом, можно приравнять к его валентности. Моновалентный катион (например, Na + , K + , Ag + ) не имеет одного электрона по сравнению с нейтральным атомом; такой катион имеет единственный положительный заряд. Двухвалентный катион (например, Ca 2+ , Zn 2+ , Cu 2+ ) не имеет двух электронов; он несет два единичных положительных заряда и т.д. Единичный отрицательный заряд моновалентного аниона (Cl – , Br – ) образован одним электроном, находящимся в избытке у нейтрального атома.
Константа диссоциации.
Согласно Аррениусу, степень диссоциации, т.е. Процент молекул, диссоциировавших на ионы, увеличивается с разбавлением раствора. Предполагая, что скорость перемещения ионов через электролит не зависит от концентрации раствора, и измеряя электропроводность, Аррениус рассчитал степень диссоциации нескольких электролитов различной концентрации. В. Оствальд в 1888 году использовал этот метод для расчета концентрации свободных ионов и недиссоциированных молекул в растворе и, таким образом, константы равновесия (константы диссоциации) реакции диссоциации. Обратимая диссоциация электролита CA на ионы C + и A – описывается уравнением CA C + + A – , а константа диссоциации составляет K = [C + ][A – ]/[CA] (значения в квадратных скобках обозначают концентрации). Последнее соотношение удовлетворительно описывает поведение только растворов слабых электролитов – слабых кислот и оснований. Сильные электролиты, т.е. водные растворы сильных кислот, оснований и большинства солей, ведут себя иначе; оказалось, что основной постулат Аррениуса о постоянстве скорости движения ионов и их независимости от концентрации не применим к сильным электролитам.
Mg(OH) + ⇄ Mg 2+ + OH –
Теория электролитической диссоциации
Электролиты – это вещества, растворы и сплавы которых проводят электрический ток.
Электрический ток – это упорядоченное движение заряженных частиц под действием электрического поля. Таким образом, в растворах электролитов или сплавов присутствуют заряженные частицы. В растворах электролитов электропроводность обычно обусловлена присутствием ионов.
Ионы – это заряженные частицы (атомы или группы атомов). Различают положительно заряженные ионы () и отрицательно заряженные ионы (анионы).
Электролитическая диссоциация – это процесс диссоциации электролита на ионы при его растворении или плавлении.
Различают электролиты и неэлектролиты. К неэлектролиты включают вещества с сильными неполярными ковалентными связями (простые вещества), все оксиды (которые являются химически Большинство органических веществ (кроме полярных соединений, таких как карбоновые кислоты, их соли и фенолы), альдегиды, кетоны, углеводороды и углеводы.
К электролиты это определенные вещества с полярными ковалентными связями и вещества с ионными кристаллическими решетками.
Какова природа процесса электролитической диссоциации?
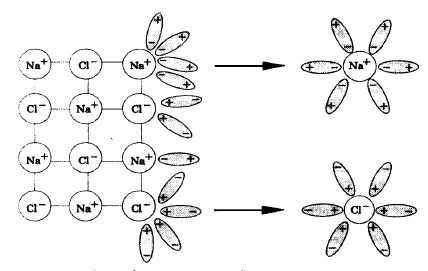
Поместите несколько кристаллов хлорида натрия в пробирку и добавьте воды. Через некоторое время кристаллы растворяются. Что произошло?
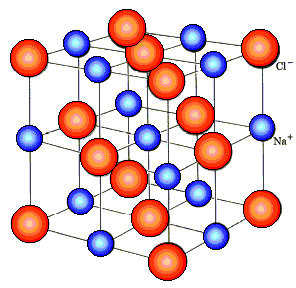
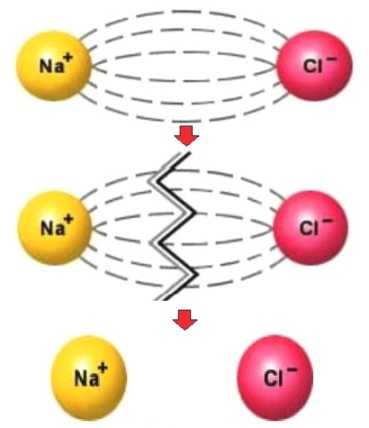
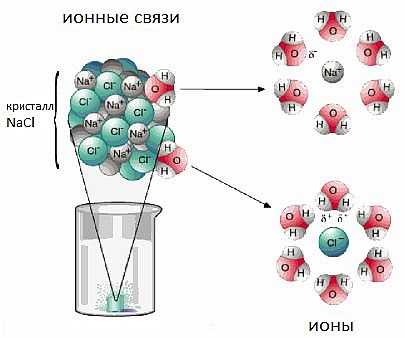
Хлорид натрия – это вещество с ионной кристаллической решеткой. Кристалл NaCl состоит из ионов Na + и Cl -. В воде кристалл может растворяться в структурных единицах – ионах. В этом процессе разрушаются ионные химические связи и некоторые водородные связи между молекулами воды. Ионы Na + и Cl будут реагировать с молекулами воды. В случае хлорид-ионов можно говорить об электростатическом притяжении дипольных (полярных) молекул воды к хлорид-аниону, а в случае катионов натрия это имеет донорно-акцепторный характер (когда электронная пара атома кислорода размещается на свободных орбиталях иона натрия). Ионы, окруженные молекулами воды, покрыты гидратное покрытие. Диссоциация хлорида натрия описывается уравнением:
NaCl = Na + + Cl –
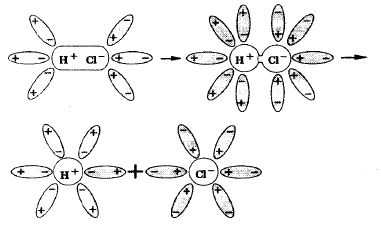
Когда соединения с полярными ковалентными связями растворяются в воде, молекулы воды, окружающие полярную молекулу, сначала растягивают связь в молекуле, увеличивая ее полярность, а затем разбивают ее на ионы, которые становятся гидратированными и равномерно распределяются в растворе. Например, солянокислый ксилол диссоциирует на ионы следующим образом: HCl = H + Cl – .
При плавлении, когда кристалл нагревается, ионы начинают интенсивно вибрировать в узлах кристаллической решетки, вызывая ее диссоциацию, образуя сплав, состоящий из ионов.
Процесс электролитической диссоциации характеризуется степенью диссоциации молекул вещества:
Степень диссоциации – это отношение числа диссоциированных (разложившихся) молекул к общему числу молекул электролита. Т.е. какая доля молекул исходного вещества диссоциирует на ионы в растворе или расплаве.
Nпродисс – число молекул, которые диссоциировали,
Nisc – начальное число молекул.
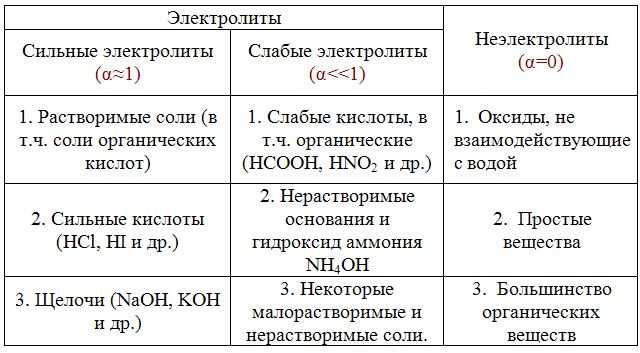
В зависимости от степени диссоциации электролиты делятся на сильный и слабый.
Сильные электролиты (α≈1):
1. Все растворимые соли (включая соли органических кислот, такие как ацетат калия CH3COOK, формиат натрия HCOONa и т.д.)
2. Сильные кислоты: HCl, HI, HBr, HNO3, H2SO4 (на первой стадии), HClO4 и т.д;
3. Щелочи: NaOH, KOH, LiOH, RbOH, CsOH; Ca(OH)2Ca(OH) , Sr(OH)2, Ba(OH)2.
Сильные электролиты Растворяются на ионы почти полностью в водных растворах, но только в ненасыщенных растворах. В насыщенных растворах даже сильные электролиты могут диссоциировать лишь частично. Это означает, что степень диссоциации сильных электролитов α приблизительно равна 1 только для ненасыщенных растворов вещества. В насыщенных или концентрированных растворах степень диссоциации сильных электролитов может быть меньше или равна 1: α≤1.
Слабые электролиты (α<1):
1. Слабые кислоты, включая органические кислоты;
2. Нерастворимые основания и гидроксид аммония NH4OH;
3. Нерастворимые и некоторые слегка растворимые соли (в зависимости от растворимости).
Неэлектролиты:
1. Оксиды, не взаимодействующие с водой (оксиды, взаимодействующие с водой, вступают в химическую реакцию с образованием гидроксидов при растворении в воде);
2. Простые вещества;
3. Большинство органических веществ со слабополярными или неполярными связями (альдегиды, кетоны, углеводороды и т.д.).
Как диссоциируют вещества? В зависимости от степени диссоциации различают сильный и слабый электролиты.
Сильные электролиты диссоциируют полностью (в насыщенных растворах), за один шаг, при этом все молекулы распадаются на ионы, почти необратимо. Примечание – при диссоциации в растворе образуются только стабильные ионы. Наиболее распространенные ионы можно найти в таблице растворимости – это ваша официальная шпаргалка для каждого экзамена. Степень диссоциации сильных электролитов составляет около 1. Например, при диссоциации фосфата натрия образуются ионы Na + и PO4 3– :
Диссоциация слабые электролиты полибазовые кислоты и полибазовые основания Диссоциация происходит постепенно и обратимо.. То есть при диссоциации слабых электролитов только очень небольшая часть исходных молекул диссоциирует на ионы. Например, карбоновая кислота:
HCO3 – ↔ H + + CO3 2–
Гидроксид магния также диссоциирует в два этапа:
Mg(OH)2 ⇄ Mg(OH) + OH -.
Mg(OH) + ⇄ Mg 2+ + OH -.
Кислые соли также диссоциируют в Кислые соли также диссоциируют постепенно; сначала диссоциируют ионные связи, а затем ковалентные полярные связи. Например, бикарбонат калия и гидроксихлорид магния:
KHCO3 ⇄ K + + HCO3 – (α=1)
HCO3 – ⇄ H + CO3 2- (α < 1)
Mg(OH)Cl ⇄ MgOH + + Cl – (α=1)
MgOH + ⇄ Mg 2+ + OH – (α<< 1)
Степень диссоциации слабых электролитов намного меньше 1: α<<1.
Основные теоремы теории электролитической диссоциации следующие:
1. При растворении в воде электролиты диссоциируют (распадаются) на ионы.
2. Причиной диссоциации электролита в воде является его гидратация, т.е. взаимодействие с молекулами воды и разрыв химических связей в них.
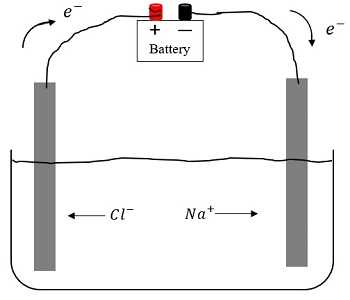
3. Под воздействием внешнего электрического поля положительно заряженные ионы движутся к положительно заряженному электроду – катоду – и называются катионами. Отрицательно заряженные электроны движутся к отрицательному электроду – аноду. Они называются анионами.
4. Электролитическая диссоциация обратима для слабых электролитов и практически необратима для сильных электролитов.
5. Электролиты могут диссоциировать на ионы в различной степени в зависимости от внешних условий, концентрации и природы электролита.
6. Химические свойства ионов отличаются от свойств простых веществ. Химические свойства растворов электролитов определяются свойствами тех ионов, которые образуются из него при диссоциации.
Примеры
1. Когда 1 моль соли диссоциировал не полностью, общее количество положительных и отрицательных ионов в растворе составило 3,4 моль. Формула соли представляет собой (a) K2S б) Ba(ClO3)2 c) NH4НЕТ3 (d) Fe(NO3)3
РешениеСначала определим силу электролитов. Это можно легко сделать по таблице растворимости. Все соли, приведенные в ответах, растворимы, то есть являются сильными электролитами. Затем запишите уравнения электролитической диссоциации и используйте их для определения максимального количества ионов в каждом растворе:
а) K2S ⇄ 2K + S 2- , при полной диссоциации 1 моль соли образуется 3 моль ионов, может образоваться не более 3 моль ионов;
б) Ba(ClO3)2 ⇄ Ba 2+ + 2ClO3 – Опять же, при диссоциации 1 моль соли образуется 3 моль ионов, не более 3 моль ионов образуется любым способом;
в) NH4НЕТ3 ⇄ NH4 + + NO3 – При разложении 1 моль нитрата аммония образуется не более 2 моль ионов, не более 2 моль ионов;
г) Fe(NO3)3 ⇄ Fe 3+ + 3NO3 – При полном разложении 1 моль нитрата железа (III) (II) образуется 4 моль ионов. Поэтому при неполном разложении 1 моль нитрата железа может образоваться меньшее количество ионов (неполное разложение возможно в насыщенном растворе соли). Поэтому нам подходит вариант 4.
Электролит является одним из основных компонентов аккумулятора, который позволяет автомобилю заводиться. Он бывает нескольких видов, различающихся по составу. Своевременный контроль количества и качества электролита в батарее может предотвратить преждевременный выход батареи из строя и сэкономить на покупке новой.
Инструкции по замене
Электролит необходимо заменить в следующих случаях
- Электролит в банках с электролитом меняет цветЦвет электролита меняется, он становится мутным. Причиной этого может быть не использование дистиллированной воды для добавки, а обычная вода. Он может содержать примеси, которые вступают в химическую реакцию с электролитом, образуя твердые соединения, которые выпадают в осадок
- После зарядки аккумулятор невозможно получить правильную плотность
- Произошла утечка электролита из-за пренебрежения.
- Новая батарея быстро разряжается. Это может быть вызвано замерзанием раствора

Замена электролита, щелочного или кислотного, требует выполнения нескольких простых действий:
- Извлечение аккумулятора из автомобиля
- Очистка аккумулятора от мусора
- Откачивание имеющейся жидкости с помощью колбы или шприца
- Промывка банок дистиллированной водой
- Заполнение электролитом с помощью воздуходувки или аналогичного устройства
Маркировка на внутренней стороне банок указывает на уровень заполнения. Если их нет, то по эмпирическому правилу электролит должен находиться на 5-7 миллиметров выше пластин. От его уровня до крышек банок должно быть не менее двух сантиметров.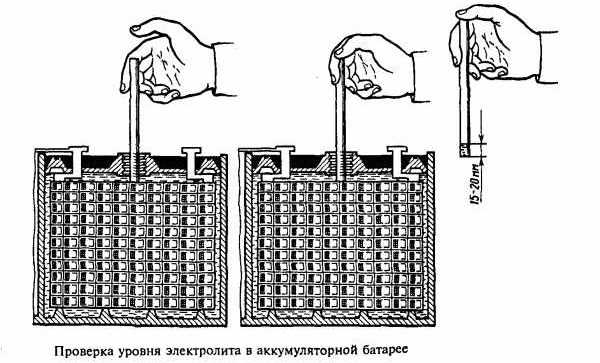
Очень важно при опорожнении электролита не наклонять его набок и особенно не переворачивать вверх дном. На дне банок могут находиться твердые частицы, которые могут застрять в пластинах, делая их совершенно бесполезными. Допускается легкое покачивание воды из стороны в сторону во время мытья, те же действия можно проделать после заливки электролита в аккумулятор.
Затем зарядите батарею и проверьте полученную плотность. Измерения следует проводить не ранее чем через несколько часов после извлечения устройства из зарядного устройства, так как существует риск завышения показаний. Если плотность недостаточно высокая или слишком высокая, ее следует скорректировать путем добавления кислоты, основания или дистиллированной воды.
Читайте далее: