Процесс электролитической диссоциации представлен химическим уравнением, в котором вместо знака равенства написаны одна или две противоположно направленные стрелки. Обычно уравнения электролитической диссоциации не дают формул молекул воды, связанных с ионами в растворе:
Электролиты и неэлектролиты в химии – формулы и определения с примерами
В начале 19 века ученые сделали важное наблюдение: электричество могут проводить не только металлы, но и растворы многих веществ, таких как уксусная кислота, поваренная соль и т.д.
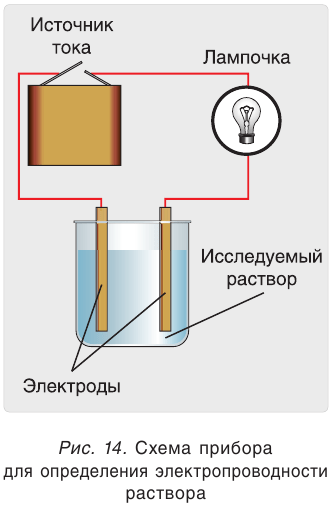
Электропроводность раствора можно определить с помощью прибора, показанного на рис. 14. Два электрода помещаются в раствор и подключаются к источнику тока. Если раствор проводит электричество, то цепь замкнута, о чем свидетельствует вольтметр или светящаяся лампочка.
Когда электроды погружены в дистиллированную воду, лампочка не загорается. Чистая вода не проводит электричество (Рисунок 15). Сухая поваренная соль NaCl также не проводит электричество, когда электроды погружены в нее. Водный раствор той же соли проводит электричество. Можно сделать вывод, что в растворе есть носители электричества – заряженные частицы (ионы). Другие соли, а также основания и кислоты ведут себя в растворах аналогичным образом. Безводный
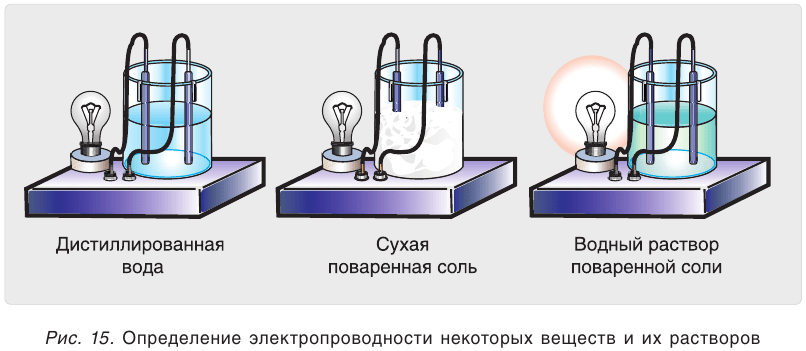
Кислоты являются очень плохими проводниками электричества, но водные растворы многих кислот являются хорошими проводниками. Сплавы ионных соединений – солей и оснований – также проводят электричество.
Мы изучаем электропроводность растворов и таких веществ, как сахароза, глюкоза и спирт. Мы видим, что лампочка в устройстве не светится. Поэтому водные растворы этих веществ не проводят электричество. Это связано с тем, что такие вещества состоят из молекул, которые переходят в раствор, не распадаясь на ионы.
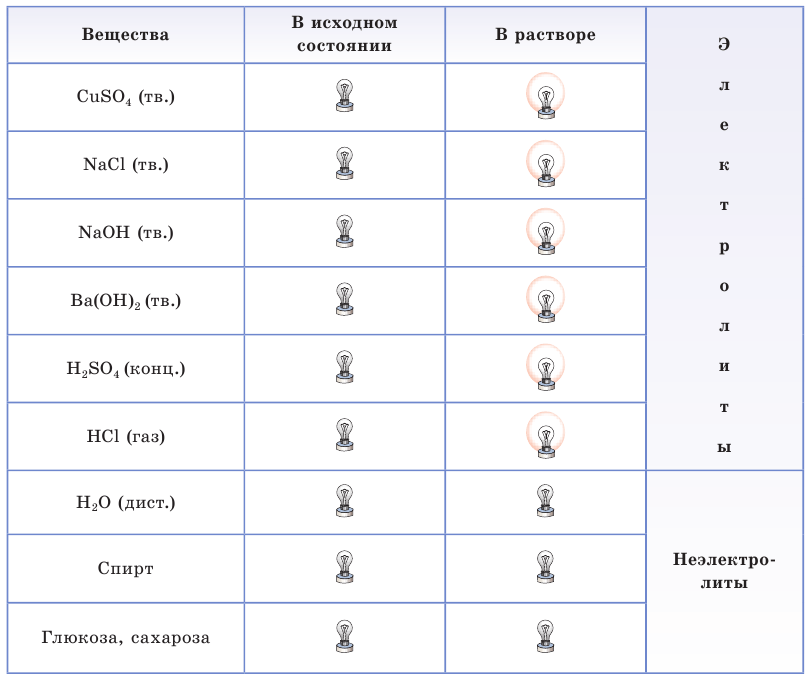
Результаты испытаний на электропроводность веществ в исходном состоянии (твердое тело, жидкость или газ) и их водных растворов приведены в таблице 10.
Таблица 10. Электропроводность некоторых веществ и их растворов
Известный английский физик Майкл Фарадей предложил разделить все вещества в зависимости от их способности проводить электричество в растворенном или расплавленном состоянии на электролиты и неэлектролиты (рис. 16). Термин “электролит” происходит от греческого слова литос – растворился (разложился).
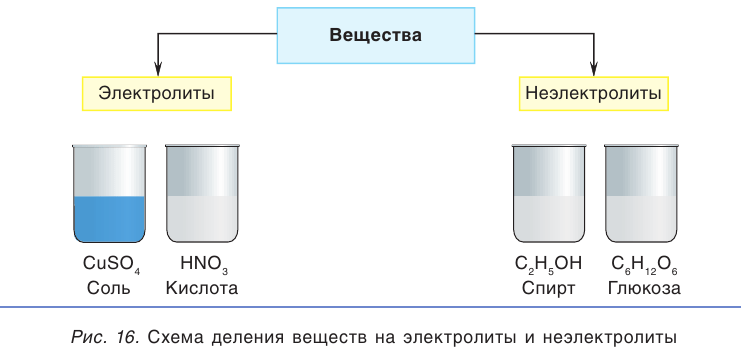
Вещества, водные или расплавленные растворы которых проводят электричество, называются электролитами.
Электролиты включают соединения с ионным типом связи. Это соли 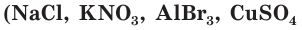 и т.д.) и базы
и т.д.) и базы 
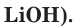 Кристаллы этих веществ состоят из ионов, расположенных в узлах кристаллической решетки и удерживаемых в таком положении электростатическими силами. Когда эти электролиты растворяются в воде, образующие их ионы переходят в раствор.
Кристаллы этих веществ состоят из ионов, расположенных в узлах кристаллической решетки и удерживаемых в таком положении электростатическими силами. Когда эти электролиты растворяются в воде, образующие их ионы переходят в раствор.
Многие кислоты, представляющие собой молекулы с ковалентными полярными связями, также являются электролитами  alt=”Электролиты и неэлектролиты в химии – формулы и определения с примерами” /> и другие).
alt=”Электролиты и неэлектролиты в химии – формулы и определения с примерами” /> и другие).
Вещества, водные растворы или расплавы которых не проводят электричество, называются неэлектролитами.
Большинство органических веществ, таких как сахароза, спирт, глицерин, простые неметаллы и т.д., не являются электролитами. Они существуют в виде неполярных или малополярных молекул, которые распределяются между молекулами воды при растворении в воде.
По способности проводить электричество в растворах и сплавах вещества делятся на электролиты и неэлектролиты.
Электролиты – это вещества, водные или расплавленные растворы которых проводят электричество.
Электролитами являются ионные соединения (основания, соли) и большинство кислот.
Вторичные проводники
Электролиты и неэлектролиты – Информационный бюллетень

Краткий вариант материала по теме “Электролиты и неэлектролиты”. Позволяет быстро сориентироваться в теме, поскольку она представлена в виде таблицы с определениями и примерами. Он поможет вам систематизировать свои знания, подготовиться к тестам и контрольным работам.
Просмотр содержания документа
Шпаргалка “Электролиты и неэлектролиты”
По способности проводить электричество в водном растворе или в расплавленном состоянии

электролиты
неэлектролиты
проводить электричество в растворе или в расплавленном состоянии
(потому что присутствуют заряженные частицы – ионы),
проводники второго типа
не проводят электричество в растворе или в расплавленном состоянии
(потому что они не образуют ионов)
ионная связь или сильно полярная ковалентная связь
кислоты (HCl, HNO3, CH3COOH)базы (KOH, NaOH, Ba(OH)2), соли (KCl, NH4НЕТ3MgSO4), вода
неполярная или слабополярная ковалентная связь
органические соединения (углеводороды, сахароза, спирты),
ЭЛЕКТРОЛИТИКА

степень диссоциации более 30%
степень диссоциации менее 3%
все соли
прочные основания (LiOH, KOH, NaOH, Ba(OH)2))
слабые основания – нерастворимые гидроксиды металлов и NH4OH.
. Степень диссоциации зависит от концентрации вещества в растворе, поэтому некоторые слабые электролиты может, после разбавления может стать сильным.
Степень диссоциации (α) – отношение числа молекул, диссоциировавших на ионы (Nдиссоциация) к общему количеству растворенных молекул (Nвсего.)
_____________________________________________________________________________________
Способность проводить электричество в водном растворе или в расплавленном состоянии

электролиты
неэлектролиты
проводить электричество в растворе или в расплавленном состоянии
(потому что присутствуют заряженные частицы – ионы),
проводники второго типа
не проводят электричество в растворе или в расплавленном состоянии
(потому что они не образуют ионов)
ионная связь или сильно полярная ковалентная связь
кислоты (HCl, HNO3CH3COOH)базы (KOH, NaOH, Ba(OH)2), соли (KCl, NH4НЕТ3MgSO4), вода
неполярная или слабополярная ковалентная связь
органические соединения (углеводороды, сахароза, спирты),
ЭЛЕКТРОЛИТИКА

степень диссоциации более 30%
степень диссоциации менее 3%
все соли
прочные основания (LiOH, KOH, NaOH, Ba(OH)2))
слабые основания – нерастворимые гидроксиды металлов и NH4OH.
. Степень диссоциации зависит от концентрации вещества в растворе, поэтому некоторые слабые электролиты может, после разбавления может стать сильным.
Степень диссоциации (α) – отношение числа молекул, диссоциировавших на ионы (Nдиссоциация) к общему количеству растворенных частиц (Nвсего.)
Существуют также батареи с язычками из пластика, которые помещаются под пробки и опускаются внутрь банки – на 5 мм в жидкость.
Необходимый уровень электролита в аккумуляторе
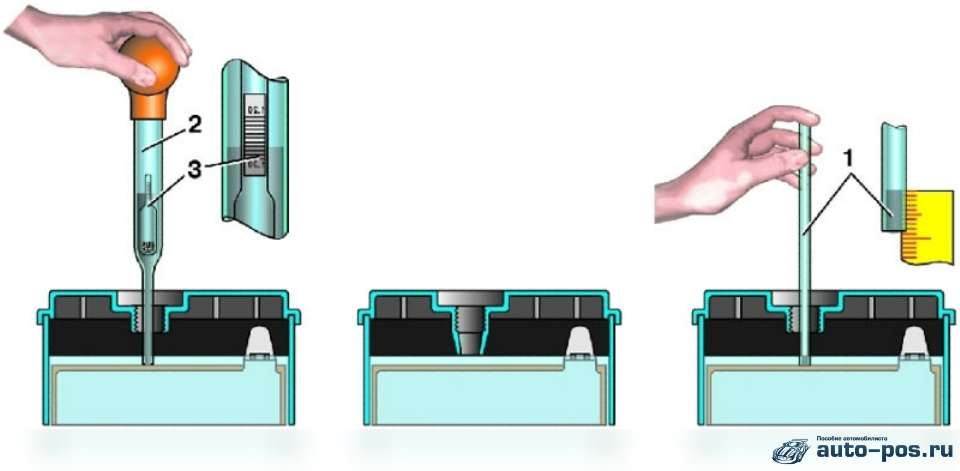
Если у вас обслуживаемая батарея, необходимо регулярно проверять уровень химического раствора в ней.
Если он снизится, долейте чистой воды. Объем аккумулятора также определяет емкость жидкости:
 Эти цифры весьма приблизительны, так как они могут варьироваться – все зависит от модели батареи, методики производства и производителя.
Эти цифры весьма приблизительны, так как они могут варьироваться – все зависит от модели батареи, методики производства и производителя.
Следует помнить об уровне раствора: он должен быть на 10-15 мм выше пластин, т.е. полностью покрывать их.
Сильные электролиты имеют меньшее падение проводимости при более высоких концентрациях, в то время как слабые электролиты имеют большую скорость падения проводимости при более высоких концентрациях.
Методы определения электролитов
Существуют методы, облегчающие определение электролитов. Ниже приводится шестиступенчатый метод:
- Является ли ваш электролит одной из семи сильных кислот?
- Встречается в металлической форме (OH)N? Тогда это прочная основа.
- Он находится в металлической форме (X)N? Тогда это соль.
- Ваша формула начинается на H? Если да, то это, вероятно, слабая кислота.
- Есть ли в нем атом азота? Тогда это может быть слабая база.
- Применимо ли что-либо из вышеперечисленного? Если да, то это не электролит.
Более того, если реакция, представленная электролитом, протекает следующим образом: NaCl (s) → Na + (ac) + Cl – (ac), в котором реакция ограничена прямой реакцией (→), он является сильным электролитом. Если он ограничен косвенным (↔), то это слабый электролит.
Как было сказано в предыдущей главе, проводимость электролита зависит от его концентрации в растворе, а также от силы электролита.
При более высоких концентрациях сильные и промежуточные электролиты не будут диссоциировать через значительные промежутки времени, но слабые электролиты будут значительно диссоциировать, пока не достигнут значений, близких к нулю при более высоких концентрациях…..
Существуют также промежуточные электролиты, которые могут диссоциировать в растворах с более высокой процентной концентрацией (менее 100%, но более 10%), и неэлектролиты, которые просто не диссоциируют (углеродные соединения, такие как сахара, жиры и спирты).
Исходя из степени диссоциации, электролиты делятся на сильные, слабые и умеренно сильные.
Электролиты и неэлектролиты

Электролиты это вещества, водные или расплавленные растворы которых проводят электричество. Электролитическая диссоциация это распад электролитов в растворах или расплавах на ионы.
Степень диссоциации это отношение числа N1 к общему числу растворенных молекул N. Он обозначается символом α, определяется экспериментально и выражается в долях единицы или в процентах:
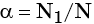
Степень диссоциации электролитов существенно зависит от типа электролита и растворителя, концентрации и температуры раствора. По мере уменьшения концентрации взаимодействие ионов в растворе, приводящее к образованию частиц, уменьшается, а степень диссоциации увеличивается. Как правило, степень диссоциации увеличивается с повышением температуры.
По степени диссоциации электролиты делятся на сильные, слабые и умеренно сильные электролиты.
Сильные электролиты – это вещества, которые почти полностью диссоциируют на ионы: HCl, HNO3, H2SO4HI, KOH, NaOH и многие водорастворимые соли (NaCl, K2SO4). Степень диссоциации этих электролитов составляет > 0,3.
Слабые электролиты – это вещества, которые диссоциируют незначительно, например, H3BO3, CH3COOH, HCN, H2S. Степень диссоциации этих электролитов составляет < 0,03.
Электролиты средней силы – это вещества, в растворах которых число диссоциирующих молекул примерно равно числу недиссоциированных молекул, например, H2SO3, HNO2, H3PO4 и т.д. Их степень диссоциации варьируется от 0,03 до 0,3.
Эта классификация весьма условна и применима к растворам электролитов 5-10% концентрации. Следует отметить, что в бесконечно разбавленных растворах степень диссоциации любого (даже слабого!) электролита близка к 1.
В электрохимической промышленности электролиты составляют основу растворов для гальванического покрытия металлов: хромирование, кадмирование, цинкование, золочение, фосфатирование и т.д. Электролиты используются для травления металлов. Медицина и биология также имеют дело с электролитами.
Неэлектролиты – это вещества, растворы или расплавы которых не проводят электричество. К неэлектролитам относятся, например, водород, кислород, сахар, бензол, эфир и многие другие органические вещества. Молекулы этих веществ содержат ковалентные малополярные и неполярные связи.
Степень диссоциации – это отношение числа молекул, диссоциированных на ионы, к общему числу молекул в растворе. Сильные ЭЛЕКТРОЛИТЫ почти полностью диссоциируют на ионы при растворении в воде. … МЕДЛЕННЫЕ ЭЛЕКТРОЛИТЫ В водных растворах они диссоциируют на ионы лишь частично (обратимо).
Читайте далее:- Электролит (химия) – это. Что такое электролит (химия)?.
- Что такое электродный потенциал; Школа для инженеров-электриков: электротехника и электроника.
- Тонкости электропроводности.
- Как работает pH-электрод.
- Электрический заряд и элементарные частицы. Закон сохранения заряда.
- Электрический ток в электролитах.
- Гальванические элементы – устройство, принцип действия, виды и основные характеристики; Сайт для электриков – статьи, советы, примеры, схемы.