Анод (+): 2 Cl – – 2ē → Cl2 0
Электролиз
Химические реакции с переносом электронов (окислительно-восстановительные реакции) делятся на два типа: спонтанные реакции и реакции, которые происходят в результате пропускания тока через раствор или расплавленный материал. Электролит.
Раствор электролита или расплавленный электролит помещается в специальную емкость – сосуд электролитическая ванна .
Электрический ток – это упорядоченное движение заряженных частиц – ионов, электронов и т.д. под воздействием внешнего электрического поля. Электрическое поле в растворе или в расплавленном электролите создается за счет электроды .
Электроды – обычно представляют собой стержни из электропроводящего материала. Их помещают в раствор или расплавленную жидкость электролити подключен к электрической цепи с источником питания.
Отрицательно заряженный электрод – это катод – притягивает положительно заряженные ионы – . Положительно заряженный электрод ( анод ) притягивает отрицательно заряженные частицы ( анионы ). Катод действует как восстановитель, а анод – как окислитель.
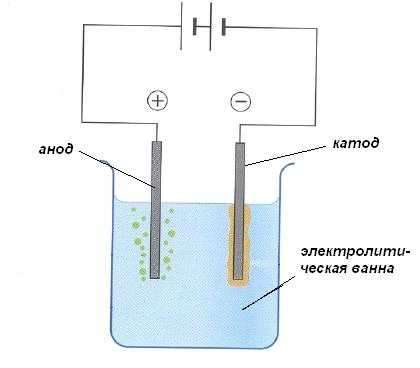
Различают электролиз с активный и инертный электроды. Активные (растворимые) электроды претерпевают химические изменения в процессе электролиза. Обычно они изготавливаются из меди, никеля и других металлов. Инертные (нерастворимые) электроды не претерпевают химических изменений. Они изготавливаются из инертных металлов, таких как платина и никель, платина или графит .
Не все вещества подвергаются электролизу при контакте с электрическим током. Существуют определенные закономерности и принципы.
Содержание
В 1832 году. Фарадей установил, что масса m вещества, выделяющегося на электроде, прямо пропорциональна электрическому заряду q, протекающему через электролит: 
Если постоянный ток I пропускается через электролит в течение времени t. Коэффициент пропорциональности 
Если постоянный ток I пропускается через электролит в течение времени t. Коэффициент пропорциональности
k” width=”” height=””> называется электрохимический эквивалент вещества. Она численно равна массе вещества, высвобождаемого при прохождении через электролит единичного электрического заряда, и зависит от химической природы вещества.
Происхождение закона Фарадея
(4)
 (4)
(4) где z – валентность атома (иона) вещества, e – заряд электрона (5)
Подставляя (2)-(5) в (1), получаем
Для чего он используется
Электролиз широко используется для осуществления следующих процессов:
- Получение веществ в чистом виде. Этот процесс используется для обработки горных пород и получения чистых веществ. В результате образуются алюминий, диоксид марганца, водород и перекись водорода.
- Очистка сточных вод.Помещая электролиты в такие растворы, он не только дезинфицирует воду, но и создает суспензию, которая выпадает в осадок.
- Тонкое покрытие: когда ионы металла осаждаются на объекте, они образуют тонкий декоративный или защитный слой.
На самом деле, список гораздо обширнее, поскольку разность потенциалов может быть использована для достижения значительных эффектов в различных целях при минимальных затратах.
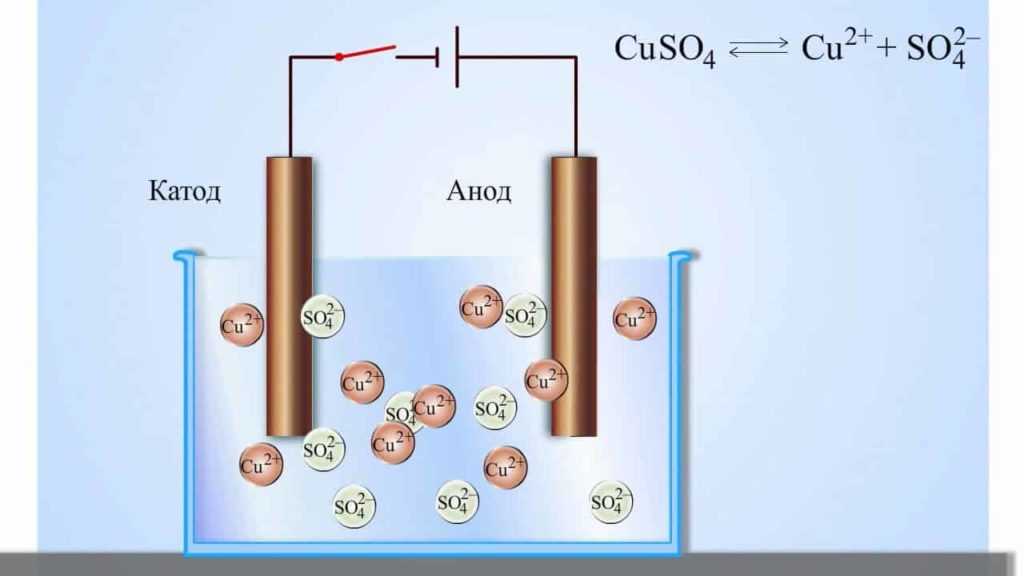
В растворе происходит процесс электролитической диссоциации:
Электролиз сплавов и растворов
Если опустить электроды в раствор или расплавленный электролит и пропустить электрический ток, ионы будут двигаться направленно: катионы к катоду (отрицательно заряженный электрод), а анионы к аноду (положительно заряженный электрод).
На катоде катионы получают электроны и восстанавливаются; на аноде анионы отдают электроны и окисляются. Этот процесс называется электролизом.
Электролиз – это окислительно-восстановительный процесс, происходящий на электродах при пропускании электрического тока через расплавленный или растворенный электролит.
Электролиз расплавленных солей
Рассмотрим процесс электролиза расплавленного хлорида натрия. В расплавленном материале происходит процесс термической диссоциации:
Под действием электрического тока катионы $Na^<+>$ перемещаются к катоду и принимают от него электроны:
Анионы $Cl^<->$ движутся к аноду и отдают электроны:
Полное уравновешивание процессов:
На катоде образуется металлический натрий, а на аноде – газообразный хлор.
Главное помнить, что при электролизе химическая реакция протекает с использованием электрической энергии, что не может произойти спонтанно.
Электролиз водных растворов электролитов
Более сложным случаем является электролиз растворов электролитов.
В солевом растворе, помимо ионов металлов и кислотных остатков, присутствуют молекулы воды. Поэтому при рассмотрении процессов, происходящих на электродах, необходимо учитывать их участие в электролизе.
Существуют следующие правила определения продуктов электролиза водных растворов электролитов:
1. Процесс на катоде Процесс, происходящий на катоде, зависит не от материала катода, а от положения металла (катиона электролита) в электрохимическом ряду напряжений, и если
1.1 Катион электролита находится в начале ряда напряжений до $Al$ включительно, затем на катоде происходит восстановление воды (выделяется водород $H_2↑$). Катионы металлов не восстанавливаются, они остаются в растворе.
1.2 Катион электролита находится в диапазоне напряжений между алюминием и водородом, тогда ионы металла и молекулы воды одновременно восстанавливаются на катоде.
1.3 Если катион электролита находится в диапазоне напряжений после водорода, то восстановление катионов металла происходит на катоде.
1.4 Если в растворе находятся катионы различных металлов, то первым восстанавливается катион металла, стоящий правее в ряду напряжений.
Катодные процессы
| $Li K Ca Ca Na Mg Al$ $Li^ <+>K^ <+>Ca^ <2+>Na^ <+>Mg^ <2+>Al^<3+>$. |
$Mn Zn Fe Ni Sn Pb$. $Mn^ <2+>Zn^ <2+>Fe^ <2+>Ni^ <2+>Sn^ <2+>Pb^<2+>$. |
$H_2$ $2H^<+>$ |
$Cu Hg Ag Pt Au$ $Cu^ <2+>Hg_2^ <2+>Ag^ <+>Pt^ <2+>Au^<3+>$. |
| Количество воды уменьшается: $2H_2O+2ē=H_2↑+2OH^<−>;$ $M^ |
Катионы металлов и вода восстанавливаются: $M^ $2H_2O+2ē=H_2↑+2OH^<−>$ |
Катионы металлов подвергаются восстановлению: $M^ |
|
| $nē→$ Усиление окислительных свойств катионов (способность принимать электроны) |
|||
2. Процесс на аноде Зависит от материала анода и типа аниона.
Анодные процессы
| Кислотный остаток $Ac^ |
Анод | |
| Растворимый | Нерастворимый | |
| Без кислот | Окисление металла анода $M^<->-nē=M^ анодный раствор |
Окисление аниона (кроме $F^<->$) $Ac^ |
| Содержащие кислород | В кислой и нейтральной среде: $2H_2O−4ē=O_2↑+4H^<+>$ В щелочных средах: $4OH^<−>−4ē=O_2↑+4H^<+>$ |
|
2.1 Если анод растворяется (железо, цинк, медь, серебро и все металлы, которые окисляются при электролизе) анодный металл окисляется, независимо от природы аниона.
2.2 Если анод не растворяется (это так называемые нейтральные – графит, золото, платина) затем:
(a) при электролизе солевых растворов анаэробные кислоты (за исключением фторидов) происходит окисление анионов на аноде;
(b) при электролизе солевых растворов (b) при электролизе растворов кислот, содержащих кислород и фториды окисление воды происходит на аноде (выделяя $O_2↑$). Анионы не окисляются, они остаются в растворе;
(c) анионы расположены в следующем порядке в соответствии с их способностью к окислению:

Давайте попробуем применить эти принципы к конкретным ситуациям.
Рассмотрим электролиз раствора хлорида натрия, когда анод нерастворим, а анион растворим.
1) Анод нерастворимый (например, графит).
В растворе происходит процесс электролитической диссоциации:
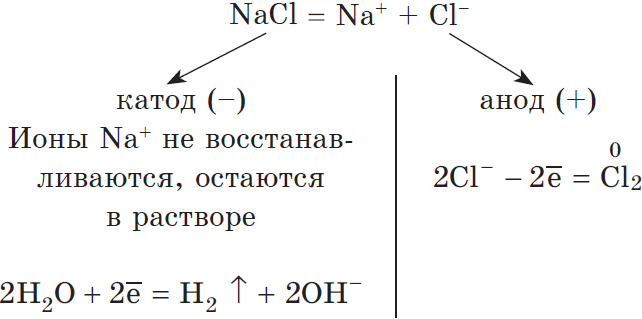
Учитывая наличие ионов $Na^<+>$ в растворе, мы выводим молекулярное уравнение:
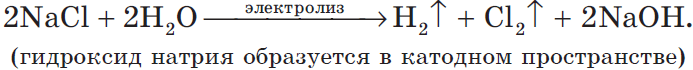
2) Анодом является растворимый (например, медь):
Если анод растворим, то анодный металл окисляется:
Катионы $Cu^<2+>$ стоят после ($H^<+>$) в ряду напряжений, поэтому они будут восстановлены на катоде.
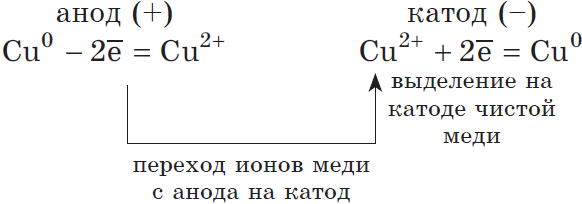
Концентрация $NaCl$ в растворе не меняется.
Рассмотрим электролиз раствора сульфата меди (II) (VI) при нерастворимый анод:
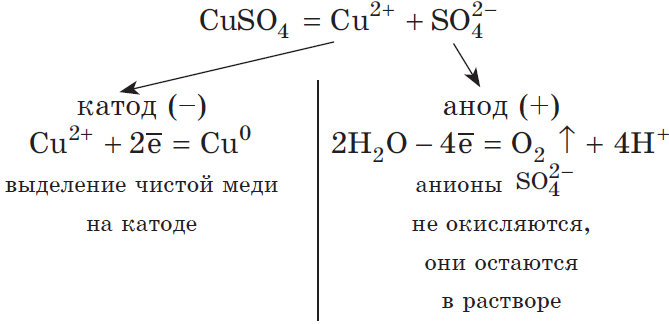
Общее ионное уравнение:
Полное молекулярное уравнение, учитывающее наличие в растворе анионов $SO_4^<2->$:
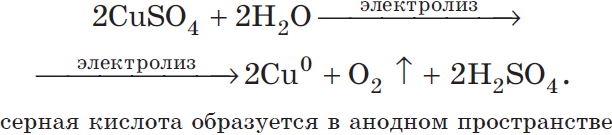
Рассмотрим электролиз раствора гидроксида калия при температуре нерастворимый анод:
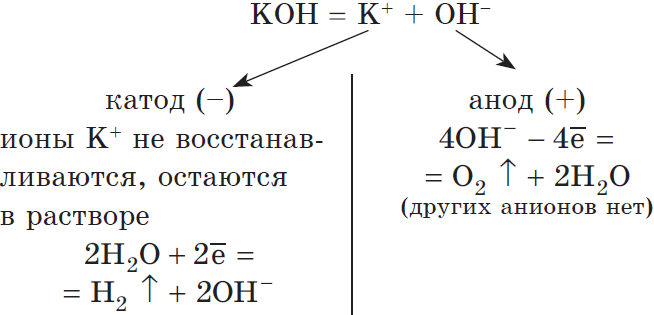
Общее ионное уравнение:
Полное молекулярное уравнение:
В этом случае получается, что происходит только электролиз воды. Аналогичный результат получен при электролизе растворов $H_2SO_4$, NaNO_3$, K_2SO_4$ и др.
Электролиз сплавов и растворов веществ широко используется в промышленности:
Очень важно не путать такие близкие определения, как гидролиз и электролиз. Первое явление – это распад раствора вещества на ионы (заряженные молекулы) в воде.
Первый закон Фарадея
Первый закон Фарадея гласит, что существует прямая зависимость между массой вещества, выделяющегося при электролизе, и величиной заряда, прошедшего через электролит.

Этот принцип подтверждается формулой m = k * qкоторая представляет собой произведение заряда вещества на его электрохимический эквивалент, равный его массе.
Проверка первого закона Фарадея заключается в следующем:
возьмите любые три электролита, например, A, B и C, и пропустите через каждый из них ток;
Если вещества одинаковы, то высвободившиеся массы можно назвать G, G1 и G2;
тогда будет справедливо следующее уравнение: G= G1+G2.
Электрохимический процесс, такой как электролиз, примеры которого можно увидеть повсюду, является неотъемлемой частью промышленности:
Практическое применение в производстве
Электрохимический процесс, такой как электролиз, примеры которого можно увидеть повсюду, является неотъемлемой частью промышленности:
- производство химически чистого сырья, такого как фтор, хлор, щелочи, чистый водород и кислород и т.д;
- использование электролиза в гидрометаллургии: переработка сырья, содержащего металлы;
- электрорафинирование (с использованием растворимых анодов) для окончательной очистки металлов;
- электроэкстракция (с использованием нерастворимых анодов) для выделения нужных металлов из растворов;
- Гальванические процессы: гальваника и гальваническое покрытие.
Информация. Процессы электролиза не протекают бесконтрольно. Медный кулонометр подключен к цепи электролизера. Единицей измерения является 1 Кл (кулон). В этом случае количество результата (продукта) анодной, катодной реакций контролируется при 100% мощности тока, необходимой для протекания реакции.
Гальваностегия – это метод электрохимического покрытия металлических поверхностей другими металлами:
- сталь никелированная, хромированная, оцинкованная;
- Медь покрывается серебром, никелем и другими металлами.
Поверхность подложки обрабатывается таким образом, чтобы покрытие было стойким и защищало конструкцию от внешних воздействий. В то же время изделиям придается эстетичный внешний вид.
Процесс гальванопластики позволяет изготавливать точные копии предметов из драгоценных металлов. Он широко используется в производстве штампов, копий скульптур, ювелирных изделий и деталей со сложной геометрией. В этом процессе важно, чтобы заготовка была отделена от покрытия.

Электролиз открывает широкие возможности для работы с металлами и электролитами. С помощью этого процесса можно не только наносить гальванические покрытия в одиночку, но и получать чистые металлы в небольших количествах. Спонтанные химические реакции, происходящие в гальванических камерах, не следует путать с реакциями, происходящими в электролизерах.
Читайте далее:- Что такое электродный потенциал; Школа для инженеров-электриков: электротехника и электроника.
- Электролит (химия) – это. Что такое электролит (химия)?.
- Электрический ток в электролитах.
- Типы эмиссии электронов.
- Топливные элементы/.
- Как работает pH-электрод.
- Гальванические элементы – устройство, принцип действия, виды и основные характеристики; Сайт для электриков – статьи, советы, примеры, схемы.