Изменение значения pH в зависимости от температуры
БАССЕЙНЫ
Вы находитесь здесь: Главная  Статьи
Статьи  Библиотека статей
Библиотека статей  Как работает и работает pH-электрод
Как работает и работает pH-электрод
Как работает и функционирует pH-электрод в станциях дозирования химических веществ
Электрод pH предназначен для измерения количества ионов водорода (H+) в воде бассейна. Чем выше количество водородных ионов и ниже количество гидроксильных групп (OH-), тем ниже pH и наоборот.  Чем ниже pH, тем более кислая среда, чем выше, тем более щелочная. В случае плавательного бассейна значение pH влияет на способность хлора действовать, поэтому состояние воды в бассейне всегда оценивается, начиная со значения pH. При регулярном регулярное обслуживание бассейна (сервис) Измерение значения pH является важным пунктом во всем перечне работ. Принцип измерения pH
Чем ниже pH, тем более кислая среда, чем выше, тем более щелочная. В случае плавательного бассейна значение pH влияет на способность хлора действовать, поэтому состояние воды в бассейне всегда оценивается, начиная со значения pH. При регулярном регулярное обслуживание бассейна (сервис) Измерение значения pH является важным пунктом во всем перечне работ. Принцип измерения pH 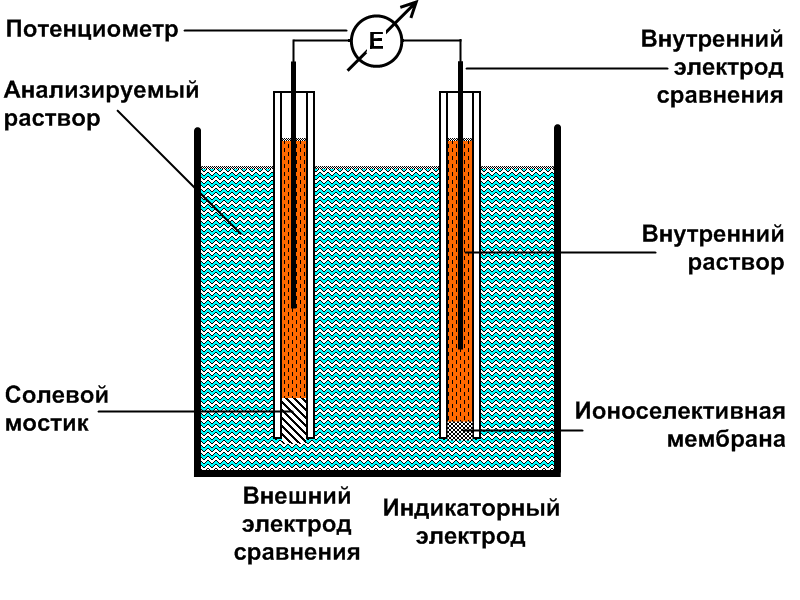 Схема измерения pH состоит из двух электродов, один из которых является электродом сравнения, а другой – измерительным электродом. Гальваническая разность потенциалов между этими электродами измеряется ph-метром, он же высокоомный миливольтметр. Измерительный электрод представляет собой ионоселективную мембрану, предназначенную для пропускания определенного типа ионов, в данном случае ионов водорода. Мембрана изготавливается из специального натриевого или литиевого стекла толщиной 0,006 – 0,1 мм сферической формы. Потенциал электрода сравнения (хлоридсеребряного электрода) является постоянным или эталонным и не изменяется при изменении pH воды. Разность потенциалов между двумя электродами для простоты называют потенциалом измерительного электрода (E), а сам метод измерения pH – потенциометрическим. Потенциал измерительного электрода зависит от концентрации или активности ионов водорода. Он рассчитывается по формуле Нернста. Ввиду отсутствия химической подготовки у большинства специалистов по бассейнам, мы не будем приводить ее здесь. Однако это приводит к простой зависимости потенциала E от pH. Эта зависимость называется водородной характеристикой электрода, а наклон водородной характеристики – наклоном. Именно этот уклон рассчитывается и отображается на экранах некоторых контроллеров станций дозирования для оценки пригодности электрода для дальнейшей эксплуатации или требуемой замены на новый электрод. Во время работы крутизна электрода постепенно уменьшается. Электрическая схема
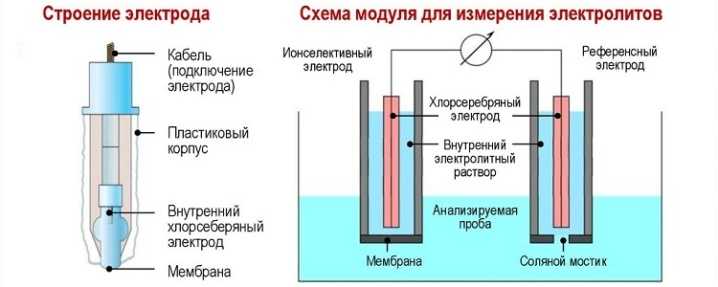
Схема измерения pH состоит из двух электродов, один из которых является электродом сравнения, а другой – измерительным электродом. Гальваническая разность потенциалов между этими электродами измеряется ph-метром, он же высокоомный миливольтметр. Измерительный электрод представляет собой ионоселективную мембрану, предназначенную для пропускания определенного типа ионов, в данном случае ионов водорода. Мембрана изготавливается из специального натриевого или литиевого стекла толщиной 0,006 – 0,1 мм сферической формы. Потенциал электрода сравнения (хлоридсеребряного электрода) является постоянным или эталонным и не изменяется при изменении pH воды. Разность потенциалов между двумя электродами для простоты называют потенциалом измерительного электрода (E), а сам метод измерения pH – потенциометрическим. Потенциал измерительного электрода зависит от концентрации или активности ионов водорода. Он рассчитывается по формуле Нернста. Ввиду отсутствия химической подготовки у большинства специалистов по бассейнам, мы не будем приводить ее здесь. Однако это приводит к простой зависимости потенциала E от pH. Эта зависимость называется водородной характеристикой электрода, а наклон водородной характеристики – наклоном. Именно этот уклон рассчитывается и отображается на экранах некоторых контроллеров станций дозирования для оценки пригодности электрода для дальнейшей эксплуатации или требуемой замены на новый электрод. Во время работы крутизна электрода постепенно уменьшается. Электрическая схема 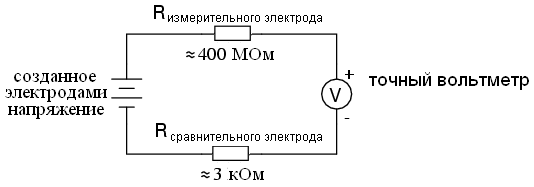 На водородный показатель влияет изменение температуры при одном и том же значении pH: при повышении температуры наклон увеличивается. Теоретическая крутизна должна составлять 59,16 мВ/pH, но по разным причинам она ниже. Если наклон водородной кривой электрода падает ниже 50 мВ/pH, электрод следует заменить на новый. Как правило, производитель раздаточных станций в своих инструкции Производитель указывает, что электроды являются расходным материалом и рассчитаны только на один год работы. Часто, при отсутствии должного обслуживания, это не учитывается, и электроды “работают” несколько лет, пока станция не выкачает целую канистру какого-нибудь химиката. Если наклон электрода падает ниже допустимого, его можно реанимировать, а иногда, если не запускать, электрод соглашается продолжать работать. ( см. Методы реанимации ) Наклон электродной функции может быть рассчитан по формуле s=(U2-U1)/(pH2-pH1. Жаль только, что в техническое помещение Жаль, что в техническом помещении бассейна нет лабораторных условий для таких измерений. Структура электрода для измерения рН
На водородный показатель влияет изменение температуры при одном и том же значении pH: при повышении температуры наклон увеличивается. Теоретическая крутизна должна составлять 59,16 мВ/pH, но по разным причинам она ниже. Если наклон водородной кривой электрода падает ниже 50 мВ/pH, электрод следует заменить на новый. Как правило, производитель раздаточных станций в своих инструкции Производитель указывает, что электроды являются расходным материалом и рассчитаны только на один год работы. Часто, при отсутствии должного обслуживания, это не учитывается, и электроды “работают” несколько лет, пока станция не выкачает целую канистру какого-нибудь химиката. Если наклон электрода падает ниже допустимого, его можно реанимировать, а иногда, если не запускать, электрод соглашается продолжать работать. ( см. Методы реанимации ) Наклон электродной функции может быть рассчитан по формуле s=(U2-U1)/(pH2-pH1. Жаль только, что в техническое помещение Жаль, что в техническом помещении бассейна нет лабораторных условий для таких измерений. Структура электрода для измерения рН 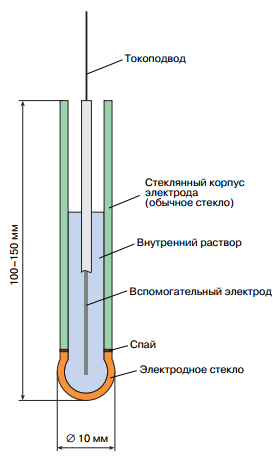
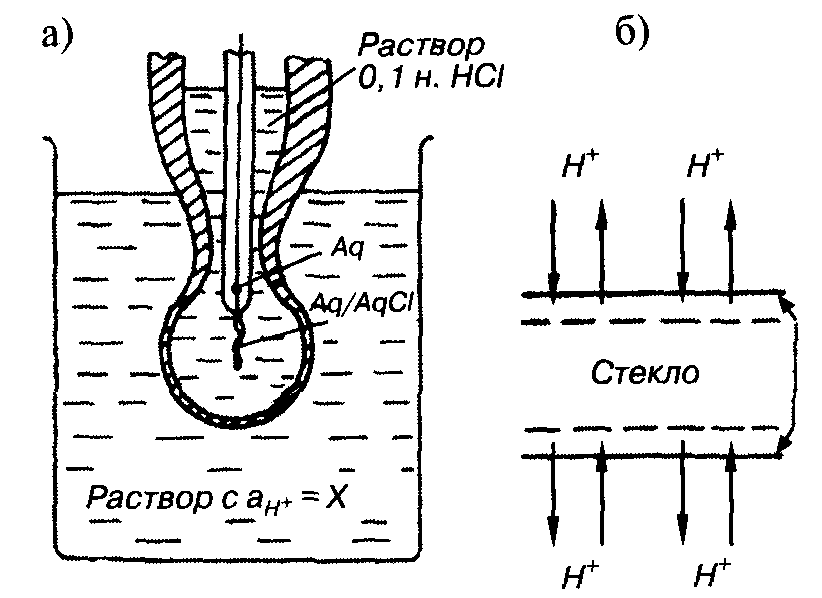 Измерительный электрод представляет собой стеклянный цилиндр со сферическим наконечником электрода из литиевого стекла, припаянным с одной стороны, и резьбовым разъемом, соединяющим хлорсеребряный электрод (Ag/AgCl) с коаксиальным помехоустойчивым кабелем с другой стороны. Полость внутри электрода заполнена высоковязким гелем KCl. Стекло электрода имеет сферическую форму и припаяно к стеклянному корпусу электрода. Толщина этой стеклянной мембраны составляет от 0,006 до 0,1 мм. Стеклянная мембрана обладает способностью избирательно пропускать только ионы водорода в обоих направлениях. На поверхности мембраны образуются гелевые пленки, которые способствуют селективности по отношению к ионам водорода. Направление движения ионов зависит от их концентрации в электролите: поток ионов направлен туда, где их меньше. В результате этой диффузии возникает электродный потенциал. Рассмотренная выше двухэлектродная система может быть объединена в один электрод и называется комбинированным электродом из-за наличия в одном корпусе измерительного и опорного электродов. Внешний корпус может быть выполнен из стекла или прозрачного пластика. Пластиковый корпус электрода более неприхотлив и ударопрочен, но внутренняя часть по-прежнему стеклянная, поэтому не стоит пытаться использовать его в качестве противоударных часов.
Измерительный электрод представляет собой стеклянный цилиндр со сферическим наконечником электрода из литиевого стекла, припаянным с одной стороны, и резьбовым разъемом, соединяющим хлорсеребряный электрод (Ag/AgCl) с коаксиальным помехоустойчивым кабелем с другой стороны. Полость внутри электрода заполнена высоковязким гелем KCl. Стекло электрода имеет сферическую форму и припаяно к стеклянному корпусу электрода. Толщина этой стеклянной мембраны составляет от 0,006 до 0,1 мм. Стеклянная мембрана обладает способностью избирательно пропускать только ионы водорода в обоих направлениях. На поверхности мембраны образуются гелевые пленки, которые способствуют селективности по отношению к ионам водорода. Направление движения ионов зависит от их концентрации в электролите: поток ионов направлен туда, где их меньше. В результате этой диффузии возникает электродный потенциал. Рассмотренная выше двухэлектродная система может быть объединена в один электрод и называется комбинированным электродом из-за наличия в одном корпусе измерительного и опорного электродов. Внешний корпус может быть выполнен из стекла или прозрачного пластика. Пластиковый корпус электрода более неприхотлив и ударопрочен, но внутренняя часть по-прежнему стеклянная, поэтому не стоит пытаться использовать его в качестве противоударных часов. 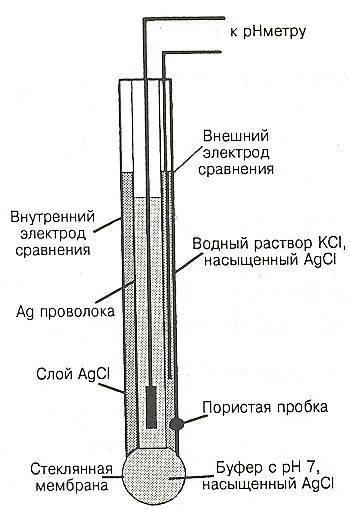
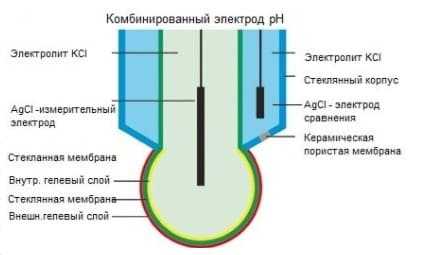
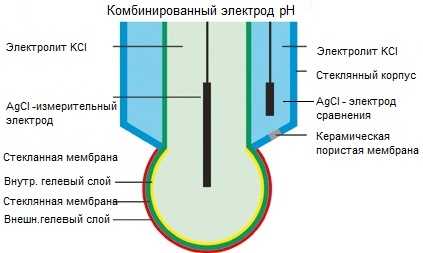 Комбинированный электрод pH сконструирован аналогично отдельным электродам для измерения и сравнения pH. Оба электрода изготовлены из хлорсеребра, вспомогательный электрод запаян и не течет. Полости электродов заполнены 3 моль/л раствором KCl. Ввод электродов в эксплуатацию Электроды вводятся в эксплуатацию во время общего ввода бассейна в эксплуатацию. ввод бассейна в эксплуатацию запуск после установки. Электроды поставляются упакованными в картонные коробки, снова погруженными в 3 моль/л раствор KCl. Хорошо хранить ампулы (посуду) для консервации вместе с раствором, потому что они могут понадобиться позже для восстановления гелевого слоя и пористой керамической пробки электрода сравнения. До дисконтирования ( весеннее обслуживание бассейна ), заполните измерительную кювету водой и внимательно осмотрите электрод, если он оттаял, треснул или сломан. Царапина на стекле электрода также будет считаться некачественной. Проверьте наличие пузырьков воздуха в растворах, залитых в электрод, встряхните электрод, как вы это делали с ртутным термометром, выпустите пузырьки вверх. Осторожно, не касаясь стеклянного кончика электрода, окуните электрод в кювету, закрутите резьбу до полного резинового уплотнения. Не протирайте стеклянный шар ничем, особенно чем-то грубым или абразивным. Гелевый слой и само стекло не должны быть повреждены. Если слой геля еще можно реанимировать, электрод можно отбраковать после повреждения стекла. Не перекручивайте разъем коаксиального кабеля при его вкручивании. Подключите разъем кабеля к соответствующему разъему pH на измерительной станции. Пропустите измеряемую воду через кювету со скоростью потока 2-3 м/с. Некоторые станции дозирования имеют поплавок с герконом или ротаметр в кювете, который точно измеряет скорость потока. Более простые станции не имеют таких устройств, и расход определяется “на глаз”. Электродам необходимо некоторое время для адаптации к условиям измерения, после чего их следует откалибровать. Электроды, хранившиеся в течение длительного времени (более 18 месяцев), даже при хранении в соответствующих условиях, могут не проявить своих свойств и, к сожалению, должны быть выброшены. Между поставкой оборудования для водоподготовки и вводом бассейна в эксплуатацию всегда проходит некоторое время, поэтому перед использованием электроды рекомендуется замочить на некоторое время в 0,1 М растворе HCl. При хранении электродов, например, на зимний период или по другим важным причинам, электроды могут храниться без потери работоспособности. Для сохранения электродов используются ампулы, в которые они упакованы производителем. В качестве консервирующей жидкости может использоваться KCl, буферный раствор pH4 или водопроводная вода. Стеклянная мембрана должна постоянно поддерживаться во влажном состоянии для сохранения гелевого слоя. Если электрод по какой-то причине высох, можно попробовать реанимировать его, поместив в раствор 3M KCl на 24 часа или хотя бы на ночь, для ускорения процесса можно нагреть раствор до 60 градусов, время сократится до 6 часов. Если электрод долгое время находился в сухом состоянии, он может вообще не выйти из комы или долгое время не функционировать. Для травления стеклянной мембраны и активации гелевого слоя производители электродов рекомендуют погружать их в слабый раствор (10%) фторида аммония на 60 секунд с последующим немедленным погружением в 5М раствор HCl для нейтрализации предыдущего реактива. Утром снова промойте в воде и откалибруйте. Очистка электродов для обслуживание В процессе эксплуатации на поверхности стеклянной мембраны и пористой керамической пробки могут откладываться различные слои, препятствующие нормальному ионному обмену и, как следствие, искажающие показания электрода. Для удаления этих слоев используются различные вещества.
Комбинированный электрод pH сконструирован аналогично отдельным электродам для измерения и сравнения pH. Оба электрода изготовлены из хлорсеребра, вспомогательный электрод запаян и не течет. Полости электродов заполнены 3 моль/л раствором KCl. Ввод электродов в эксплуатацию Электроды вводятся в эксплуатацию во время общего ввода бассейна в эксплуатацию. ввод бассейна в эксплуатацию запуск после установки. Электроды поставляются упакованными в картонные коробки, снова погруженными в 3 моль/л раствор KCl. Хорошо хранить ампулы (посуду) для консервации вместе с раствором, потому что они могут понадобиться позже для восстановления гелевого слоя и пористой керамической пробки электрода сравнения. До дисконтирования ( весеннее обслуживание бассейна ), заполните измерительную кювету водой и внимательно осмотрите электрод, если он оттаял, треснул или сломан. Царапина на стекле электрода также будет считаться некачественной. Проверьте наличие пузырьков воздуха в растворах, залитых в электрод, встряхните электрод, как вы это делали с ртутным термометром, выпустите пузырьки вверх. Осторожно, не касаясь стеклянного кончика электрода, окуните электрод в кювету, закрутите резьбу до полного резинового уплотнения. Не протирайте стеклянный шар ничем, особенно чем-то грубым или абразивным. Гелевый слой и само стекло не должны быть повреждены. Если слой геля еще можно реанимировать, электрод можно отбраковать после повреждения стекла. Не перекручивайте разъем коаксиального кабеля при его вкручивании. Подключите разъем кабеля к соответствующему разъему pH на измерительной станции. Пропустите измеряемую воду через кювету со скоростью потока 2-3 м/с. Некоторые станции дозирования имеют поплавок с герконом или ротаметр в кювете, который точно измеряет скорость потока. Более простые станции не имеют таких устройств, и расход определяется “на глаз”. Электродам необходимо некоторое время для адаптации к условиям измерения, после чего их следует откалибровать. Электроды, хранившиеся в течение длительного времени (более 18 месяцев), даже при хранении в соответствующих условиях, могут не проявить своих свойств и, к сожалению, должны быть выброшены. Между поставкой оборудования для водоподготовки и вводом бассейна в эксплуатацию всегда проходит некоторое время, поэтому перед использованием электроды рекомендуется замочить на некоторое время в 0,1 М растворе HCl. При хранении электродов, например, на зимний период или по другим важным причинам, электроды могут храниться без потери работоспособности. Для сохранения электродов используются ампулы, в которые они упакованы производителем. В качестве консервирующей жидкости может использоваться KCl, буферный раствор pH4 или водопроводная вода. Стеклянная мембрана должна постоянно поддерживаться во влажном состоянии для сохранения гелевого слоя. Если электрод по какой-то причине высох, можно попробовать реанимировать его, поместив в раствор 3M KCl на 24 часа или хотя бы на ночь, для ускорения процесса можно нагреть раствор до 60 градусов, время сократится до 6 часов. Если электрод долгое время находился в сухом состоянии, он может вообще не выйти из комы или долгое время не функционировать. Для травления стеклянной мембраны и активации гелевого слоя производители электродов рекомендуют погружать их в слабый раствор (10%) фторида аммония на 60 секунд с последующим немедленным погружением в 5М раствор HCl для нейтрализации предыдущего реактива. Утром снова промойте в воде и откалибруйте. Очистка электродов для обслуживание В процессе эксплуатации на поверхности стеклянной мембраны и пористой керамической пробки могут откладываться различные слои, препятствующие нормальному ионному обмену и, как следствие, искажающие показания электрода. Для удаления этих слоев используются различные вещества.
| Тип загрязняющей пленки | Как и чем чистить |
| Смешанные | Промойте водой, высушите и замочите в 5% растворе HCl на 15 минут. Промойте, высушите и замочите на 1 час в 3М растворе KCl, промойте в воде, откалибруйте |
| Неорганические | Промойте водой, высушите и замочите на 15 минут в 0,1М растворе EDT. Промойте, высушите и замочите на 1 час в 3М растворе KCl, промойте в воде, откалибруйте |
| Протеин | Промойте водой, высушите и замочите в 5% растворе HCl на 15 минут, также можно в 0,1 моль растворе HCl с 0,1% пепсина. Вымойте и высушите, замочите на 1 час в растворе 3M KCl, промойте в воде, откалибруйте |
| Масло | Промойте раствором моющего средства или этанолом. Вымойте, высушите, замочите на 1 час в растворе 3M KCl, промойте в воде, откалибруйте |
| Сульфид серебра | Замочить в 0,1М растворе тиомочевины Промыть, высушить и замочить на 1 час в 3М растворе KCl, промыть в воде, откалибровать |
| Твердый осадок | Замочите в перекиси водорода или гипохлорите натрия. Промойте, высушите, замочите на 1 час в 3М растворе KCl, промойте в воде, откалибруйте |
Никогда не вытирайте электрод чем-либо при переходе от жидкости к жидкости. Допускается только капать капли, оставшиеся на кончике стеклянной мембраны, не прикасаясь к ней. Калибровка электрода Каждый отдельный электрод имеет свои собственные характеристики, которые отличаются от идеального электрода. Это связано с производственными допусками, старением электрода во время хранения и использования, неправильным хранением и использованием. Отклонение pH-электрода от идеальных электродных характеристик компенсируется операцией калибровки. Суть процесса калибровки электрода заключается в применении поправочного коэффициента к формуле преобразования контроллера из единиц напряжения (мВ) в единицы pH для учета дрейфа электрода, вызванного вышеупомянутыми причинами. Одновременно определяется наклон графика, используя две точки калибровки (два калибровочных (буферных) раствора pH7 и pH4). Все автоматические станции дозирования химикатов поставляются в комплекте с буферными растворами как для pH-электрода, так и для Redox-электрода. В инструкции, поставляемой с каждой дозирующей станцией, указана периодичность калибровки электродов. У некоторых производителей этот срок составляет две недели, у других – шесть месяцев. Разумеется, эти рекомендации даются не производителем станции, а производителем электродов. Они, безусловно, знают об отклонении параметров измерения в зависимости от времени и условий эксплуатации их электродов. Правильность показаний электродов проверяется при каждом обслуживание плавательного бассейна и при необходимости их калибруют и заменяют, если они не работают.  Буферные растворы (калибровочные жидкости)
Буферные растворы (калибровочные жидкости) 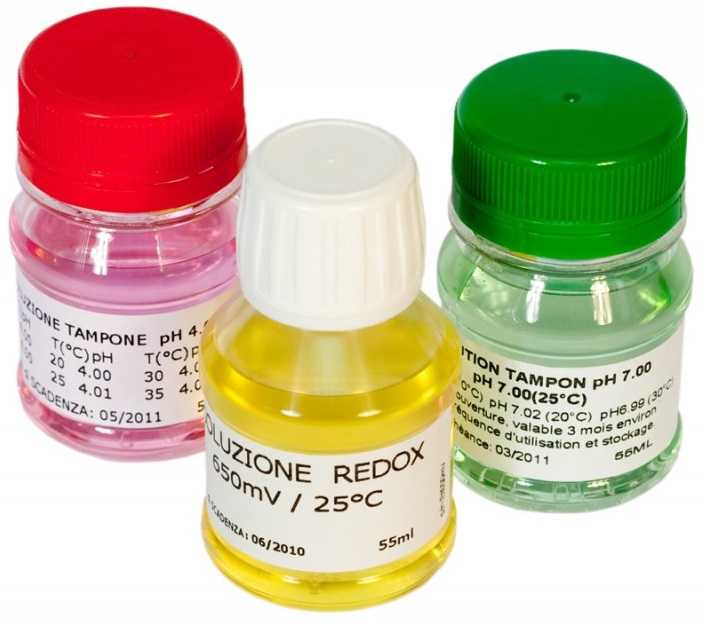 Буферные растворы поставляются вместе со станцией дозирования, но могут быть приобретены и отдельно. Они не имеют длительного срока службы и должны обновляться через регулярные промежутки времени. В идеале, обновляйте их одновременно с заменой электродов, каждый год. Не используйте растворы, простоявшие некоторое время с нераспечатанными пробками.
Буферные растворы поставляются вместе со станцией дозирования, но могут быть приобретены и отдельно. Они не имеют длительного срока службы и должны обновляться через регулярные промежутки времени. В идеале, обновляйте их одновременно с заменой электродов, каждый год. Не используйте растворы, простоявшие некоторое время с нераспечатанными пробками.
Чтобы избежать путаницы при калибровке электродов, растворы должны иметь цветовую маркировку, а бутылки должны быть помечены наклейками разного цвета и одинаковыми крышками. Это также указывает на отклонение pH буферного раствора при различных температурах. Лучше всего хранить растворы в темном, прохладном месте. Некоторые советуют хранить их в холодильнике. В этом случае перед использованием растворы следует подогреть до 25 градусов.
Влияние температуры Только температура влияет на наклон графика, остальные параметры влияют на смещение графика по осям. В следующих таблицах показано расхождение значений pH при различных температурах для измеренных водных и буферных растворов. Однако, поскольку при рабочих температурах в бассейне эти расхождения не столь велики, ими можно пренебречь. Однако в некоторых станциях дозирования температурные датчики используются в измерительных кюветах или отдельно, чтобы ввести температурный фактор в формулу для преобразования значения pH.
Изменение значения pH в зависимости от температуры
Влияние температуры на pH стандартных (буферных) растворов
В производстве в основном используются рН-метры рН-210, рН-215 и т.д., а также ионометры, предназначенные для определения активности моно- и двухвалентных анионов и катионов (значение рН) в водных растворах, такие как И-120, И-130, И-135 и др.
pH-метр
pH-метры – это приборы, предназначенные для определения значения pH и окислительно-восстановительного потенциала водных растворов, а также для использования в качестве высокоомных милливольтметров.
Приборы могут проводить измерения путем отбора проб с прикрепленными зондами или непосредственно в лабораторных условиях.
Эти приборы предназначены для использования в научно-исследовательских учреждениях, на промышленных предприятиях и в различных отраслях промышленности.
Основными используемыми приборами являются pH-метры pH-210, pH-215 и т.д., а также иономеры, предназначенные для определения активности одновалентных и двухвалентных анионов и катионов (значение pH) в водных растворах, такие как И-120, И-130, И-135 и др.
Принцип измерения значения pH
Для измерения значения pH используется потенциометрический метод, который основан на использовании электрического сигнала (потенциала) специального датчика, называемого измерительный электродв зависимости от состава анализируемого раствора. Измерительный электрод реагирует на ионы водорода, и его потенциал зависит от содержания этих ионов в растворе и следует уравнению Нернста:
E = E0 + R×T/F×ln an = E0 – 2,3×R×T/F×rH,
где R – универсальная газовая постоянная, равная 8,315 × 107 эрг/С×моль;
T – температура раствора, К;
F – 96000 кулон/г экв (число Фарадея);
an – активность ионов водорода в растворе;
pH – значение pH раствора;
E0 – потенциал стеклянного электрода относительно стандартного водородного электрода при an=1.
В настоящее время абсолютное значение потенциала измерить невозможно, но можно измерить потенциал относительно другого электрода, потенциал которого не зависит от состава раствора и условно равен нулю. Этот электрод называется электрод сравнения или вспомогательный электрод.
Поэтому измерения всегда проводятся с использованием двух электродов – измерительного и эталонного. Кроме того, в настоящее время доступны комбинированные электроды, которые содержат в одном корпусе измерительный и контрольный электроды.
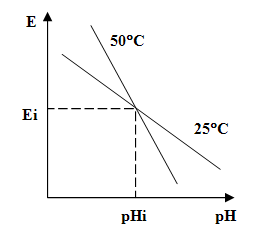
Обратите также внимание, что функция электрода зависит от температуры раствора. Эта зависимость показана на графике.
По мере повышения температуры наклон (крутизна) электродной характеристики увеличивается.
Концентрация анализируемых ионов, при которой электродный потенциал не зависит от температуры, называется изопотенциальная точка..
Значения концентрации раствора и электродного потенциала в этой точке называются координаты изопотенциальной точки.
Для стеклянных электродов координаты изопотенциальной точки стандартизированы, т.е. указаны производителем, но для других электродов обычно не указываются. Современные измерительные приборы позволяют автоматически учитывать температурные изменения характеристик электрода (термокомпенсация), для этого необходимо ввести в прибор координаты изопотенциальной точки и текущую температуру. Последний показатель может быть введен вручную или с помощью датчика температуры, подключенного к прибору.
При выборе электродов рекомендуется выбирать электрод, изопотенциальная точка которого лежит вблизи средней концентрации анализируемых растворов.
Рассмотрим измерительную систему со стеклянным измерительным электродом и вспомогательным электродом, схема которой показана на рисунке 1.
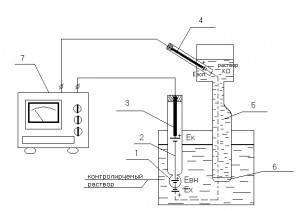
Рисунок 1: Схема измерения значения pH раствора.
1 – стеклянный шар полого электрода; 2 – стеклянный электрод; 3 – внутренний контактный электрод; 4 – вспомогательный электрод; 5 – электролитический ключ; 6 – пористая перегородка; 7 – милливольтметр.
При погружении электрода в раствор между поверхностью стеклянного электрода-шарика 1 и раствором происходит ионный обмен, в результате которого ионы лития в поверхностных слоях стекла замещаются ионами водорода и стеклянный электрод приобретает свойства водородного электрода.
Между поверхностью стекла и контролируемым раствором создается разность потенциалов Ex, величина которой зависит от активности водородных ионов в растворе и его температуры.
Для создания электрической цепи во время измерения используются контактные электроды: внутренний контактный электрод 3, который находится в контакте с раствором, заполняющим внутреннюю часть стеклянного электрода, и внешний контактный (вспомогательный) электрод 4, который находится в контакте с контролируемым раствором.
Для защиты от воздействия высокой температуры (при измерении рН растворов, температура которых выше температуры окружающего воздуха) вспомогательный электрод помещают вне контролируемого раствора, а соединение с ним осуществляют с помощью электролитического ключа 5 – трубки, заполненной раствором хлористого калия и заканчивающейся стекловолоконной пробкой 6.
Раствор хлористого калия непрерывно проникает через стекловолоконную пробку, что предотвращает попадание в электродную систему 4 посторонних ионов из контролируемого раствора, которые могут изменить значение электродного потенциала.
Электродвижущая сила электродной системы равна алгебраической сумме контактных потенциалов электродов Ek и Eusp, потенциала, возникающего на внутренней поверхности стеклянного электрода и определяемого значением pH внутреннего раствора Eun, и потенциала, возникающего на внешней поверхности стеклянного электрода Ek.
Значения Ek, Evsp и Yvn не зависят от состава испытуемого раствора и изменяются только с температурой
E = Ek + Evsp + Eur + Ex = E0 – 2,3×R×T/F×pH.
Общая электродвижущая сила электродной системы зависит от значения pH раствора.
Измеряя ЭДС электродной системы милливольтметром, шкала которого градуирована в единицах pH, определяют значение pH контролируемого раствора.
Принцип работы
Электродная решетка, которая является датчиком, имеет высокое внутреннее сопротивление, которое достигает 500-1000 МОм.
Для измерения ЭДС электродной системы используется компенсационная схема, позволяющая значительно снизить ток, потребляемый датчиком во время измерения.
Схема, объясняющая принцип работы pH-метра, показана на рисунке 2.
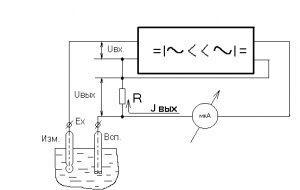
Рисунок 2: Принципиальная схема устройства.
ЭДС Ex электродной решетки сравнивается с падением напряжения на сопротивлении R, через которое в конечном усилительном каскаде протекает ток I out. Падение напряжения Uвх на сопротивлении R противоположно по знаку электродвижущей силе Ех, и на вход усилителя подается напряжение: Uвх=Ех-Uв=Ех-R×Iв.
Напряжение Uinx преобразуется преобразователем колебаний в переменное напряжение, которое затем многократно усиливается и снова преобразуется в постоянное напряжение с помощью фазового детектора. Это напряжение контролируется током I, протекающим через последний каскад усилителя. Если коэффициент усиления усилителя достаточно велик, напряжение U out мало отличается от напряжения ЭДС Ex, поэтому ток, протекающий через электроды во время измерения ЭДС, очень мал.
Ток I out, протекающий через резистор R, пропорционален ЭДС электродной системы и значению pH контролируемого раствора.
Электродная система
Основной особенностью электродной системы является зависимость ее ЭДС от значения pH и температуры раствора. В общем случае ЭДС может быть выражена уравнением:
E=Ei-[S20+a(t-20)] (рН-рНі),
где E – ЭДС в милливольтах;
t – температура электрода;
рН – значение рН раствора;
pNi – значение pH раствора, соответствующее изопотенциальной точке;
S20 – наклон характеристической кривой в изопотенциальной точке;
a – температурный коэффициент наклона.
Зависимость ЭДС электродной системы от pH и температуры может быть представлена следующим приближенным уравнением:
Стоит отметить, что значение pH пропорционально ЭДС, а само измерительное устройство действует как адаптированный вольтметр.
Как это работает?
Как известно, химики давно освоили технологию, позволяющую с максимальной точностью определять кислотность практически любого раствора. В первую очередь это касается качественных реакций и изменения цвета индикаторов, таких как фенолфталеин. Однако на практике это не всегда работает эффективно. Необходимо иметь как можно более точные данные о состоянии рассматриваемого носителя и постоянно контролировать его, чтобы иметь возможность своевременно вносить коррективы в производственные процессы. Именно с этой целью в те времена были разработаны приборы для анализа водородного показателя.
По своей сути и принципу работы любой pH-метр – это прибор, измеряющий значения разности потенциалов. Это относится к ЭДС (электродвижущей силе) в электрохимической системе, состоящей из 2 электродов и самой среды.
Стоит отметить, что значение pH пропорционально ЭДС, а сам измерительный прибор действует как адаптированный вольтметр.
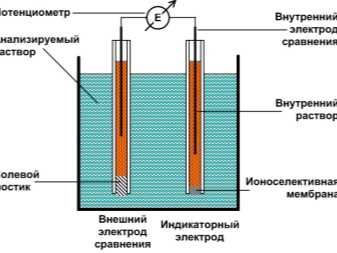

Разница в том, что его шкала показывает не вольты, а измеряемый уровень активности ионов водорода. Как правило, описанные примеры современных измерительных приборов имеют конструкцию, основными элементами которой являются два электрода, т.е. электрод выполнен из стекла и имеет высокий уровень сопротивления:
- Главный из них изготовлен из стекла и обладает высокой прочностью;
- дополнительный электрод из хлорида серебра.
Важным моментом является то, что основным и наиболее жестким требованием является внутреннее сопротивление электрода, выполняющего роль зонда. Хороший pH-метр должен иметь внутреннее сопротивление не менее 1011 Ом. Не секрет, что электродвижущая сила напрямую зависит от температуры. По этой причине в схему каждого устройства включена так называемая тепловая компенсация для анализа данных при температурах, отличных от стандартного значения +25 градусов Цельсия. Важно отметить, что для достижения максимальной точности измерений рекомендуется записывать результаты в этом температурном режиме.
Нередко можно встретить pH-метры для воды, почвы и других сред со встроенным термометром для контроля их состояния.
Если прибор или тест жидкости показывает отклонение pH в сторону кислой или щелочной среды, это можно компенсировать с помощью регуляторов pH, таких как pH-UP и pH-DOWN. Первые снижают уровень кислотности, вторые повышают его. Продукция выпускается в сухом и жидком виде.
Калибровка одноточечного рН-метра

Одноточечные устройства калибруются следующим образом. Используется фиксированный pH, равный 6,86. Поворотом винта, погружая измерительный прибор в раствор, показания pH-метра настраиваются на уровень pH калибруемого раствора.
Для измерения pH среды электрод прибора погружают в раствор и замыкают электрическую цепь, не внося никаких примесей в саму среду. Гальваническая цепь представлена электродом сравнения и хлорсеребряным электродом в исследуемом растворе. Разность потенциалов, возникающая в результате переноса электронов на электрод сравнения, вызывает эквивалентный перенос протонов в раствор изнутри электрода. При постоянной концентрации положительных ионов H внутри стеклянного электрода ЭДС отражает активность ионов водорода в растворе, или ph.
Как работает ph-метр
Ph-метры популярны во многих областях человеческой деятельности: водоподготовка, гидропоника, аквариумистика, сельское хозяйство, наука, микробиологические и лабораторные исследования, медицина, химическая, пищевая промышленность и другие.
Ph-метры используются для контроля питьевой воды, биологических жидкостей, лекарств, продуктов питания и многого другого.
Все, наверное, знают из уроков химии, что существуют кислые (ph меньше 7), основные (ph больше 7) и нейтральные среды (ph равен 7 – дистиллированная вода).
Эксперименты с фенолфталеином, лакмусом, различными метиловыми индикаторами и другими кислотно-основными индикаторами позволяют оценить pH, но это весьма приблизительно. Гораздо удобнее ориентироваться на цифровые значения, особенно если требуется большая точность. Поэтому популярность ph-метров вполне оправдана.
Как работает ph-метр
ph-метр (“pondus Hydrogenii”) фактически измеряет активность ионов водорода. Принцип работы ph-метра основан на разности потенциалов, возникающей в исследуемой среде между электродами прибора (электродвижущая сила). Именно поэтому прибор ассоциируется с милливольтметром. Поскольку рассчитанная ЭДС пропорциональна pH, шкала, соответственно, в ph. Это значение рассчитывается с помощью уравнения Нернста. Однако нам это не нужно, так как прибор создан с учетом всех функций.
pH-метр состоит из пары электродов и исследуемой среды. Один электрод является измерительным электродом, который реагирует на ионы водорода, а другой – вспомогательным (или электродом сравнения).
В современных приборах измерительный электрод изготавливается из стекла, поскольку его можно использовать в широком диапазоне ph. Он изготовлен из боросиликатного стекла, которое устойчиво к окислителям, но при этом достаточно тонкое и электропроводное. Индикаторный электрод представляет собой трубку с тонкостенным шариком на конце, заполненную суспензией хлорида серебра в растворе соляной кислоты. В эту среду вводится серебряная проволока, образуя хлорсеребряный электрод. Положительные ионы водорода вытесняются в стекло.
Электрод сравнения часто содержит ртутно-каломельную пасту в насыщенном растворе хлорида калия. Корпус электрода непроницаем для положительных ионов водорода, а хлорид калия действует как проводник между раствором и ртутно-каломельным полуэлементом.
Для измерения pH среды электрод погружают в раствор и замыкают электрическую цепь без попадания в среду каких-либо примесей. Гальваническая цепь представлена электродом сравнения и хлорсеребряным электродом в исследуемом растворе. Из-за разности потенциалов, возникающей в результате переноса электронов на электрод сравнения, происходит эквивалентный перенос протонов в раствор изнутри электрода. При постоянной концентрации положительных ионов H внутри стеклянного электрода ЭДС отражает активность ионов водорода в растворе, или ph.
На что следует обращать внимание при работе с pH-метром?
Значение ЭДС зависит от температуры, поэтому измерительная функция прибора зависит от температуры раствора. Для достижения максимальной точности рекомендуется проводить измерения при температуре 25 °C. Часто современные pH-метры оснащены встроенным термометром для определения температуры раствора.
Функция автоматической температурной компенсации (ATC) позволяет автоматически учитывать изменения температуры. Для стеклянных электродов координаты изопотенциальной точки нормируются производителем.
При выборе pH-метра следует обратить внимание на наличие функции температурной компенсации для упрощения эксплуатации прибора.
Таким образом, мы узнали, “как работает pH-метр”: с помощью пары электродов. Современные приборы объединяют оба электрода в одном корпусе, а также осуществляют температурную компенсацию. Технологии и исследования также позволяют объединить в одном корпусе другие функции для смежных измерительных задач: ORP, RTD, EC.
В зависимости от условий применения можно выбрать карманные pH-метры, лабораторные pH-метры и профессиональные pH-метры с различными дополнительными опциями интерфейса, такими как память результатов, запись показаний, подключение к компьютеру и т.д.
Стоит отметить, что ведущую роль сохраняют портативные рН-метры благодаря их функциональности, удобству и низкой стоимости.
Существуют портативные pH-метры для измерения pH. pH-метр модели 2696 – это ручной прибор с автоматической температурной компенсацией от 0 до 40°C. Он предназначен для измерения pH и температуры водных растворов, мясных, молочных, рыбных и других пищевых продуктов. pH-метр также можно использовать в качестве милливольтметра. pH-метр основан на потенциометрическом методе измерения pH. Потенциал от подключенного рН-электрода подается на измерительный преобразователь, где он усиливается, фильтруется, преобразуется в цифровой код, обрабатывается и выводится в виде значения рН на цифровой дисплей. Датчик температуры, сопротивление которого изменяется в зависимости от температуры измеряемой среды, используется для измерения температуры и автоматической компенсации температурных изменений в показаниях прибора в зависимости от температуры анализируемой среды. Преобразователь измеряет сопротивление, рассчитывает температуру среды, выдает ее на цифровой дисплей и учитывает значение pH при измерении.
Конструкция и принципы работы приборов для измерения рН
Принцип действия приборов для измерения pH основан на измерении электродвижущей силы элемента, состоящего из электрода сравнения с известным потенциалом и индикаторного электрода, потенциал которого является результатом концентрации ионов водорода в исследуемом растворе.
Для измерения pH используются следующие приборы: pH-метр 340, иономер EV-74, иономер-130, портативные pH-метры, цифровые pH-метры и другие. Все pH-измерительные приборы состоят из двух основных элементов – измерительного прибора, шкала которого откалибрована в единицах pH, с устройством для автоматической температурной компенсации и устройством для настройки и калибровки прибора по буферным растворам, и штатива с закрепленными на нем электродами. Современные портативные цифровые pH-метры используют один специальный ионоселективный электрод вместо электродной системы.
Прибор подключается к сети и нагревается в течение не менее 30 минут. Перед тестированием прибор проверяется с использованием стандартных буферных растворов pH 3,57; 4,00; 5,00; 6,88; 9,22 при 20 °C в соответствии с инструкциями, прилагаемыми к приборам. После проведения испытаний электроды тщательно промываются дистиллированной водой.
Затем концы электродов погружаются в заранее приготовленный тестовый раствор, и как только прибор достигает устойчивого состояния, считывается значение pH на шкале.
Если прибор имеет несколько диапазонов измерения, показания в широком диапазоне рН (от 1,0 до 14,0) отсчитываются по нижней шкале прибора, а показания в узких диапазонах рН (1-2; 2-5; 5-8; 8-11; 11-14) отсчитываются по верхней шкале путем переключения переключателя “диапазон” из положения 15rN в положение ZrN (только для показаний), а переключатель “предел измерения” – в нужный диапазон. После каждого измерения электроды тщательно промываются дистиллированной водой.
Имеются ручные приборы для измерения pH. pH-метр модели 2696 – это ручной прибор с автоматической температурной компенсацией от 0 до 40°C. Он предназначен для измерения pH и температуры водных растворов, мясных, молочных, рыбных и других пищевых продуктов. pH-метр также можно использовать в качестве милливольтметра. pH-метр основан на потенциометрическом методе измерения pH. Потенциал от подключенного pH-электрода подается на измерительный преобразователь, где он усиливается, фильтруется, преобразуется в цифровой код, обрабатывается и выводится в виде значения pH на цифровой дисплей. Датчик температуры используется для измерения температуры и автоматической компенсации температурных изменений измеряемой среды, сопротивление которого изменяется в зависимости от температуры среды. Преобразователь измеряет сопротивление, рассчитывает температуру среды, отображает ее в цифровом виде и учитывает при измерении значения pH.
Внешний вид pH-метра показан на рис. 5.2. pH-метр состоит из измерительного преобразователя (1), комбинированного pH-электрода (2) и датчика температуры (3).
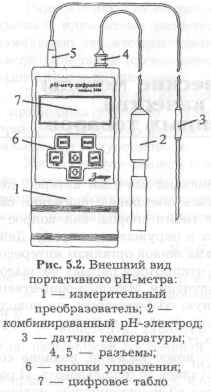
Измерительный преобразователь (1) выполнен в пластиковом корпусе, внутри которого находится двухсторонняя плата с электронными компонентами. На передней панели расположены кнопки для включения и выключения питания, кнопки для выбора и установки режима работы, кнопки для настройки устройства в соответствии с
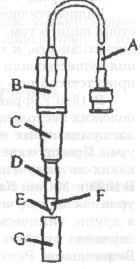
стандартные настройки буфера. В верхней части панели расположен цифровой дисплей (7) для отображения измеренных значений. На верхней панели измерительного преобразователя расположены разъемы (4 и 5) для подключения pH-электрода и датчика температуры соответственно. На задней панели измерительного преобразователя расположен батарейный отсек и подставка для стационарной установки pH-метра на столе. Внешний вид pH-электрода показан на рис. 5.3.
Читайте далее:- Что такое электродный потенциал; Школа для инженеров-электриков: электротехника и электроника.
- Топливные элементы/.
- Измерительный инструмент – это инструмент для измерения. Что такое измерительный инструмент?.
- Значение слова 'потенциал' в 9 словарях.
- Тонкости электропроводности.
- Строение атома водорода (H), схема и примеры.
- Электролит (химия) – это. Что такое электролит (химия)?.