Обычная практика, особенно среди водителей транспорта, – называть любое оборудование аккумулятором, независимо от количества его составных частей – банок. Однако это не совсем верно. Состоящий из нескольких последовательно соединенных банков, он представляет собой батарею, которая получила аббревиатуру “аккумулятор”. Его внутренняя структура показана на рисунке.
Структура и функции аккумулятора
 В широком техническом смысле термин “аккумулятор” относится к устройству, которое позволяет хранить определенный вид энергии при определенных условиях эксплуатации и распределять ее для использования человеком при других условиях.
В широком техническом смысле термин “аккумулятор” относится к устройству, которое позволяет хранить определенный вид энергии при определенных условиях эксплуатации и распределять ее для использования человеком при других условиях.
Они используются там, где необходимо накопить энергию на определенный период времени, а затем использовать ее для крупных трудоемких процессов. Например, гидравлические аккумуляторы, используемые в шлюзах, позволяют поднимать суда на новый уровень в русле реки.
Электрические аккумуляторы работают с электричеством одинаково: они сначала накапливают электрическую энергию от внешнего источника заряда, а затем отдают ее подключенным потребителям для выполнения работы. По своей природе они являются химическими источниками энергии, способными многократно и периодически разряжаться и перезаряжаться.
Во время работы между компонентами электродных пластин и наполняющим веществом – электролитом – происходят химические реакции.
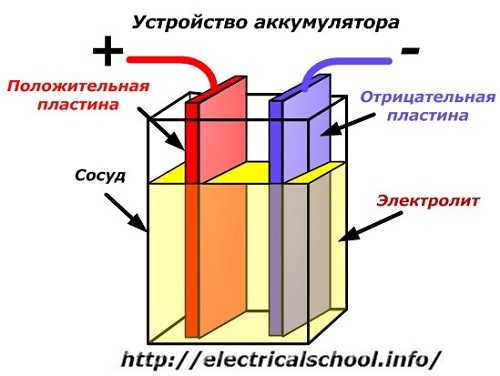
Принципиальная схема батареи может быть представлена упрощенным рисунком, на котором две пластины из разных металлов помещены в корпус емкости, а клеммы обеспечивают электрический контакт. Электролит заливается между пластинами.
Работа аккумулятора во время разряда
Когда заряд, например, лампочка, подключается к электродам, образуется замкнутая электрическая цепь, по которой протекает разрядный ток. Он образуется в результате движения электронов в металлических деталях и анионов с катионами в электролите.
Этот процесс в обычном виде показан на схеме с конструкцией никель-кадмиевого электрода.
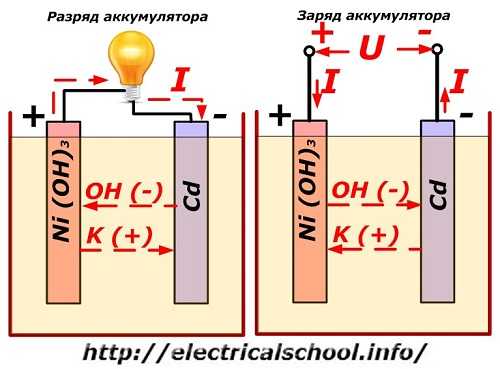
Здесь в качестве материала положительного электрода используются оксиды никеля с добавлением графита, что повышает электропроводность. Металл отрицательного электрода – губчатый кадмий.
Во время разряда молекулы активного кислорода из оксидов никеля попадают в электролит и перемещаются к отрицательным пластинам, где окисляют кадмий.
Работа аккумулятора во время зарядки
При отключенной нагрузке постоянное (в некоторых ситуациях пульсирующее) напряжение, превышающее напряжение заряжаемой батареи, прикладывается к клеммам пластин одинаковой полярности, когда плюсовая и минусовая клеммы источника и приемника пересекаются.
Зарядное устройство всегда имеет большую емкость, которая “подавляет” оставшуюся энергию в аккумуляторе и производит электрический ток в направлении, противоположном направлению разряда. В результате изменяются внутренние химические процессы между электродами и электролитом. Например, в банке с никель-кадмиевой пластиной положительный электрод обогащается кислородом, а отрицательный электрод восстанавливается до чистого кадмия.
Когда аккумулятор разряжается и заряжается, химический состав материала пластин (электрода) меняется, но электролит остается неизменным.
Как подключаются батареи
Величина разрядного тока, которую может выдержать одна коробка, зависит от многих факторов, но в первую очередь от конструкции, используемых материалов и размеров. Чем больше площадь поверхности электродной пластины, тем больший ток может быть пропущен через нее.
Этот принцип используется для параллельного соединения элементов батареи одного типа, когда для нагрузки требуется больший ток. Но для зарядки такой конструкции потребуется увеличить мощность источника. Этот метод редко используется для сборных конструкций, поскольку в настоящее время гораздо проще купить необходимую батарею сразу. Однако его используют производители кислотных батарей, объединяя различные пластины в единый блок.
В зависимости от используемых материалов, между двумя электродами обычных бытовых батарей может быть получено напряжение 1,2/1,5 или 2,0 вольт. (В реальности этот диапазон гораздо шире.) Для многих электрических устройств этого явно недостаточно. Поэтому батареи одного типа соединяются последовательно, и часто это делается в одном корпусе.
Примером такой конструкции является широко используемая автомобильная разработка на основе серной кислоты и свинцовых электродных пластин.
Принято, особенно среди водителей транспорта, называть любое устройство, независимо от количества составляющих его элементов – банок – аккумулятором. Однако это не совсем верно. Состоящий из нескольких последовательно соединенных банков, он представляет собой аккумулятор, получивший сокращенное название “батарея”. Его внутренняя структура показана на рисунке.
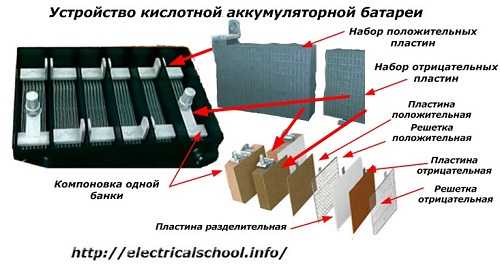
Каждая коробка состоит из двух блоков с набором пластин для положительного и отрицательного электрода. Блоки устанавливаются друг на друга без металлического контакта, что обеспечивает надежную гальваническую связь через электролит.
Контактные пластины имеют дополнительную сетку и отделены друг от друга разделительной пластиной.
Объединение пластин в блоки увеличивает их рабочую поверхность, снижает общее удельное сопротивление всей конструкции и позволяет увеличить грузоподъемность подключенного груза.
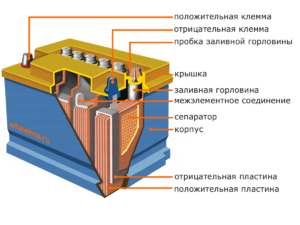
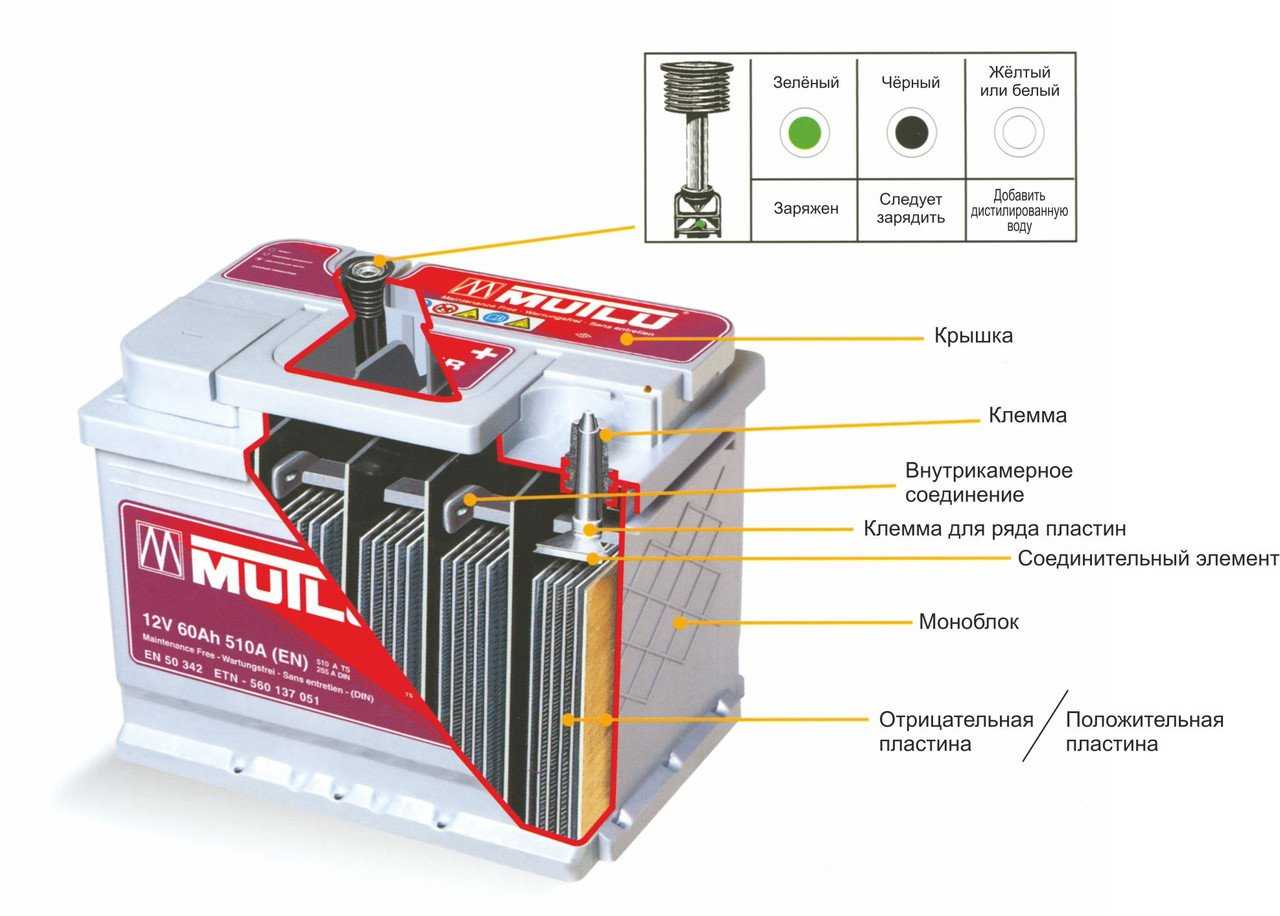
Внешняя часть корпуса такой батареи имеет компоненты, показанные на рисунке ниже.
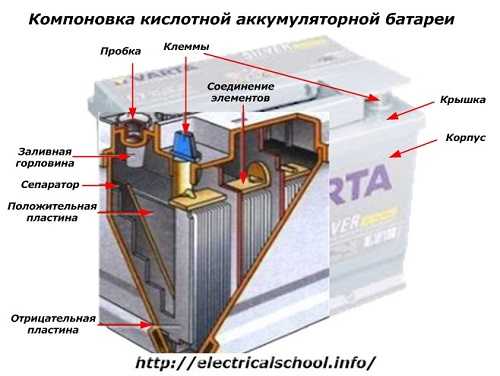
На нем видно, что твердый пластиковый корпус закрыт крышкой и имеет две клеммы (обычно конусообразные) сверху для подключения к электрическим цепям автомобиля. Эти клеммы отмечены знаками полярности ‘+’ и ‘-‘. Положительная клемма обычно немного больше по диаметру, чем отрицательная, чтобы предотвратить ошибки при подключении.
Обслуживаемые батареи имеют заливное отверстие в верхней части каждой батареи для проверки уровня электролита или долива дистиллированной воды во время работы. В нее ввинчивается пробка для защиты внутренней части банки от мусора и предотвращения вытекания электролита при наклоне батареи.
Поскольку при высоком заряде может произойти газообразование электролита (возможный процесс при интенсивном вождении), в пробках сделаны отверстия, чтобы предотвратить повышение давления внутри банки. Через них будут выходить кислород и водород, а также пары электролита. Избегайте ситуаций с чрезмерным зарядным током.
На этом же рисунке показано соединение ячеек между банками и расположение электродных пластин.
Стартерные батареи (свинцово-кислотные) работают по принципу двойной сульфатации. Во время разряда/заряда в них происходит электрохимический процесс, сопровождающийся изменением химического состава активной массы электродов и выделением/поглощением воды в электролите (серной кислоте).
Это объясняет увеличение удельного веса электролита во время зарядки и его уменьшение во время разрядки. Другими словами, плотность – это мера электрического состояния батареи. Плотность измеряется с помощью специального прибора – автомобильного ареометра.
Дистиллированная вода, содержащаяся в электролите кислотных батарей, при температуре замерзания превращается в твердый лед. Поэтому необходимо принять специальные меры для предотвращения замерзания аккумуляторов автомобиля в холодное время года.
Какие типы батарей существуют
Современное производство для различных целей выпускает более трех десятков изделий с различными составами электродов и электролитов. Двенадцать известных моделей основаны только на литии.
Величина, характеризующая параметр тока, протекающего в стартере транспортного средства при запуске приводного устройства, обычно называется пусковым током. Пусковой ток или ток стартера возникает при повороте ключа зажигания и запуске двигателя стартера. Единицей измерения является ампер. Ток холодного пуска – это показатель того, как поведет себя аккумулятор в холодную погоду и сможет ли он запустить двигатель при отрицательных температурах. На это указывает количество тока, которое батарея способна отдать в первые 30 секунд при температуре -18°C. Высокие пусковые токи повышают вероятность запуска автомобиля при отрицательных температурах.
Чтобы понять, как работает батарея, необходимо узнать о ее структуре и о том, что находится внутри нее, что заставляет ее работать. Основным принципом работы аккумулятора является разность потенциалов при погружении двух пластин в электролит. 12-вольтовая батарея объединяет шесть аккумуляторов, каждый из которых вырабатывает 2 вольта. Все они соединены общим корпусом, образующим единое целое.
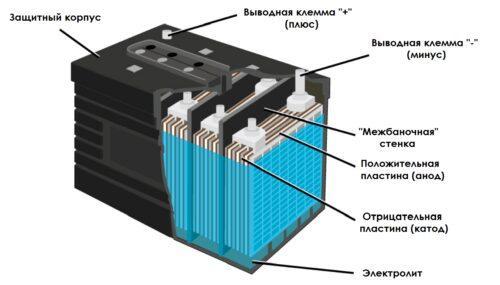
Батарея в поперечном сечении
Когда эта конструкция работает, пластины выделяют сульфат свинца при контакте с серной кислотой, что создает электрический ток. Вода также высвобождается, поэтому концентрация электролита становится менее плотной. При зарядке аккумулятора процесс обратный, свинец повторно металлизируется, а электролит становится более концентрированным. Принцип работы батареи основан на методе двойной сульфатации, который полностью восстанавливает первоначальные свойства батареи. Срок службы батареи зависит от качества материалов, из которых она изготовлена.
Макет

Строительная схема
Батарея – это устройство, которое при подключении к источнику постоянного тока накапливает энергию в химической форме, а затем высвобождает ее, преобразуя в электрическую энергию. Он пригоден для повторного использования благодаря возможности переработки и обратимости химических реакций. Разряженный – заряженный. Аккумуляторные батареи используются в качестве автономных и резервных источников энергии для электрооборудования и различных приборов.
Принцип работы аккумулятора
Принцип работы аккумуляторной батареи основан на создании разности потенциалов между двумя электродами, погруженными в электролит. Когда нагрузка (электроприбор) подключается к клеммам аккумулятора, электролит и активные электроды вступают в реакцию. Это вызывает движение электронов, что, по сути, является электрическим током.
Когда аккумулятор разряжен (нагрузка подключена), губчатый свинцовый анод высвобождает положительные ионы двухвалентного свинца в электролит. Избыточные электроны проходят через внешний замкнутый контур к катоду, где четырехвалентные ионы свинца восстанавливаются до двухвалентных ионов свинца.
Когда они соединяются с отрицательными ионами серного остатка электролита, на обоих электродах образуется сульфат свинца.
Ионы кислорода из катодного диоксида свинца и ионы водорода из электролита объединяются, образуя молекулы воды. Поэтому плотность электролита уменьшается.
Как работает батарея из 3 турионов
Во время зарядки происходит обратная реакция. При подаче внешнего напряжения двухвалентные ионы свинца на положительном электроде отдают по два электрона и окисляются до четвертичных ионов. Эти электроны движутся к аноду и нейтрализуют двухвалентные ионы свинца, уменьшая губчатый свинец. На катоде в результате косвенных реакций снова образуется диоксид свинца. Химические реакции, происходящие в одном элементе, создают напряжение 2 В, поэтому на клеммах 6-элементной батареи образуется напряжение 12 В.
Отдельные аккумуляторные ячейки вырабатывают небольшие напряжения и токи. Например, наиболее распространенное значение напряжения составляет от 1 до 2 вольт. Эти значения явно недостаточны для работы большинства устройств. Для того чтобы увеличить получаемое напряжение или силу тока, необходимо организовать комбинацию батарей в аккумулятор. Необходимо разработать описание этих методов.
Цикл зарядки аккумулятора
Чтобы начать зарядку, необходимо отключить нагрузку от клемм аккумулятора. На свободные клеммы аккумулятора должен быть подан постоянный ток с напряжением, превышающим выходное напряжение зарядного устройства.
Во время зарядки необходимо соблюдать полярность, т.е. положительные и отрицательные клеммы аккумулятора и зарядного устройства должны быть одинаковыми. Обратите внимание, что зарядное устройство следует выбирать с большей емкостью, чем сам аккумулятор, чтобы преодолеть сопротивление оставшейся в аккумуляторе энергии и произвести электрический ток в направлении, противоположном току разряда. В результате обратимые химические реакции, протекающие в батарее, изменят свое направление.
В качестве примера для рассмотрения можно также использовать никель-кадмиевый аккумулятор. Гидроксиды кадмия и никеля, образовавшиеся во время цикла разряда, вступают в реакцию. Продуктами этой реакции будут гидроксид оксида никеля, вода и восстановленный кадмий.
Из вышесказанного следует, что во время цикла разряда меняется только химический состав электродов. Электролит только создает среду, необходимую для протекания реакции. Со временем он может испариться, что не лучшим образом сказывается на сроке службы батареи. Описанный выше принцип работы справедлив для любого типа батарей, различается лишь химический состав электродов и электролита.
Такие батареи называются свинцово-кислотными, и это название описывает принцип работы этих устройств.
Параметры и характеристики батареи
Параметры и характеристики батарей зашифрованы в их обозначениях, и сейчас мы рассмотрим, что они означают.
Мы рассмотрим пример наиболее распространенной батареи 6СТ-55.

Таким образом, в названии батареи число 6 означает, что батарея состоит из 6 элементов.
- ST – указывает на то, что батарея является стартерной.
- 55 – указывает емкость батареи, которая составляет 55 Ампер*час.
Чтобы понять, какой аккумулятор вам нужен, необходимо знать две вещи:
- Тип двигателя;
- Рабочий объем двигателя вашего автомобиля;
Ниже мы рассмотрим, какие двигатели подходят для тех или иных батарей. Это таблица для бензиновых двигателей:
- Двигатели объемом до 1,6 л. Для этих двигателей подходят аккумуляторы 6ST-45;
- Двигатели объемом от 1,6 до 2,5 литров. Для них подходит модель 6СТ-55;
- Двигатели объемом от 2,5 до 3 литров. 6ST-60 подходит для этих двигателей;
- Двигатели с рабочим объемом от 3 до 3,5 литров. Для 6ST-75 подходят двигатели с рабочим объемом от 3 до 3,5 литров;
- Двигатели объемом более 3,5 л. Для этих двигателей подходит масло 6ST-90.
Для дизельных двигателей параметры немного отличаются:
- Двигатели с рабочим объемом до 1,5 л. 6ST-55 подходит для этих двигателей;
- Двигатели с рабочим объемом от 1,5 до 2,0 л. 6ST-60 подходит для этих двигателей;
- Двигатели объемом от 2 до 2,7 л. 6ST-75 подходит для этих двигателей;
- Двигатели с рабочим объемом от 2,7 до 3,5 литров. Двигатели с рабочим объемом от 2,7 до 3,5 литров. 6ST-90 подходит для этих двигателей;
- Двигатели с рабочим объемом от 3,5 до 6,5 литров. Двигатели с рабочим объемом от 3,5 до 6,5 литров. 6ST-132 подходит для них;
- Двигатели с рабочим объемом более 6,5 л. Для них подходит 6ST-192 или больше.
Как видите, из-за разного принципа работы дизельных и бензиновых двигателей для них используются аккумуляторы разной емкости.
Для дизельных двигателей требуется батарея большей емкости.
Сепараторы. Сепараторы устанавливаются между электродами и служат диэлектриками, которые надежно защищают элементы батареи от короткого замыкания. Эти элементы также изготовлены из кислотостойкого полимера, который не будет поврежден агрессивной средой в течение всего срока службы батареи.
Особенности конструкции
Батарейные блоки могут значительно отличаться друг от друга. Особенности конструкции аккумулятора включают:
- Размер батареи.
- Состав металлического сплава, из которого изготовлены пластины.
- Тип электролита.
- Расположение электрических клемм на корпусе.
Емкость батареи зависит от размера пластин и количества электролита в каждой банке, поэтому изделия, устанавливаемые на стартеры дизельных грузовиков, могут быть в несколько раз больше по весу и объему, чем батареи легковых автомобилей.
Тип свинцового сплава определяет внутреннее электрическое сопротивление батареи и устойчивость элемента к агрессивным средам. Состав металла также влияет на интенсивность испарения влаги, поэтому в необслуживаемых моделях пластины изготавливаются из свинца, легированного кальцием.
Тип электролита, используемого в батарее, также влияет на многие параметры батареи. Жидкий раствор замерзает при низких температурах, а при кипячении приводит к испарению воды, поэтому замена его на гель может значительно продлить срок службы продукта. Гелевые батареи гораздо лучше выдерживают глубокие разряды, поэтому их можно использовать не только в качестве стартерных устройств, но и для питания электроустановок.
Батареи также могут отличаться расположением клемм на корпусе. Это следует учитывать при выборе новой батареи, иначе придется удлинять плюсовой провод от автомобиля к источнику питания.
Читайте далее:- Электролит (химия) – это. Что такое электролит (химия)?.
- Гальванические элементы – устройство, принцип действия, виды и основные характеристики; Сайт для электриков – статьи, советы, примеры, схемы.
- Что такое электродный потенциал; Школа для инженеров-электриков: электротехника и электроника.
- Шаговые двигатели: свойства и практические схемы управления. Часть 2.
- Как правильно заряжать кислотный аккумулятор.
- Как работает pH-электрод.
- Зарядка никель-кадмиевых батарей: действия, уровень разряда.