Протон – положительно заряженная частица
масса протона равна единице, заряд протона равен единице
Нахождение количества протонов
Нахождение числа нейтронов, протонов и электронов в атоме .
Атом состоит из ядра и электронов, вращающихся вокруг ядра.
Ядро состоит из протонов и нейтронов.
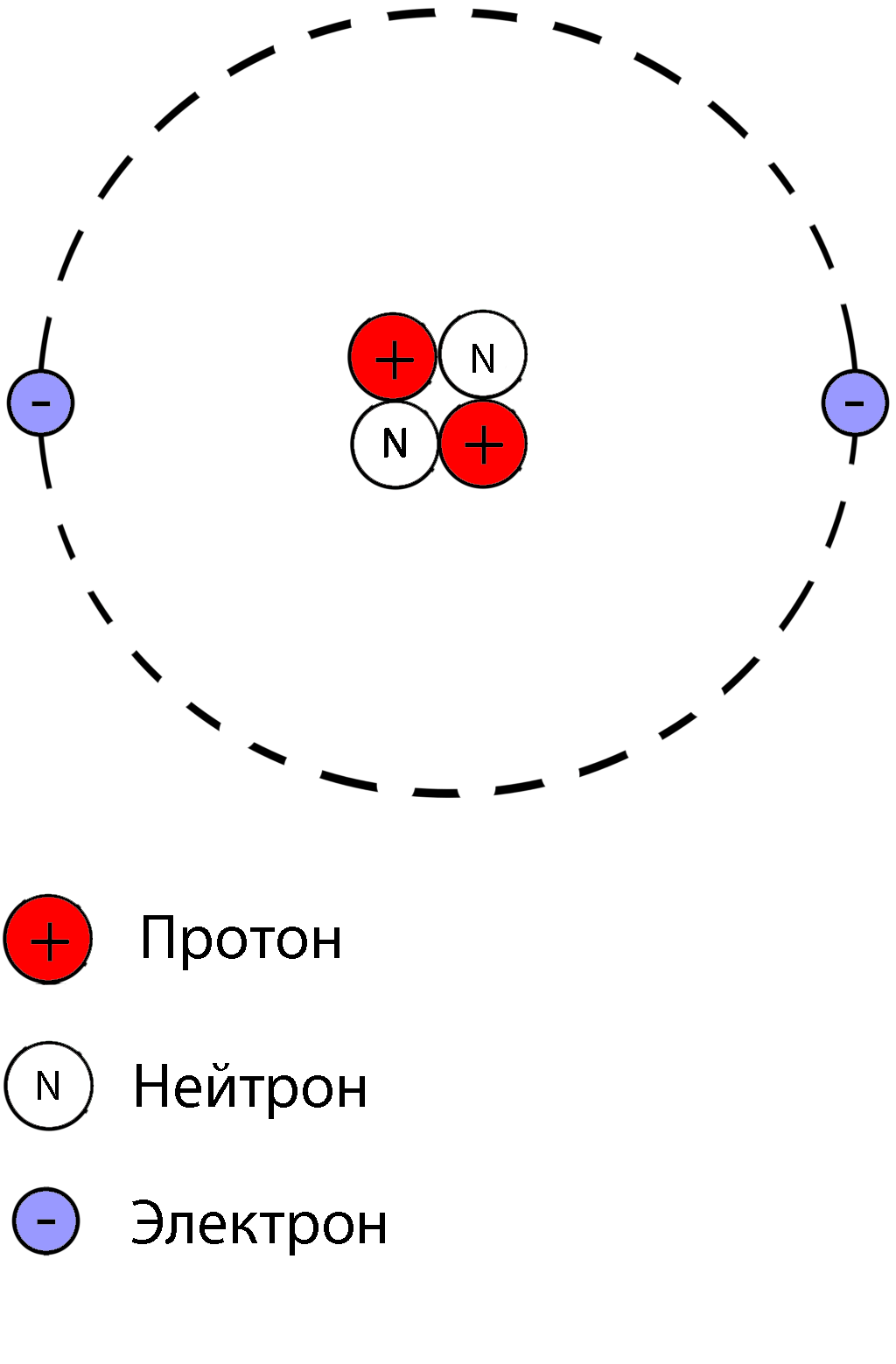
Протон – это положительно заряженная частица
масса протона равна единице, заряд протона равен единице
Нейтрон – нейтральная частица
Нейтрон – нейтральная частица с массой, равной единице, заряд нейтрона равен нулю
Электронно-нейтральная частица
электрон имеет заряд, равный -1, и массу, равную нулю
Порядковый номер элемента в таблице Менделеева указывает на количество электронов в атоме
Число протонов в атоме равно числу электронов, так как атом электрически нейтрален
Масса атома – это сумма числа протонов и числа нейтронов, масса электрона не учитывается.
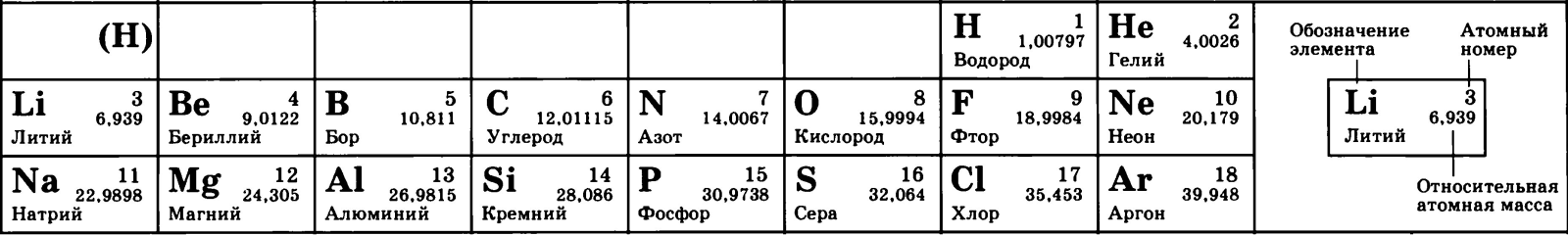
Рассмотрите фрагмент периодической таблицы и найдите количество протонов, нейтронов и электронов в атоме водорода
Затем давайте нарисуем модель атома водорода
Порядковый номер атома водорода равен единице, поэтому он имеет
1 электрон
1 протон
Чтобы найти количество нейтронов, нужно вычесть количество протонов из их массы.
Масса атома водорода равна единице
В атоме водорода нет нейтронов
Модель атома водорода:
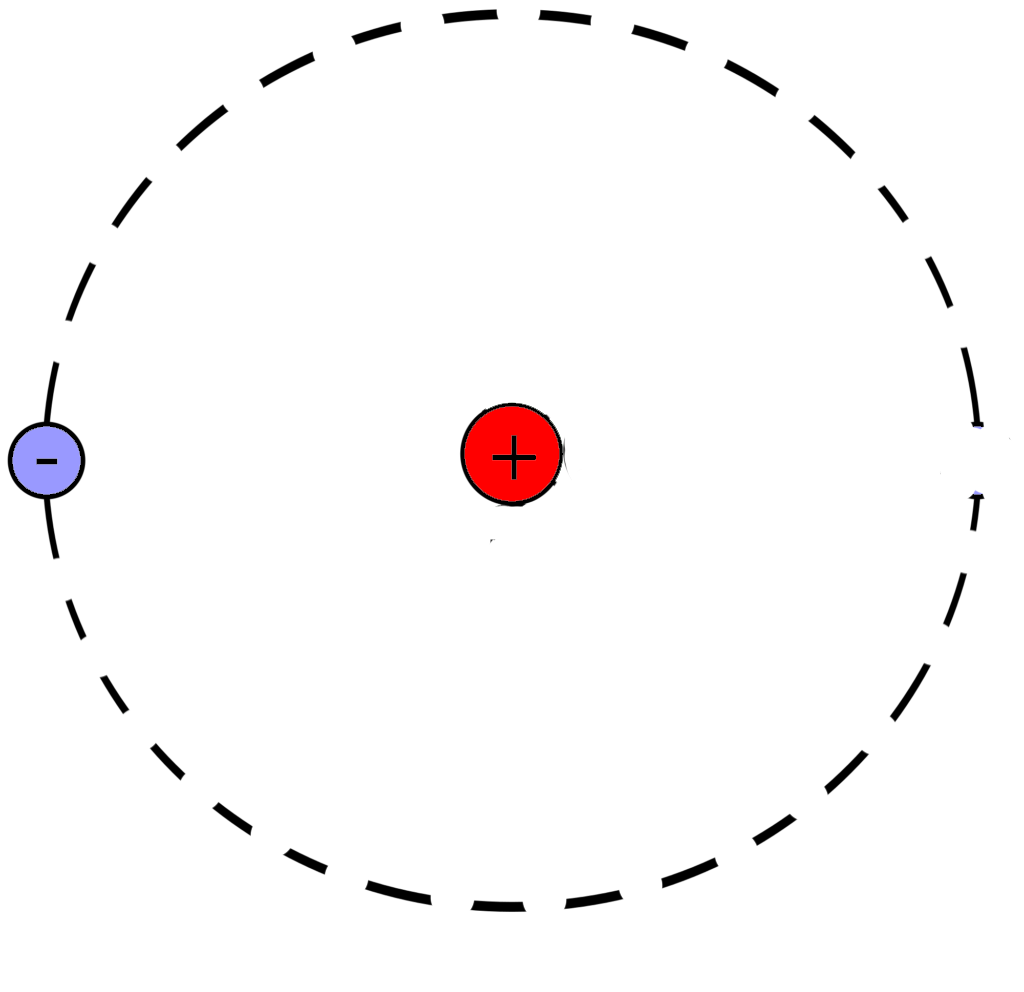

Рассмотрите участок периодической таблицы и найдите количество протонов, нейтронов и электронов в атоме гелия
Далее нарисуйте модель атома гелия
Порядковый номер атома гелия равен 2, поэтому атом имеет
2 электрона
2 протона
Чтобы найти количество нейтронов, вычтите количество протонов из массы
Масса атома гелия равна 4
В атоме гелия 2 нейтрона
Модель атома гелия:
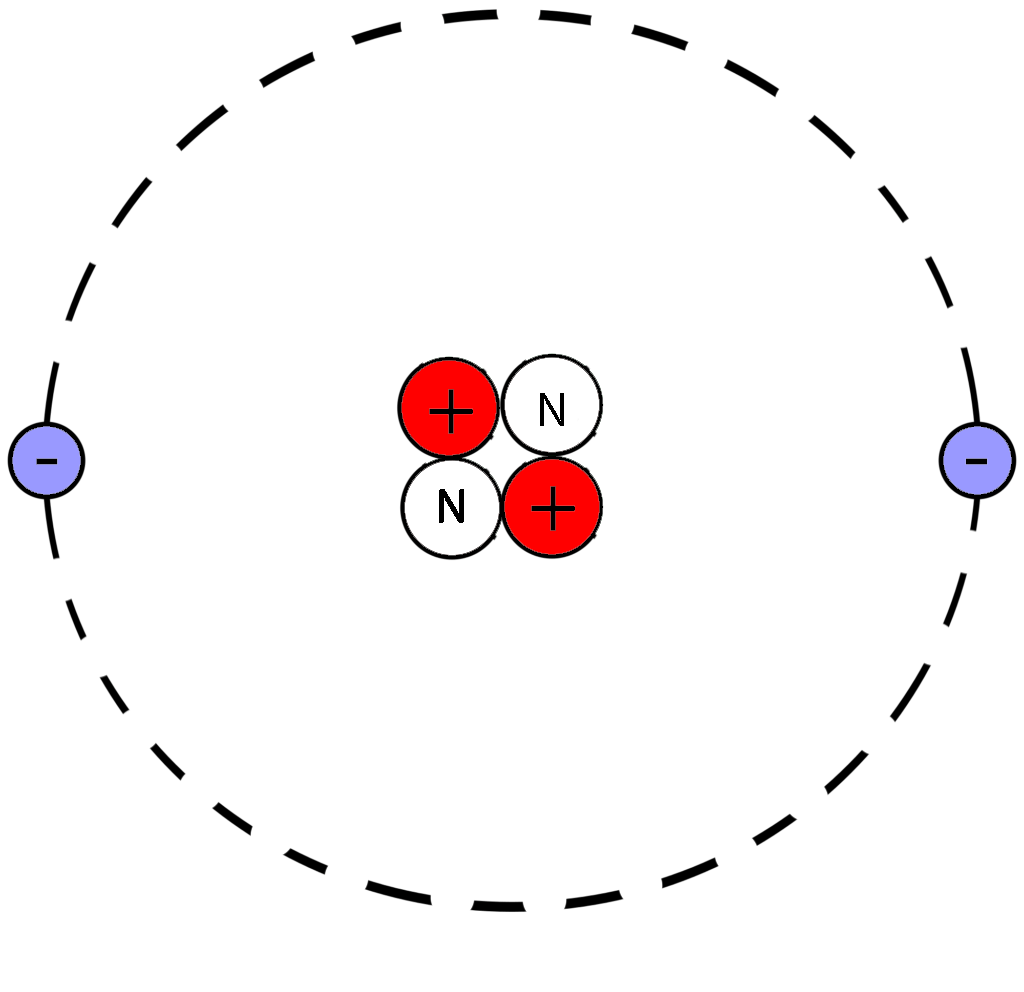

Используя выдержку из таблицы Менделеева, найдите число протонов, нейтронов и электронов в атоме лития.
Округлите массу атома до 7.
См.
Число протонов в атоме всегда равно его порядковому номеру
Число нейтронов равно разности массы и числа протонов, т.е. масса – число протонов.
Количество электронов равно количеству протонов.
Скорее всего, период можно использовать для определения количества атомов, протонов, нейтронов, электронов и т.д.
подсказка. Что можно узнать из числа периода, как найти число протонов нейтронов и электронов?
См.
Число протонов в атоме всегда равно его периодическому номеру
Число нейтронов равно разности массы и числа протонов, т.е. масса – число протонов.
Количество электронов равно количеству протонов.
Скорее всего, по номеру периода можно определить количество атомов, протонов, нейтронов, электронов и т.д. и т.п.
Номер периода может быть использован для определения количества электронных уровней.
Зная атомную массу и номер периода элемента, можно определить количество нейтронов, протонов и электронов.
Атомная масса = протоны + нейтроны.
Атомная масса = количество нейтронов
Количество ядер = заряд ядра (количество протонов)
Количество протонов = количеству электронов.
Необходимо знать порядковый номер элемента N и его округленную атомную массу A
Количество протонов = N = количество электронов
Количество нейтронов = A-N
Я не помню номер периода. Числа протонов (и электронов) – это номера элементов в таблице. Число нейтронов = атомная масса – число.
Давайте рассчитаем количество нейтронов в атоме на примере кислорода 16 O:
Количество протонов нейтронов электронов в атоме элемента (Таблица)
Количество протонов, нейтронов и электронов в атоме химического элемента (изотопа) можно определить, зная порядковый номер элемента в периодической таблице Менделеева и его атомную массу:
— Количество протонов = количество электронов = серийный номер элемента
— Количество нейтронов = атомный вес – количество протонов
Давайте рассчитаем количество нейтронов в атоме на примере кислорода 16 O:
16 – 8 = 8 (в кислороде 8 нейтронов)
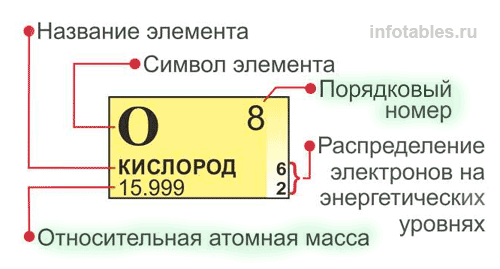
Таблица количества протонов нейтронов электронов в атоме химического элемента
В справочной таблице перечислены элементы (изотопы) и их число протонов, нейтронов и электронов, а также атомный вес изотопа.
| Элемент, изотоп | Количество протонов (= электронов) | Количество нейтронов | Атомный вес изотопа |
| 1 H | 1 | 0 | 1,0078 |
| 2 H | 1 | 1 | 2,0141 |
| 3 Он | 2 | 1 | 3,0160 |
| 4 Он | 2 | 2 | 4,0026 |
| 6 Li | 3 | 3 | 6,0151 |
| 7 Li | 3 | 4 | 7,0160 |
| 9 Be | 4 | 5 | 9,0122 |
| 10 B | 5 | 5 | 10,0129 |
| 11 B | 5 | 6 | 11,0093 |
| 12 C | 6 | 6 | 12,0000 |
| 13 C | 6 | 7 | 13,0034 |
| 14 N | 7 | 7 | 14,0031 |
| 15 N | 7 | 8 | 15,0001 |
| 16 O | 8 | 8 | 15,9949 |
| 17 O | 8 | 9 | 16,9991 |
| 18 O | 8 | 10 | 17,9992 |
| 19 F | 9 | 10 | 18,9984 |
| 20 Не | 10 | 10 | 19,9924 |
| 21 Не | 10 | 11 | 20,9938 |
| 22 Не | 10 | 12 | 21,9914 |
| 23 Na | 11 | 12 | 22,9898 |
| 24 мг | 12 | 12 | 23,9850 |
| 25 мг | 12 | 13 | 24,9858 |
| 26 мг | 12 | 14 | 25,9826 |
| 27 Эл | 13 | 14 | 26,9815 |
| 28 Si | 14 | 14 | 27,9769 |
| 29 Si | 14 | 15 | 28,9765 |
| 30 Si | 14 | 16 | 29,9738 |
| 31 P | 15 | 16 | 30,9738 |
| 32 S | 16 | 16 | 31,9721 |
| 33 S | 16 | 17 | 32,9715 |
| 34 S | 16 | 18 | 33,9679 |
| 36 S | 16 | 20 | 35,9671 |
| 35 Кл | 17 | 18 | 34,9689 |
| 37 Кл | 17 | 20 | 36,9659 |
| 36 Ар | 18 | 18 | 35,9675 |
| 38 Ар | 18 | 20 | 37,9627 |
| 40 Ар | 18 | 22 | 39,9624 |
| 39 K | 19 | 20 | 38,9637 |
| 40 K* | 19 | 21 | 39,9640 |
| 41 K | 19 | 22 | 40,9618 |
| 40 Ca | 20 | 20 | 39,9626 |
| 42 Ca | 20 | 22 | 41,9586 |
| 43 Ca | 20 | 23 | 42,9588 |
| 44 Ca | 20 | 24 | 43,9555 |
| 46 Ca | 20 | 26 | 45,9537 |
| 48 Ca | 20 | 28 | 47,9525 |
| 45 Sc | 21 | 24 | 44,9559 |
| 46 Ti | 22 | 24 | 45,9526 |
| 47 Ti | 22 | 25 | 46,9518 |
| 48 Ti | 22 | 26 | 47,9479 |
| 49 Ти | 22 | 27 | 48,9479 |
| 50 Ti | 22 | 28 | 49,9448 |
| 50 V* | 23 | 27 | 49,9472 |
| 51 V | 23 | 28 | 50,9440 |
| 50 Cr | 24 | 26 | 49,9460 |
| 52 Cr | 24 | 28 | 51,9405 |
| 53 Cr | 24 | 29 | 52,9406 |
| 54 Cr | 24 | 30 | 53,9389 |
| 55 Мн | 25 | 30 | 54,9380 |
| 54 Fe | 26 | 28 | 53,9396 |
| 56 Fe | 26 | 30 | 55,9349 |
| 57 Fe | 26 | 31 | 56,9354 |
| 58 Fe | 26 | 32 | 57,9333 |
| 59 Co | 27 | 32 | 58,9332 |
| 58 Ни | 28 | 30 | 57,9353 |
| 60 Ни | 28 | 32 | 59,9308 |
| 61 Ни | 28 | 33 | 60,9311 |
| 62 Ни | 28 | 34 | 61,9283 |
| 64 Ни | 28 | 36 | 63,9280 |
| 63 Cu | 29 | 34 | 62,9296 |
| 65 Cu | 29 | 36 | 64,9278 |
| 64 Zn | 30 | 34 | 63,9291 |
| 66 Zn | 30 | 36 | 65,9260 |
| 67 Zn | 30 | 37 | 66,9271 |
| 68 Zn | 30 | 38 | 67,9248 |
| 70 Zn | 30 | 40 | 69,9253 |
| 69 Ga | 31 | 38 | 68,9256 |
| 71 га | 31 | 40 | 70,9247 |
| 70 Ge | 32 | 38 | 69,9242 |
| 72 Ge | 32 | 40 | 71,9221 |
| 73 Ge | 32 | 41 | 72,9235 |
| 74 Ge | 32 | 42 | 73,9212 |
| 75 As | 33 | 42 | 74,9216 |
| 74 Se | 34 | 40 | 73,9225 |
| 76 Se | 34 | 42 | 75,9192 |
| 77 Se | 34 | 43 | 76,9199 |
| 78 Se | 34 | 44 | 77,9173 |
| 80 Se | 34 | 46 | 79,9165 |
| 82 Se | 34 | 48 | 81,9167 |
| 79 Br | 35 | 44 | 78,9183 |
| 81 Br | 35 | 46 | 80,9163 |
| 78 Кр | 36 | 42 | 77,9204 |
| 80 Кр | 36 | 44 | 79,9164 |
| 82 Кр | 36 | 46 | 81,9135 |
| 83 Кр | 36 | 47 | 82,9141 |
| 84 Кр | 36 | 48 | 83,9115 |
| 86 Кр | 36 | 50 | 85,9106 |
| 85 Кр | 37 | 48 | 84,9118 |
| 87 Гб | 37 | 50 | 86,9092 |
| 84 Sr | 38 | 46 | 83,9134 |
| 86 Sr | 38 | 48 | 85,9093 |
| 87 Sr | 38 | 49 | 86,9089 |
| 88 Sr | 38 | 50 | 87,9056 |
| 89 Y | 39 | 50 | 88,9058 |
| 90 Zr | 40 | 50 | 89,9047 |
| 91 Zr | 40 | 51 | 90,9056 |
| 92 Zr | 40 | 52 | 91,9050 |
| 94 Zr | 40 | 54 | 93,9063 |
| 93 Nb | 41 | 52 | 92,9064 |
| 92 мес. | 42 | 50 | 91,9068 |
| 94 Мо | 42 | 52 | 93,9051 |
| 95 мо | 42 | 53 | 94,9058 |
| 96 мес. | 42 | 54 | 95,9047 |
| 97 мо | 42 | 55 | 96,9060 |
| 98 мес. | 42 | 56 | 97,9054 |
| 100 мо | 42 | 58 | 99,9075 |
| 96 Ru | 44 | 52 | 95,9076 |
| 98 Ru | 44 | 54 | 97,9053 |
| 99 Ru | 44 | 55 | 98,9059 |
| 100 Ru | 44 | 56 | 99,9042 |
| 101 Ru | 44 | 57 | 100,9056 |
| 102 Ru | 44 | 58 | 101,9043 |
| 104 Ru | 44 | 60 | 103,9054 |
| 103 Rh | 45 | 58 | 102,9055 |
| 102 Pd | 46 | 56 | 101,9056 |
| 104 Rh | 46 | 58 | 103,9040 |
| 105 EPS | 46 | 59 | 104,9051 |
| 106 ЭПС | 46 | 60 | 105,9035 |
| 108 ЭПС | 46 | 62 | 107,9039 |
| 110 Pf | 46 | 64 | 109,9052 |
| 107 Ag | 47 | 60 | 106,9051 |
| 109 Ag | 47 | 62 | 108,9048 |
| 106 Cd | 48 | 58 | 105,9065 |
| 108 Cd | 48 | 60 | 107,9042 |
| 110 Cd | 48 | 62 | 109,9030 |
| 111 Cd | 48 | 63 | 110,9042 |
| 112 Cd | 48 | 64 | 111,9028 |
| 113 Cd*. | 48 | 65 | 112,9044 |
| 114 Cd | 48 | 66 | 113,9034 |
| 116 Cd* | 48 | 68 | 115,9048 |
| 113 W | 49 | 64 | 112,9041 |
| 115 W* | 49 | 66 | 114,9039 |
| 112 Sn | 50 | 62 | 111,9048 |
| 114 Sn | 50 | 64 | 113,9028 |
| 115 Sn | 50 | 65 | 114,9033 |
| 116 Sn | 50 | 66 | 115,9017 |
| 117 Sn | 50 | 67 | 116,9030 |
| 118 Sn | 50 | 68 | 117,9016 |
| 119 Sn | 50 | 69 | 118,9033 |
| 120 Sn | 50 | 70 | 119,9022 |
| 122 Sn | 50 | 72 | 121,9034 |
| 124 Sn | 50 | 74 | 123,9053 |
| 121 Сб | 51 | 70 | 120,9038 |
| 123 Сб | 51 | 72 | 122,9042 |
| 120 Te | 52 | 68 | 119,9040 |
| 122 Te | 52 | 70 | 121,9030 |
| 123 Te | 52 | 71 | 122,9043 |
| 124 Te | 52 | 72 | 123,9028 |
| 125 Te | 52 | 73 | 124,9044 |
| 126 Te | 52 | 74 | 125,9033 |
| 128 Te* | 52 | 76 | 127,9045 |
| 130 Te* | 52 | 78 | 129,9062 |
| 127 I | 53 | 74 | 126,9045 |
| 124 Xe* | 54 | 70 | 123,9059 |
| 126 Xe | 54 | 72 | 125,9043 |
| 128 Xe | 54 | 74 | 127,9035 |
| 129 Xe | 54 | 75 | 128,9048 |
| 130 Xe | 54 | 76 | 129,9035 |
| 131 Xe | 54 | 77 | 130,9051 |
| 132 Xe | 54 | 78 | 131,9042 |
| 134 Xe | 54 | 80 | 133,9054 |
| 136 Xe* | 54 | 82 | 135,9072 |
| 133 Cs | 55 | 78 | 132,9055 |
| 130 Ba* | 56 | 74 | 129,9063 |
| 132 Ба | 56 | 76 | 131,9051 |
| 134 Ба | 56 | 78 | 133,9045 |
| 135 Ба | 56 | 79 | 134,9057 |
| 136 Ба | 56 | 80 | 135,9046 |
| 137 Ба | 56 | 81 | 136,9058 |
| 138 Ба | 56 | 82 | 137,9052 |
| 138 La* | 57 | 81 | 137,9071 |
| 139 La | 57 | 82 | 138,9064 |
| 136 Ce | 58 | 78 | 135,9072 |
| 138 Ce | 58 | 80 | 137,9060 |
| 140 Ce | 58 | 82 | 139,9054 |
| 142 Ce | 58 | 84 | 141,9092 |
| 141 Пр | 59 | 82 | 140,9077 |
| 142 Нд | 60 | 82 | 141,9077 |
| 143 Нд | 60 | 83 | 142,9098 |
| 144 Нд | 60 | 84 | 143,9101 |
| 145 Нд | 60 | 85 | 144,9126 |
| 146 Нд | 60 | 86 | 145,9131 |
| 148 Нд | 60 | 88 | 147,9169 |
| 150 Нд* | 60 | 90 | 149,9209 |
| 144 См | 62 | 82 | 143,9120 |
| 147 См | 62 | 85 | 146,9149 |
| 148 См* | 62 | 86 | 147,9148 |
| 149 См | 62 | 87 | 148,9172 |
| 150 См | 62 | 88 | 149,9173 |
| 152 См | 62 | 90 | 151,9197 |
| 154 См | 62 | 92 | 153,9222 |
| 151 Eu* | 63 | 88 | 150,9199 |
| 153 Eu | 63 | 90 | 152,9212 |
| 152 Gd*. | 64 | 88 | 151,9198 |
| 154 Gd | 64 | 90 | 153,9209 |
| 155 Gd | 64 | 91 | 154,9226 |
| 156 Gd | 64 | 92 | 155,9221 |
| 157 Gd | 64 | 93 | 156,9240 |
| 158 Gd | 64 | 94 | 157,9241 |
| 160 Gd | 64 | 96 | 159,9271 |
| 159 Тб | 65 | 94 | 158,9253 |
| 156 Dy | 66 | 90 | 155,9243 |
| 158 Dy | 66 | 92 | 157,9244 |
| 160 Dy | 66 | 94 | 159,9252 |
| 161 Dy | 66 | 95 | 160,9269 |
| 162 Dy | 66 | 96 | 161,9268 |
| 163 Dy | 66 | 97 | 162,9287 |
| 164 Dy | 66 | 98 | 163,9292 |
| 165 Ho | 67 | 98 | 164,9303 |
| 162 Er | 68 | 94 | 161,9288 |
| 164 эр | 68 | 96 | 163,9292 |
| 166 Er | 68 | 98 | 165,9303 |
| 167 Er | 68 | 99 | 166,9320 |
| 168 эр | 68 | 100 | 167,9324 |
| 170 Er | 68 | 102 | 169,9355 |
| 169 Тм | 69 | 100 | 168,9342 |
| 168 Yb | 70 | 98 | 167,9339 |
| 170 Yb | 70 | 100 | 169,9348 |
| 171 Yb | 70 | 101 | 170,9363 |
| 172 Yb | 70 | 102 | 171,9364 |
| 173 Yb | 70 | 103 | 172,9382 |
| 174 Yb | 70 | 104 | 173,9389 |
| 176 Yb | 70 | 106 | 175,9426 |
| 175 Lu | 71 | 104 | 174,9408 |
| 176 Lu* | 71 | 105 | 175,9427 |
| 174 Hf* | 72 | 102 | 173,9400 |
| 176 Hf | 72 | 104 | 175,9414 |
| 177 Hf | 72 | 105 | 176,9432 |
| 178 Hf | 72 | 106 | 177,9437 |
| 179 Hf | 72 | 107 | 178,9458 |
| 180 Hf | 72 | 108 | 179,9466 |
| 181 W | 73 | 108 | 180,9480 |
| 180 W* | 74 | 106 | 179,9467 |
| 182 W | 74 | 108 | 181,9482 |
| 183 W | 74 | 109 | 182,9502 |
| 184 W | 74 | 110 | 183,9509 |
| 186 W | 74 | 112 | 185,9544 |
| 185 W | 75 | 110 | 184,9530 |
| 187 W | 75 | 112 | 186,9558 |
| 184 W | 76 | 108 | 183,9525 |
| 186 Осы* | 76 | 110 | 185,9538 |
| 187 Оса | 76 | 111 | 186,9558 |
| 188 Ос | 76 | 112 | 187,9558 |
| 189 Ос | 76 | 113 | 188,9581 |
| 190 Ос | 76 | 114 | 188,9581 |
| 192 Ос | 76 | 116 | 191,9615 |
| 191 Ир | 77 | 114 | 190,9606 |
| 193 Ир | 77 | 116 | 191,9626 |
| 190 Пт | 78 | 112 | 189,9599 |
| 192 Пт | 78 | 114 | 191,9610 |
| 194 Пт | 78 | 116 | 193,9627 |
| 195 Пт | 78 | 117 | 194,9648 |
| 196 Пт | 78 | 118 | 195,9650 |
| 198 Пт | 78 | 120 | 197,9679 |
| 197 Au | 79 | 118 | 196,9666 |
| 196 рт. ст. | 80 | 116 | 195,9658 |
| 198 рт. ст. | 80 | 118 | 197,9668 |
| 199 рт. ст. | 80 | 119 | 198,9683 |
| 200 рт.ст. | 80 | 120 | 199,9683 |
| 201 рт. ст. | 80 | 121 | 200,9703 |
| 202 рт.ст. | 80 | 122 | 201,9706 |
| 204 рт. ст. | 80 | 124 | 203,9735 |
| 203 Тл | 81 | 122 | 202,9723 |
| 205 Тл | 81 | 124 | 204,9744 |
| 204 Pb | 82 | 122 | 203,9730 |
| 206 Пб | 82 | 124 | 205,9745 |
| 207 Pb | 82 | 125 | 206,9759 |
| 208 Pb | 82 | 126 | 207,9767 |
| 209 Bi* | 83 | 126 | 208,9804 |
| 232 Th | 90 | 142 | 232,0381 |
| 235 U* | 92 | 143 | 235,0439 |
* являются нестабильными изотопами и имеют длительный период полураспада, равный возрасту Вселенной.
Ar (O) = 16 а.е.м.
Z (O) = 8 (протоны)
N = Ar (O) – Z (O) = 16 – 8 = 8 (нейтроны)
Ответ: Число протонов и нейтронов в атоме кислорода равно 8.
Число протонов в атоме равно заряду его ядра (обозначается Z), или порядковому номеру элемента в периодической таблице Менделеева.
Где N – число нейтронов, A – атомная масса элемента (в целых числах), Z – заряд ядра атома или порядковый номер атома в периодической таблице Менделеева.
Расширенный ответ
Масса атома – это сумма двух величин: масса протонов + масса нейтронов. Дело в том, что масса электронов пренебрежимо мала.
Масса нейтрона = 1.674 927 498 04(95)⋅10-²²⁷ кг = 1.008 664 915 60(57) а.е.м.
Масса протона = 1,672 621 923 69(51)⋅10-²⁷ кг = 1,007276466621(53) а.е.м.
Масса электрона = 9,109383 7015(28)⋅10-³¹ кг = 0,000548579909065 а.е.м.
Это означает, что даже 100 электронов дадут в сумме всего 0,0548579909065 а.е.м.
Первоначально Д. Менделеев основывал построение своей периодической таблицы на атомных весах элементов. Однако дальнейшее развитие науки показало, что свойства химических элементов напрямую зависят не от атомной массы химического элемента, а от заряда ядра его атома. Так, в периодической таблице химические элементы расположены в порядке возрастания заряда ядра атома, а номер элемента в таблице соответствует заряду его ядра. А заряд ядра равен сумме зарядов протонов. Это означает, что No (элемента) = Z (заряд ядра или число протонов).
Остальная часть массы ядра приходится на нейтроны. Для определения числа нейтронов в атоме достаточно из атомной массы вычесть число протонов, которое равно заряду ядра или номеру элемента в таблице Менделеева.
Примеры
Сколько протонов и нейтронов содержится в атоме натрия?
Ar (Na) = 23 а.е.
Z (Na) = 11 (протоны)
N = Ar (Na) – Z (Na) = 23 – 11 = 12 (нейтроны)
Ответ: Число протонов в атоме натрия равно 11, а число нейтронов в атоме натрия равно 12.
Сколько протонов и нейтронов содержится в атоме фосфора?
Ar (P) = 31 а.е.
Z (P) = 15 (протоны)
N = Ar (P) – Z (P) = 31 – 15 = 16 (нейтроны)
Ответ: Число протонов в атоме фосфора равно 15, а число нейтронов в атоме фосфора равно 16.
Сколько протонов и нейтронов содержится в атоме золота?
Ar (Au) = 197 а.е.
Z (Au) = 79 (протоны)
N = Ar (Au) – Z (Au) = 197 – 79 = 118 (нейтроны)
Ответ: число протонов в атоме золота равно 79, а число нейтронов в атоме золота равно 118.
Сколько протонов и нейтронов содержится в атоме кремния?
Ar (Si) = 28 а.е.
Z (Si) = 14 (протоны)
N = Ar (Si) – Z (Si) = 28 – 14 = 14 (нейтроны)
Ответ: число протонов и нейтронов в атоме кремния равно 14.
Сколько протонов и нейтронов содержится в атоме углерода?
Ar (C) = 12 a.u.
Z (C) = 6 (протоны)
N = Ar (C) – Z (C) = 12 – 6 = 6 (нейтроны)
Ответ: Число протонов и нейтронов в атоме углерода равно 6.
Сколько протонов и нейтронов содержится в атоме калия?
Ar (K) = 39 а.е.
Z (K) = 19 (протоны)
N = Ar (K) – Z (K) = 39 – 19 = 20 (нейтроны)
Ответ: число протонов в атоме калия равно 19, а число нейтронов в атоме калия равно 20.
Сколько протонов и нейтронов содержится в атоме железа?
Ar (Fe) = 39 а.е.
Z (Fe) = 19 (протоны)
N = Ar (Fe) – Z (Fe) = 56 – 26 = 30 (нейтроны)
Ответ: число протонов в атоме железа равно 19, а число нейтронов в атоме железа равно 30.
Сколько протонов и нейтронов содержится в атоме алюминия?
Ar (Al) = 27 а.е.
Z (Al) = 13 (протоны)
N = Ar (Al) – Z (Al) = 27 – 13 = 14 (нейтроны)
Ответ: Число протонов в атоме алюминия равно 13, а число нейтронов в атоме алюминия равно 14.
Сколько протонов и нейтронов содержится в атоме фтора?
Ar (F) = 19 а.е.
Z (F) = 9 (протоны)
N = Ar (F) – Z (F) = 19 – 9 = 10 (нейтроны)
Ответ: Число протонов в атоме фтора равно 9, а число нейтронов в атоме фтора равно 10.
Сколько протонов и нейтронов содержится в атоме хлора?
Ar (Cl) = 35 а.е.
Z (Cl) = 17 (протоны)
N = Ar (Cl) – Z (Cl) = 35 – 17 = 18 (нейтроны)
Ответ: число протонов в атоме хлора равно 17, а число нейтронов – 18.
Сколько протонов и нейтронов содержится в атоме кислорода?
Ar (O) = 16 а.е.
Z (O) = 8 (протоны)
N = Ar (O) – Z (O) = 16 – 8 = 8 (нейтроны)
Ответ: число протонов и нейтронов в атоме кислорода равно 8.
Сколько протонов и нейтронов содержится в атоме серы?
Ar (S) = 32 а.е.
Z (S) = 16 (протоны)
N = Ar (S) – Z (S) = 32 – 16 = 16 (нейтроны)
Ответ: число протонов и нейтронов в атоме серы равно 16.
Сколько протонов и нейтронов содержится в атоме магния?
Ar (Mg) = 32 а.е.
Z (Mg) = 16 (протоны)
N = Ar (Mg) – Z (Mg) = 24 – 12 = 12 (нейтроны)
Ответ: Число протонов в атоме магния равно 16, а число нейтронов – 12.
Сколько протонов и нейтронов содержится в атоме цинка?
Ar (Zn) = 65 а.е.
Z (Zn) = 30 (протоны)
N = Ar (Zn) – Z (Zn) = 65 – 30 = 35 (нейтроны)
Ответ: число протонов в атоме цинка равно 30, а число нейтронов в атоме цинка равно 35.
Общее количество фантомных частиц По после реакции
(O 17 8 + p 1 1):
393 + 12 = 405
Состав атомного ядра. Расчет протонов и нейтронов

Согласно современным представлениям, атом состоит из ядра и распределенных вокруг него электронов. Атомное ядро, в свою очередь, состоит из более мелких элементарных частиц – ряда протоны и нейтроны (обычно называемые нуклонами), связанные между собой ядерными силами.
Количество протонов в ядре определяет структуру электронной оболочки атома. А электронная оболочка определяет физические и химические свойства вещества. Количество протонов соответствует порядковому номеру атома в периодической таблице химических элементов Менделеева, также известному как зарядовое число, атомный номер, атомный номер. Например, число протонов в атоме гелия равно 2. В периодической таблице он имеет номер 2 и обозначается как He2 Символом для обозначения числа протонов является латинская буква Z. При записи формулы число, обозначающее количество протонов, часто помещают внизу символа элемента, справа или слева: Он2 / 2Он.
Количество нейтронов соответствует определенному изотопу элемента. Изотопы – это элементы с одинаковым атомным номером (одинаковым количеством протонов и электронов), но разным массовым числом. Массовое число – общее число нейтронов и протонов в ядре атома (обозначается латинской буквой A). При написании формул массовое число указывается в верхней части символа элемента с одной стороны: Он 4 2/ 4 2He (изотоп гелия – гелий-4).
Таким образом, чтобы узнать число нейтронов в изотопе, необходимо вычесть число протонов из общего массового числа. Например, мы знаем, что в атоме гелия-4 He 4 2 атом содержит 4 элементарные частицы, так как массовое число изотопа равно 4. В то же время мы знаем, что Он 4 2 имеет 2 протона. Вычитая из 4 (общее массовое число) 2 (число протонов), получаем 2 – число нейтронов в ядре гелия-4.
ПРОЦЕСС ПОДСЧЕТА КОЛИЧЕСТВА ФАНТОМНЫХ ЧАСТИЦ В ЯДРЕ АТОМА. В качестве примера мы рассмотрели гелий-4 (He 4 2), ядро которого состоит из двух протонов и двух нейтронов. Поскольку ядро гелия-4, называемое альфа-частицей (α-частицей), является наиболее эффективным в ядерных реакциях, его часто используют для экспериментов в этом направлении. Следует отметить, что в формулах ядерных реакций вместо He 4 часто используется символ α. 2 используется символ α.
Именно при участии альфа-частиц E. Резерфорд осуществил первую в официальной истории физики реакцию ядерного превращения. В ходе реакции α-частицы (He 4 2) “бомбардировали” ядра изотопа азота (N 14 7), образуя изотоп оксигена (O 17 8) и протон (p 1 ). 1)
Эта ядерная реакция протекает следующим образом:
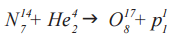
Давайте подсчитаем количество фантомных частиц Po до и после этого преобразования.
ДЛЯ ПОДСЧЕТА КОЛИЧЕСТВА ФАНТОМНЫХ ЧАСТИЦ ПО НЕМУ НЕОБХОДИМО:
Шаг 1 Рассчитайте количество нейтронов и протонов в каждом ядре:
– число протонов указано в подстрочном индексе;
– Найдите число нейтронов, вычитая число протонов (подстрочный индекс) из общего массового числа (надстрочный индекс).
Шаг 2: Подсчитайте количество фантомных частиц По в атомном ядре:
– Умножьте количество протонов на количество фантомных частиц Po, содержащихся в 1 протоне;
– Умножьте количество нейтронов на количество фантомных частиц Po, содержащихся в 1 нейтроне;
Шаг 3 Добавьте количество фантомных частиц Po:
– прибавить полученное число фантомных частиц Po в протонах к полученному числу в нейтронах в ядрах до реакции;
– прибавить полученное число фантомных частиц Po в протонах к полученному числу в нейтронах в ядрах после реакции;
– сравнить количество фантомных частиц Po до реакции с количеством фантомных частиц Po после реакции.
ПРИМЕР ДЕТАЛЬНОГО РАСЧЕТА ЧИСЛА ФАНТОМНЫХ ЧАСТИЦ В АТОМНЫХ ЯДРАХ.
(Ядерная реакция с участием α-частицы (He 4 2), выполненный Э. Резерфордом в 1919 году)
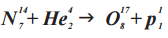
ДО РЕАКЦИИ (N 14 7 + He 4 2)
N 14 7
Количество протонов: 7
Количество нейтронов: 14-7 = 7
Количество фантомных частиц Po:
В 1 протоне – 12 Po, поэтому в 7 протонах: (12 x 7) = 84;
В 1 нейтроне – 33 Po, значит в 7 нейтронах: (33 x 7) = 231;
Общее количество фантомных частиц Po в ядре: 84+231 = 315
4 2
Количество протонов 2
Количество нейтронов 4-2 = 2
Количество фантомных частиц Po:
В 1 протоне – 12 Po, поэтому в 2 протонах: (12 x 2) = 24
в 1 нейтроне – 33 Po, значит в 2 нейтронах: (33 x 2) = 66
Общее число фантомных частиц По в ядре: 24+66 = 90
Общее количество фантомных частиц По до реакции
N 14 7 + He 4 2
315 + 90 = 405
ПОСЛЕ РЕАКЦИИ (O 17 8) и один протон (p 1 1):
O 17 8
Количество протонов: 8
Количество нейтронов: 17-8 = 9
Количество фантомных частиц Po:
В 1 протоне – 12 Po, поэтому в 8 протонах: (12 x  = 96
= 96
В 1 нейтроне – 33 Po, значит в 9 нейтронах: (9 x 33) = 297
Общее количество фантомных частиц Po в ядре: 96+297 = 393
p 1 1
Количество протонов: 1
Количество нейтронов: 1-1=0
Количество фантомных частиц Po:
В 1 протоне 12 линий.
Нет нейтронов.
Общее количество фантомных частиц Po в ядре: 12
Общее количество фантомных частиц По после реакции
(O 17 8 + p 1 1):
393 + 12 = 405
Давайте сравним количество фантомных частиц Po до и после реакции:
| Перед реакцией | После реакции |
| 405 | 405 |
Количество фантомных частиц Po до и после реакции одинаково.
ПРИМЕР СОКРАЩЕННОЙ ФОРМЫ ДЛЯ РАСЧЕТА КОЛИЧЕСТВА ФАНТОМНЫХ ЧАСТИЦ PO В ЯДЕРНОЙ РЕАКЦИИ.
Дальнейшие расчеты количества фантомных частиц Po приведены в сокращенной форме, в которой показано общее количество фантомных частиц Po в каждом ядре, а также их сумма до и после реакции.
Известной ядерной реакцией является реакция взаимодействия α-частиц с изотопом бериллия, в которой был обнаружен нейтрон, впервые открытый как самостоятельная частица путем ядерного превращения. Реакция была проведена в 1932 году английским физиком Джеймсом Чедвиком. Формула реакции такова:
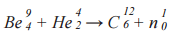
213 + 90 → 270 + 33 – число фантомных частиц По в каждом ядре
303 = 303 – общая сумма фантомных частиц По до и после реакции
Количество фантомных частиц Po до и после реакции одинаково.
Теперь определим число нейтронов в атоме, для чего выведем следующую формулу N=A-Z, в которой из атомной массы вычитаем порядковый номер элемента из числа его протонов. В качестве примера рассмотрим атом хлора, который в таблице Менделеева определяется как – Cl. В этом случае Z=17, исходя из чего число протонов и электронов равно – 17. A=35.453.
Как определить количество электронов, протонов и нейтронов в ядре атома?
Науке давно известно, что атомы любого химического элемента состоят из: положительно заряженного ядра и, соответственно, отрицательно заряженных электронов. В свою очередь, ядра атомов содержат положительно заряженные протоны и нейтроны с нулевым зарядом.
Многие люди задаются вопросом: как определить количество электронов, протонов и нейтронов в атомном ядре по Периодической таблице?
Для этого, конечно, нужно посмотреть непосредственно на саму периодическую таблицу.
Каждый элемент в химической системе Периодической таблицы имеет свой порядковый номер, который равен числу протонов (обозначается как ‘Z’) и числу электронов в атоме этого компонента.
Кроме того, с каждым субкомпонентом связан свой ядерный набор (одинаково классифицируемый как “А”), который, таким образом, указан в таблице рядом со знаком субкомпонента. Атомный номер компонента равен сумме числа протонов и числа нейтронов (обозначается “N”) в его ядре, в этом случае существует
мы имеем следующую формулу: A=N+Z
Теперь определим число нейтронов в атоме, для чего выведем следующую формулу N=A-Z, в которой из атомной массы вычитаем порядковый номер элемента, соответствующий его числу протонов. Примером может служить атом хлора, который в таблице Менделеева обозначен как Cl. В этом случае Z=17, исходя из чего число протонов и электронов равно – 17. A=35.453.
Но ведь количество нейтронов никак не может быть малым числом! Как именно это возможно? В таких вариантах ядерное изобилие округляется до значения, близкого к единице, в данном случае до 35 (в самом процессе малые значения ядерной темноты сочетаются с наличием изотопов – разновидностей 1-го и того же химического компонента, также отличающихся числом нейтронов в ядре).
Теперь мы можем найти количество нейтронов:
N=A-Z=35-17=18 нейтронов. Наконец, мы получаем результат 18 нейтронов.
Атомы различных химических компонентов имеют разную массу, объем, структуру и свойства.