Полярные молекулы также называют диполями. Неполярные соединения нейтральны или лишены диполей.
Полярность . – Свойство, показывающее изменение распределения электронной плотности вблизи ядер по сравнению с их первоначальным распределением в нейтральных молекулах, образующих связь.
Поляризуемость – Способность поляризоваться под воздействием электрического поля.
Мера полярности электрический момент диполя. В нейтральных соединениях она равна нулю. Его значение зависит от разницы в электроотрицательности элементов.
Длина диполя – Расстояние между его полюсами. Это свойство также влияет на степень поляризации.
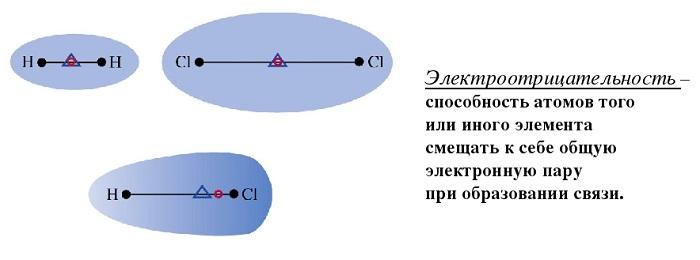
Каждое соединение состоит из ядра (положительные частицы) и электронов (отрицательные частицы). Как положительные, так и отрицательные частицы имеют собственные электрические центры тяжести.
Если центры тяжести частиц перекрываются, связь считается неполярной. Если полюса не перекрываются, то это дипольная связь.
Характеристика ионных связей:
Механизм химической связи
Существует два механизма, с помощью которых атомы взаимодействуют друг с другом:
обмен – предполагает взятие одного внешнего электрона из каждого атома и объединение их в общую пару;
Донор-акцептор – происходит, когда один атом (донор) отдает два электрона, а другой атом (акцептор) принимает их на свою свободную орбиталь.
Каким бы ни был механизм, химическая связь между атомами сопровождается выделением энергии. Чем выше ЭО атома, т.е. его способность притягивать электроны, тем сильнее всплеск энергии.
| Энергия связывания это энергия, которая выделяется при взаимодействии атомов. Он определяет прочность химической связи и равен силе, необходимой для ее разрыва. |
На прочность также влияют следующие параметры:
Длина связи – Расстояние между ядрами атомов. По мере уменьшения этого расстояния энергия связи увеличивается, а прочность связи возрастает.
Множественность связей – Число пар электронов, образующихся при взаимодействии атомов. Чем выше число, тем выше энергия и, следовательно, прочность связи.
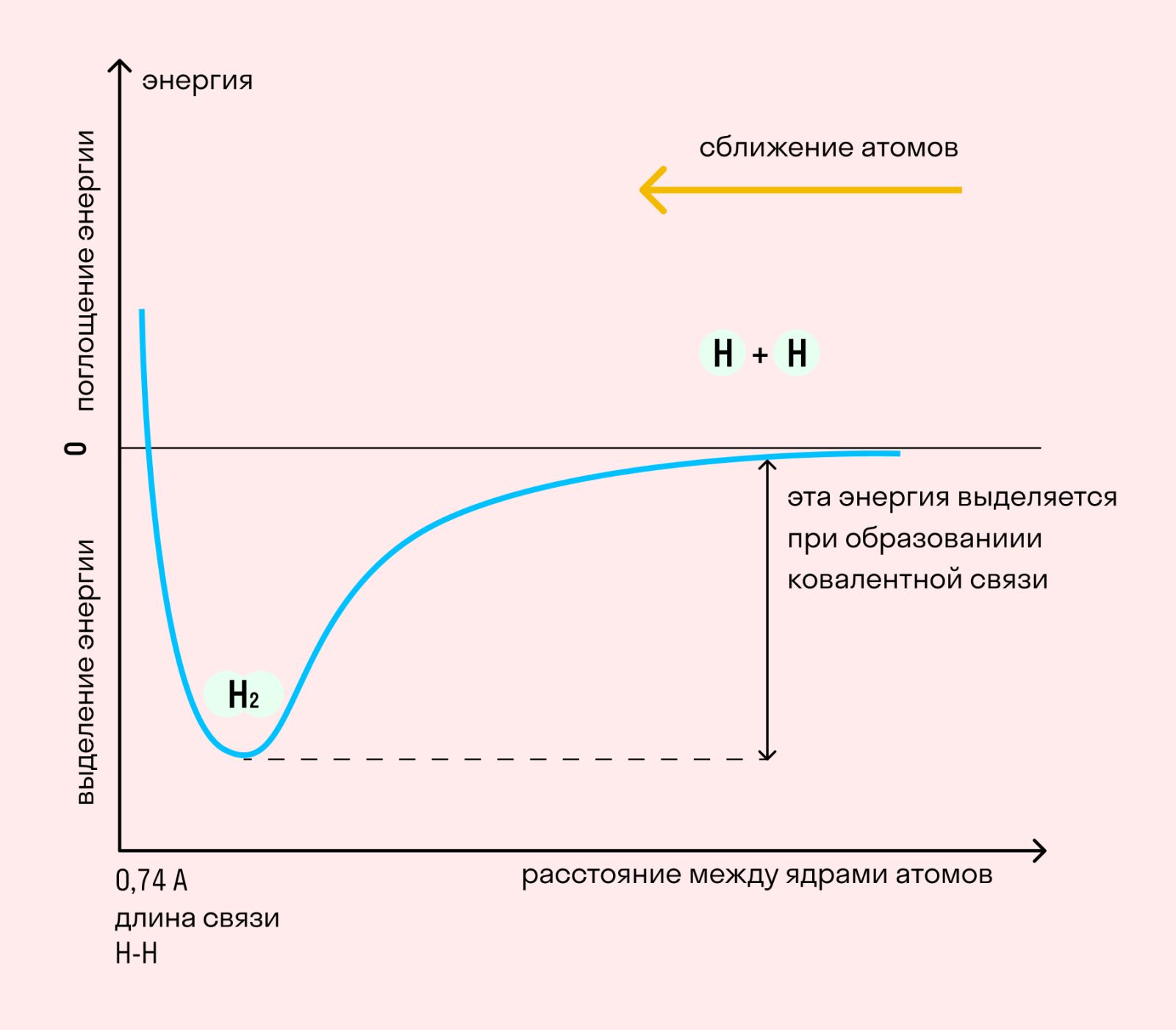
На примере химической связи в молекуле водорода посмотрим, как меняется энергия системы при уменьшении расстояния между ядрами атомов. Когда ядра сближаются, электронные орбитали атомов начинают перекрываться, образуя общую молекулярную орбиталь. Неспаренные электроны перемещаются от одного атома к другому через область перекрывания, и появляются общие электронные пары. Это сопровождается все большим высвобождением энергии. Сближение происходит до тех пор, пока притягивающая сила не уравновесится отталкивающей силой одноименных зарядов.
Полярность молекул
Полярные и неполярные молекулы
Полярные и неполярные молекулы. В каждой молекуле есть как положительно заряженные частицы – атомные ядра, так и отрицательно заряженные частицы – электроны. Для каждого типа частиц (точнее, зарядов) можно найти точку, которая будет его “электрическим центром тяжести”. Эти точки называются полюсами частицы. Если в молекуле электрические центры тяжести положительных и отрицательных зарядов совпадают, то молекула является неполярной. Это, например, молекулы H 2 , N 2 образованные одинаковыми атомами, в которых общие пары электронов одинаково принадлежат обоим атомам, а также многие симметрично построенные молекулы с атомными связями, как, например, метан CH 4 , четыреххлористый углерод CCl 4 . Однако если молекула построена асимметрично, например, состоит из двух разнородных атомов, то, как мы уже говорили, общая пара электронов может быть более или менее смещена в сторону одного из атомов. Очевидно, что в этом случае, из-за неравномерного распределения положительных и отрицательных зарядов внутри молекулы, их электрические центры тяжести не будут совпадать и получится полярная молекула (рис. 32).
Полярные молекулы являются диполями. Этот термин обычно относится к любой электрически нейтральной системе, т.е. системе, состоящей из положительных и отрицательных зарядов, распределенных таким образом, что их электрические центры тяжести не совпадают.
Полярность молекул
Частицы, состоящие из атомов одного и того же элемента, как правило, являются неполярный Так же как и сами облигации не являются полярными. Таким образом, молекулы H 2 , F 2 , N 2 являются неполярными.
Молекулы, образованные атомами различных элементов, могут быть полярная и неполярный . Это зависит от геометрическая форма .
Если форма симметрична, то молекула неполярна (BeH 2 , BF 3 , CH 4 CO 2 , SO 3 ), если она асимметрична (из-за наличия неспаренных пар или неспаренных электронов), то молекула полярна (NH 3 , H 2 O , SO 2 НЕТ 2 ).
Когда один из боковых атомов в симметричной молекуле заменяется атомом другого элемента, геометрическая форма также искажается и появляется полярность, например, в хлорпроизводные метана CH 3 Cl, CH 2 Cl 2 и CHCl 3 (молекулы метана метан CH 4 являются неполярными).
Полярность асимметричная молекула происходит от полярность ковалентных связей между атомами элементов с различной электроотрицательностью. .
Как уже упоминалось выше, существует частичный изменить электронной плотности вдоль оси связи к атому более электроотрицательного элемента, например:
(здесь δ – парциальный электрический заряд на атомах).
Крупнее разница в электроотрицательности элементов, тем больше абсолютное значение заряда δ i полярная это будет ковалентная связь.
Полярная ковалентная связь – тип ковалентной связи, образование которой объясняется взаимодействием атомов с существенно различной электроотрицательностью.
Определение, основные формулы
полярная ковалентная связь – вид ковалентной связи, образование которой объясняется взаимодействием атомов с существенно различной электроотрицательностью.
В молекуле хлористого водорода реализуется полярная ковалентная химическая связь, представленная обобщенной электронной парой атомов H и C l. Реальный электрический заряд, образованный на атомах молекулы, имеет частное значение, обозначаемое греческой буквой δ (дельта). Вектор смещения электронной пары может быть указан стрелкой.
Если взаимодействующие элементы имеют разные электроотрицательности, то общая электронная пара движется в сторону элемента с большей электроотрицательностью. В этом процессе частичный отрицательный заряд может наблюдаться в атоме с более высоким EO, из-за наличия избытка отрицательно заряженных электронов.
Этот процесс приводит к образованию частичных зарядов H + 0 , 18 и C l – 0 , 18 на атомах соединения. При этом в молекуле образуется пара полюсов, т.е. положительный и отрицательный. Такая ковалентная связь называется полярной.
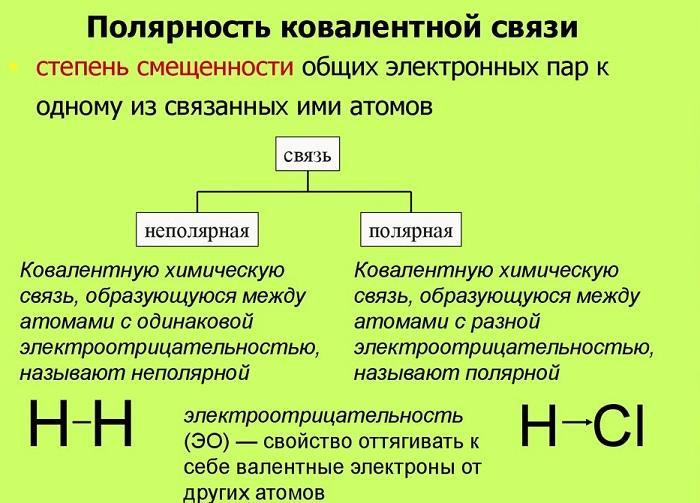
Ковалентная неполярная связь это вид химической связи, которая образуется между атомами, имеющими одинаковую электроотрицательность.
9. В высших оксидах элементов 3-го периода, по мере увеличения порядкового номера элемента, изменяется тип химической связи
Упражнения Упражнения
1. Ковалентные неполярные связи образуются каждым из веществ, формулы которых приведены ниже
2. Любое вещество, формула которого основана на ковалентных полярных связях
3. Только ионная связь может образовать любое вещество, формула которого имеет вид
4. Металлическая связь характерна для элементов, перечисленных в списке
1. Ba, Rb, Se
2. Cr, Ba, Si
3. Na, P, Mg
4) Rb, Na, Cs
5. Соединения, имеющие только ионные и только ковалентные полярные связи, являются соответственно
6. Между элементами образуется ионная связь
1) хлор и бром
2) бром и сера
3. цезий и бром
4) фосфор и кислород.
7. Между элементами образуется полярная ковалентная связь
1) кислород и калий
2. сера и фтор
3. бром и кальций
4) рубидий и хлор.
8. Химическая связь в летучих водородных соединениях элементов группы VA периода 3 выглядит следующим образом
1) ковалентный полярный
2) ковалентный неполярный
3) ионный
4) металлический
9. В высших оксидах элементов третьего периода тип химической связи изменяется с увеличением порядкового номера элемента
1) от ионной связи к полярной ковалентной связи
2) от металлической связи к неполярной ковалентной связи
3) от полярной ковалентной связи к ионной связи
4) от ковалентной полярной связи к металлической связи.
10. длина связи E-H увеличивается во многих веществах
11. длина связи E-H уменьшается в ряде веществ
12. Количество электронов, участвующих в образовании химических связей в молекуле хлористого водорода
13. Количество электронов, участвующих в образовании химических связей в молекуле P2O5, —
14. В хлориде фосфора (V) химическая связь
1) ионный
2) полярный ковалентный
3) неполярная ковалентная связь
4) металлическая связь
15. Наиболее полярная химическая связь в молекуле
1. фтористый водород
2) хлористый водород
3. вода
4. сероводород
16. Наименее полярная химическая связь в молекуле
1. хлористый водород
2. бром
3. вода
4. сероводород
17. Связь образуется в веществе благодаря общей электронной паре
18. Ковалентная связь образуется между элементами, которые имеют следующие порядковые номера
1) 3 и 9
2) 11 и 35
3) 16 и 17
4) 20 и 9
19. Ионная связь образуется между элементами, которые имеют следующие порядковые номера
1) 13 и 9
2) 18 и 8
3) 6 и 8
4) 7 и 17
20. В списке веществ, формулы которых объединяются только ионной связью, это
К диэлектрикам также относятся следующие вещества (NaCl, KCl, KBr, .)молекулы которых имеют ионную структуру. Ионные кристаллы – это пространственные сети, в которых попеременно встречаются ионы разных знаков. Эти кристаллы нельзя разделить на отдельные молекулы, но их можно рассматривать как систему из двух ионных подрешеток, вложенных друг в друга. Когда к ионному кристаллу прикладывается электрическое поле, происходит определенная деформация кристаллической решетки или относительное смещение подрешеток, в результате чего возникают дипольные моменты.
Элементарная физика
Диэлектрики (изолятор) – это вещества, которые не способны проводить электричество. Идеальных изоляторов в природе не существует. Все вещества проводят электричество, по крайней мере, в небольшой степени. Однако вещество, называемое диэлектриком, проводит электричество в несколько раз хуже, чем вещество, называемое проводником.
Если диэлектрик внести в электрическое поле, то поле и сам диэлектрик претерпевают значительные изменения. Чтобы понять, почему это происходит, мы должны учитывать, что атомы и молекулы содержат положительно заряженные ядра и отрицательно заряженные электроны.
Поскольку положительный заряд всех ядер молекулы равен суммарному заряду электронов, молекула в целом электрически инертна. Если заменить положительные заряды ядер частиц на суммарный заряд +qкоторый является центром “притяжения” положительных зарядов и заряда всех электронов суммарным отрицательным зарядом -qчастица, находящаяся в центре тяжести отрицательных зарядов, может рассматриваться как электрический диполь с электрическим импульсом, определяемым уравнением (7.1)
В отсутствие внешнего электрического поля центры тяжести положительных и отрицательных зарядов совпадают. Эти частицы не имеют собственного дипольного момента и называются неполярными. неполярный.
Асимметричные молекулы имеют несбалансированные центры тяжести зарядов разных знаков, смещенные друг к другу. В этом случае молекулы имеют внутренний дипольный момент и называются полярными. полярный.
Под воздействием внешнего электрического поля заряды в неполярной молекуле движутся навстречу друг другу: положительные заряды – к полю, отрицательные – от поля. В результате молекула приобретает дипольный момент, величина которого, как показывает эксперимент, пропорциональна напряженности поля. В рационализированной системе коэффициент пропорциональности записывается в виде , где – электрическая постоянная, а – величина, называемая поляризуемость молекулы. Принимая во внимание, что направления и совпадают, можно написать
Процесс поляризации неполярной молекулы протекает так, как если бы положительные и отрицательные заряды молекулы были связаны между собой упругими силами. Поэтому говорят, что неполярная молекула ведет себя во внешнем поле как упругий диполь.
Действие внешнего поля на полярную молекулу в основном сводится к тенденции поворачивать молекулу так, чтобы ее дипольный момент был фиксирован в направлении поля. Внешнее поле практически не влияет на дипольный момент. Следовательно, полярная молекула ведет себя как жесткий диполь во внешнем поле.
К диэлектрикам также относятся вещества (NaCl, KCl, KBr, …)молекулы имеют ионную структуру. Ионные кристаллы представляют собой пространственные сети с регулярным чередованием ионов разных знаков. Можно не разделять отдельные молекулы, а рассматривать их как систему из двух ионных подсетей, вложенных друг в друга. Когда к ионному кристаллу прикладывается электрическое поле, происходит своего рода деформация решетки или относительное смещение подрешеток, в результате чего возникают дипольные моменты.
Таким образом, введение всех трех диэлектрических групп во внешнее электрическое поле приводит к ненулевому результирующему диэлектрическому электрическому моменту, другими словами, к поляризации диэлектрика. Поляризация это процесс ориентации диполей или появление ориентированных по полю диполей во внешнем электрическом поле.
Существует три типа поляризации в зависимости от трех групп диэлектриков:
Электрон, или деформационная поляризация диэлектрик с неполярными молекулами, с индукцией дипольного момента на атомах из-за деформации электронных орбиталей
показательный, или дипольная поляризация диэлектриков с полярными молекулами, включающая ориентацию имеющихся дипольных моментов молекул вдоль поля. Тепловое движение, естественно, препятствует полной ориентации молекул, но совместное действие обоих факторов (электрического поля и теплового движения) приводит к преимущественной ориентации дипольных моментов молекул в направлении поля. Чем выше напряженность электрического поля и ниже температура, тем больше преобладает ориентация;
ионная поляризация диэлектриков с ионными кристаллическими решетками, что предполагает смещение подсети положительных ионов вдоль поля и отрицательных ионов в сторону от поля, в результате чего возникают дипольные моменты.
Читайте далее: