Катализаторы – химические вещества вовлечен в химической реакции, которые изменяют скорость и направление химической реакции.но не потребляемый в ходе реакции (в конце реакции они не изменяются ни количественно, ни по составу). Примерный каталитический механизм реакции A + B может быть представлен следующим образом:
Химическая кинетика. Скорость химических реакций
Скорость химической реакции показывает, насколько быстро протекает реакция. Взаимодействие происходит, когда молекулы сталкиваются в пространстве. Реакция происходит не при каждом столкновении, а только тогда, когда молекулы обладают достаточной энергией.
Скорость реакции – Число элементарных столкновений взаимодействующих частиц, приводящих к химическому превращению, в единицу времени.
Определение скорости химической реакции связано с условиями, в которых протекает реакция. Если реакция является однородным – то есть продукты и реактивы находятся в одной фазе – тогда скорость химической реакции определяется как изменение концентрации вещества в единицу времени:
υ = ΔC / Δt
Если реактанты или продукты находятся в разных фазах и столкновение молекул происходит только на границе фаз, то реакция называется гетерогенныйа его скорость определяется изменением количества вещества в единицу времени на единицу площади реакции:
υ = Δν / (S-Δt)
В результате решения мы видим, что если уменьшить концентрацию водорода вдвое, то скорость реакции уменьшается в 8 раз.
Скорость химической реакции
Скорость химической реакции – это фундаментальное понятие в химической кинетике, которое выражает отношение количества реактива (в молях) к продолжительности времени, в течение которого происходило взаимодействие.
Скорость реакции отражает изменение концентрации реагирующих веществ в единицу времени. Единицы измерения для гомогенной реакции: моль/л * сек. Физический смысл заключается в том, что каждую секунду определенное количество одного вещества превращается в другое в единице объема.
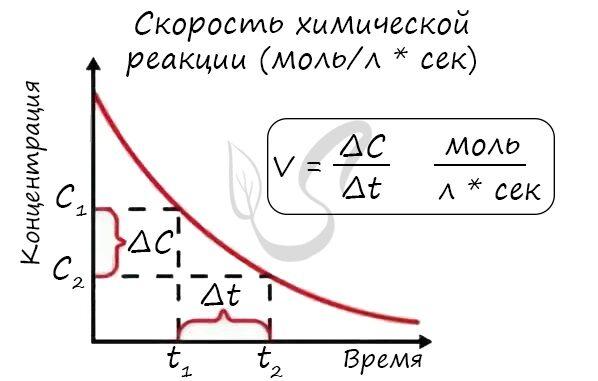
Я встречал задачи, в которых были указаны молярная концентрация вещества до и после реакции, время и объем. Это было необходимо для расчета скорости реакции. Давайте решим такую простую задачу на примере:
Молярная концентрация вещества до реакции составляла 1,5 моль/л, после реакции – 3 моль/л. Объем смеси составляет 10 литров, а реакция заняла 20 секунд. Рассчитайте скорость реакции.
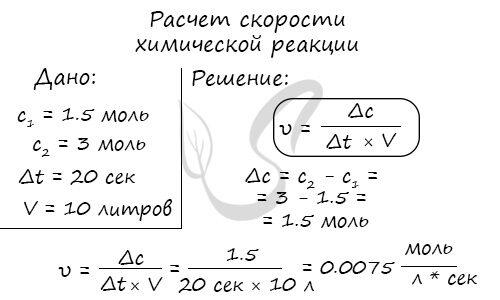
Влияние природы реактантов
При изучении состояний вещества возникает вопрос: где реакции протекают быстрее всего: между газами, растворами или твердыми телами?
Помните, что самая быстрая скорость реакции происходит между растворами, в жидкостях. В газах она несколько ниже.

Если реакция гетерогенная: жидкость + твердое тело, газ + твердое тело, жидкость + газ, то большую роль играет поверхность контакта реагирующих веществ.
Очевидно, что большой кусок железа, помещенный в соляную кислоту, будет реагировать гораздо дольше, чем дробленое железо – железные опилки.

Химическая активность также играет важную роль. Например, чтобы ответить на вопрос: какой металл Li или K быстрее реагирует с водой? Мы отдадим предпочтение литию, потому что он находится слева от калия в ряду активности металлов, поэтому литий более активен, чем калий.

Иногда для правильного ответа на вопрос о скорости реакции требуется знание активности кислоты. Более подробно мы обсудим эту тему в разделе гидролиза, а пока отмечу: чем сильнее (активнее) кислота, тем быстрее протекает реакция.
Например, реакция магния с серной кислотой протекает гораздо быстрее, чем реакция магния с уксусной кислотой. Это объясняется тем, что серная кислота является сильной (активной) кислотой, а уксусная кислота обладает меньшей активностью и является слабой кислотой.
Как уже упоминалось, слабые и сильные кислоты и основания изучаются в теме гидролиза.
Влияние изменения концентрации
Влияние концентрации “прямо пропорционально” скорости реакции: когда концентрация реагирующего вещества увеличивается, при ее уменьшении скорость реакции уменьшается.
Отмечу деталь, которая может быть важна, если в реакции участвуют газы: при увеличении давления концентрация вещества в единице объема увеличивается (представьте, что газ сжимается). Поэтому повышение давления, если среди исходных веществ есть газ, увеличивает скорость реакции.

Закон сохранения массы определяет взаимосвязь между концентрациями реактантов и их продуктов. Скорость простой реакции aA + bB → cC задается уравнением:
Физический смысл константы скорости – k – заключается в том, что она численно равна скорости реакции при условии, что концентрации реагирующих веществ равны 1. Обратите внимание, что стехиометрические коэффициенты уравнения переведены в степени – a и b.
Полученное следствие закона эффективной массы необходимо не только “запомнить”, но и понять. Поэтому мы решим несколько задач, в которых нужно будет написать подобную формулу.
Окисление диоксида серы происходит в соответствии с уравнением: 2SO2(г) + O2 = 2SO3(г). Как изменится скорость этой реакции, если объемы системы уменьшить в три раза?

Решение показывает, что в этом случае скорость реакции увеличится в 27 раз.
Давайте решим еще одну проблему. Приведем реакцию синтеза аммиака: N2 + HH2 = 2NH3. Как изменится скорость реакции прямого образования аммиака, если концентрацию водорода уменьшить вдвое?

В результате решения мы видим, что если уменьшить концентрацию водорода в два раза, то скорость реакции уменьшается в 8 раз.
Влияние изменения температуры на скорость реакции
Постулат, который я рекомендую временно принять: “Повышение температуры увеличивает скорость абсолютно всех химических реакций: как экзотермических, так и эндотермических. Исключений нет!”
Очень часто в следующей теме, химическом равновесии, вас будут пытаться запутать и ввести в заблуждение, но не сдавайтесь и помните постулат!
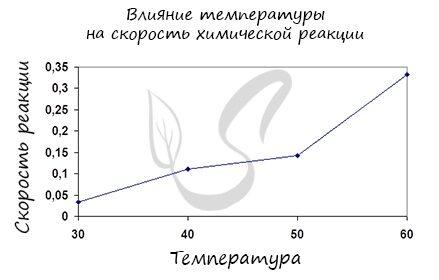
Таким образом, влияние температуры на скорость реакции “прямо пропорционально”: чем выше температура, тем выше скорость реакции – чем ниже температура, тем ниже скорость реакции. Однако, как и в случае с концентрацией, здесь есть нечто большее, чем простая “пропорция”.
Правило Вант-Гоффа, голландского химика, позволяет точно оценить влияние температуры на скорость химической реакции. Это происходит следующим образом: “На каждые 10 градусов повышения температуры константа скорости гомогенной элементарной реакции увеличивается в два-четыре раза.

- υ1 – скорость реакции при температуре t1
- υ2 – скорость реакции при температуре t2
- γ – температурный коэффициент, который может составлять от 2 до 4 раз
Если в вашем решении температурный коэффициент меньше 2 или больше 4, то, скорее всего, вы где-то допустили ошибку. Используйте этот факт для самопроверки.
Для тренировки давайте решим несколько задач, требующих применения правила Ванта-Гоффа.
Как изменится скорость гомогенной реакции при повышении температуры с 27°C до 57°C с температурным коэффициентом три?

“Вычислите температурный коэффициент скорости реакции, если известно, что при понижении температуры с 250°C до 220°C скорость реакции уменьшилась в восемь раз”.

Катализаторы и ингибиторы
Катализатор (греч. catalysis – разрушать) – это вещество, которое ускоряет химическую реакцию, но не участвует в ней. Катализатор не расходуется в ходе химической реакции.
Во многих химических реакциях в нашем организме участвуют катализаторы – белковые молекулы, ферменты. Без катализаторов такие реакции заняли бы сотни лет, но с катализаторами они занимают доли секунды.
Катализ – это явление ускорения химической реакции под воздействием катализатора, а химические реакции с участием катализатора называются каталитическими реакциями.

Ингибитор (лат. inhibere) – это вещество, которое замедляет или предотвращает химическую реакцию.
Ингибиторы используются для замедления коррозии металлов, окисления топлива и старения полимеров. Многие препараты являются ингибиторами.
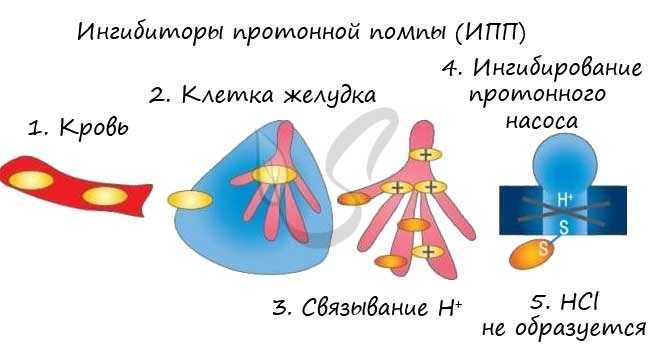
Например, для лечения гастрита (гастер – воспаление желудка) или язвы часто назначают ингибиторы протонной помпы – химические препараты, блокирующие выработку HCl слизистой оболочкой желудка. В результате соляная кислота перестает воздействовать на поврежденную стенку желудка, и воспаление спадает.
© Юрий Сергеевич Беллевич 2018-2021
Эта статья написана Юрием Сергеевичем Беллевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе копирование на другие сайты и ресурсы в Интернете) или любое другое использование информации и объектов без предварительного согласия владельца авторских прав преследуется по закону. Для получения разрешения на использование данного материала и получения разрешения, пожалуйста, свяжитесь с Юрий Беллевич..
Запишем закон действия масс для данной реакции.
w1 = k*[CO] 2 [O2].
Как найти температурный коэффициент
Принцип Вант-Гоффа:
На каждые 10 градусов повышения температуры скорость реакции увеличивается примерно в 2-4 раза.
v2 = v1*y Δt/10 .
v – скорость реакции.
y (гамма) – температурный коэффициент скорости, число, характеризующее ускорение реакции при нагревании на 10 градусов.
Δt – разница температур.
Закон массового действия (LMA):
Скорость химической реакции пропорциональна произведению концентраций реагирующих веществ.
Например, для реакции aA + bB = C, v = k*[A] a * [B] b ,
k – константа скорости, [A]и [B] – концентрации реагирующих веществ, a и b – стехиометрические коэффициенты.
10.1 – Температурная зависимость скорости реакции.
Задание.
При температуре 0 o C реакция, для которой температурный коэффициент равен 2, завершается за 120 с.
При какой температуре эта реакция может завершиться за 15 секунд?
Решение.
Скорость реакции будет увеличиваться при v2/v1 = 120/15 = 8 раз.
Согласно уравнению Вант-Гоффа,
v2/v1 = y Δt/10 .
8 = 2 Δt/10 , Δt/10 = 3, следовательно, разница температур Δt = 30 градусов.
t = 0 + Δt = 30 o C.
Поддержка проекта
Через какое время закончится реакция при температуре 30 o C, если она закончилась через 20 минут при температуре 10 градусов?
Температурный коэффициент равен 2.
Согласно уравнению Ванта-Гоффа, скорость будет увеличиваться при
v2/v1 = y Δt/10 = 2 (30-10)/10 = 2 2 = 4 раза.
Реакция завершится при t = 20/4 = 5 минут.
При температуре 0 градусов Цельсия реакция завершается за 1 час 21 минуту, а при температуре 40 оС – за 1 минуту.
Определите температурный коэффициент реакции.
1 час 21 минута равна 81 минуте. Таким образом, скорость увеличения v2/v1 = 81/1 = 81 раз.
Δt/10 = (40 – 0)/10 = 4.
v2/v1 = y Δt/10 .
81 = y 4 .
y = 3.
Поддержка проекта
Во сколько раз скорость реакции 2CO(г) + O2(y) = 2CO2 если давление увеличится в 2 раза, а температура останется неизменной?
Запишите закон действия масс для этой реакции.
w1 = k*[CO] 2 [O2].
Увеличение давления в 2 раза означает увеличение концентрации в 2 раза.
w2 = k*[2CO] 2 [2О2] = 8k*[CO] 2 [O2]
Во сколько раз нужно увеличить внешнее давление в системе, чтобы скорость реакции A(d) + 2B(d) -> C(d) увеличилась в 125 раз?
Как и в предыдущем примере, запишем:
w1 = [A][B ] 2
Дайте давлению увеличиться в x раз. Тогда,
w2 = [xA][xB] 2 = x 3 [A][B ] 2
w2/w1 = x 3 [A][B ] 2 / [A][B ] 2 = x 3
По конвенции,
х 3 = 125
х = 5
Поддержка проекта
Во сколько раз увеличивается скорость реакции 2NO + O2 = 2NO2 при разбавлении смеси реагирующих газов в 3 раза?
При разбавлении смеси реагирующих газов в 3 раза концентрация уменьшается в 3 раза.
w2 = k*[1/3] 2 [1/3] = (1/27)k*[NO] 2 [O2]
w2/w1 = 1/27.
Это означает, что концентрация уменьшится в 27 раз.
Реакция протекает по уравнению: A + 2B ↔ C; его константа скорости при определенной температуре равна 0,4, а начальные концентрации составляли (моль/дм 3 ): [A] =0.3 и [B]=0.5. Вычислите скорость этой реакции при той же температуре в начальный момент времени и после вступления в реакцию 0.1 моль/дм 3 вещества A.
Решение.
Напишите кинетическое уравнение, используя закон действующей массы.
v = k[A][B] 2
Следовательно, в начальный момент v = 0,4*0,3*0,5 2 = 0,03
После реакции 0,1 моль/дм3 с A его концентрация составит [A]= 0,3 – 0,1 = 0,2
Концентрация B, согласно уравнению реакции, составит 0,5 – 0,1*2 = 0,3.
v = 0,4*0,2*0,3 2 = 0,0072.
Поддержка проекта
Константа скорости определенной реакции при температуре 440 градусов Цельсия составляет 0,48 с -1 , а при температуре 400 градусов 0,03 с -1 . Рассчитайте температурный коэффициент и энергию активации реакции.
Для определения температурного коэффициента мы используем правило Вант-Гоффа.
k2/k1 = γ Δt/10
0,48/0,03 = γ (440 – 400)/10
γ 4 = 16
γ = 2.
Для определения энергии активации мы используем Уравнение Аррениуса в виде интеграла.
ln(k2/k1) = (Ea/R)(1/T1 – 1/T2)
Альтернативно, перейдя к десятичному логарифму:
lg(k2/k1) = (Ea/2,3R)(1/T1 – 1/T2)
Не забудьте перевести температуру в Кельвины!
ln(0,48/0,03) = (Ea/8,314)(1/673 – 1/713)
Ea = 3,87*10 5 кДж/моль.
9.5.1.Задача.
Вычислите температурный коэффициент Ванта-Гоффа в диапазоне 10-50 градусов Цельсия, если энергия активации равна 85 кДж/моль.
Не забудьте перевести килоджоули в джоули, градусы Цельсия в Кельвины.
ln(k2/k1) = (Ea/R)(1/T1 – 1/T2)
ln(k2/k1) = (85000/8,314)(1/283 – 1/323)
ln(k2/k1) = 4,474
k2/k1 = e 4,474 = 2,718 4,474 = 87,7.
Определите коэффициент Ванта-Гоффа.
k2/k1 = γ Δt/10
87,7 = γ 4
9.5.2.
Ввод в эксплуатацию.
В диапазоне 12-52 градусов Цельсия коэффициент Вант-Гоффа равен 3,5. Найдите энергию активации.
При допущениях идеализации изменение давления и изменение объема линейны.
содержание
Если интересующая переменная зависит от температуры без гистерезиса и скачков, т.е. однозначно, то ее температурная зависимость может быть описана на основе эталонной температуры. В простейшем случае достаточно аппроксимирующей функции с одним температурным коэффициентом: ξ < displaystyle xi> T < displaystyle T> T 0 < displaystyle T_ <0>>.
В качестве контрольной температуры часто выбирают 20 °C.
В общем, любая температурная характеристика может быть описана рядом Тейлора:
Аппроксимация получается с помощью полинома Тейлора степени n:
В наиболее распространенных результатах линейной аппроксимации: знак n равен 1
Температурные коэффициенты можно рассчитать следующим образом, выведя известную функцию: ξ ( τ )
Обратите внимание, что температурные коэффициенты зависят от опорной температуры.
Таким образом, уравнение Аррениуса имеет вид
Здесь – число всех столкновений, доля пространственно благоприятных столкновений (принимает значения от 0 до ), доля активных столкновений, т.е. энергетически благоприятных столкновений.
Как найти температурный коэффициент
При постоянной температуре реакция возможна, если взаимодействующие молекулы обладают определенным запасом энергии. Аррениус назвал этот избыток энергии энергией активации, а молекулы – энергией активации.
Согласно Аррениусу, константа скорости и энергия активации связаны между собой соотношением, называемым уравнением Аррениуса:
| (5.3) |
предэкспоненциальный множитель, – универсальная газовая постоянная, – абсолютная температура.
Таким образом, при постоянной температуре скорость реакции определяется . Чем больше , тем меньше число активных молекул и тем медленнее протекает реакция. По мере уменьшения скорости скорость увеличивается, и при = 0 реакция протекает мгновенно.
Эта величина характеризует природу реактантов и определяется экспериментально из соотношения . Записав уравнение (5.3) в логарифмической форме и решив его для констант при двух температурах, получим :
Если = 50-100 кДж∙моль -1 , то из уравнения Аррениуса следует, что при изменении температуры реакции на 10 градусов ее скорость изменится в 2-4 раза. Этот принцип был установлен эмпирически Вант-Гоффом:
γ – температурный коэффициент скорости химической реакции. Правило Вант-Гоффа имеет ограниченное применение, поскольку γ зависит от температуры и вне диапазона = 50-100 кДж ∙ моль -1 правило вообще не выполняется.
На рис. 5.4 показано, что энергия, затраченная на перевод исходных продуктов в активное состояние (A* – активированный комплекс), затем полностью или частично высвобождается при переходе к конечным продуктам. Разница между энергиями начального и конечного продуктов определяет ход реакции, который не зависит от энергии активации.
Поэтому на пути от начального состояния к конечному система должна преодолеть энергетический барьер. Только активные молекулы, обладающие в момент столкновения необходимой избыточной энергией, равной , могут преодолеть барьер и вступить в химическое взаимодействие. При повышении температуры доля активных молекул в реакционной среде увеличивается.
Предэкспоненциальный множитель характеризует общее количество столкновений. Для реакций с простыми молекулами это близко к теоретическому значению столкновений, т.е. рассчитанному по кинетической теории газов. Для сложных молекул ≠ , поэтому необходимо ввести управляющий фактор :
Стерический фактор учитывает тот факт, что для взаимодействия сложных активных молекул необходима определенная взаимная ориентация: протекание процессов облегчается столкновением молекул в местах встречи их реактивных связей или неиспользованных электронных пар.
Поэтому уравнение Аррениуса имеет вид
Здесь – количество всех столкновений, здесь – доля столкновений, выгодных в пространстве (принимает значения от 0 до ), здесь – доля активных столкновений, то есть энергетически выгодных.
Размерность константы скорости получается из соотношения
и, как видно из уравнения Аррениуса, размерность предфактора одинакова.
Для концентрации i, выраженной в моль∙л -1 , она имеет следующие приблизительные значения в реакциях с различными молекулярными плотностями:
| 10 13 -10 14 c -1 | 10 11 -10 12 л∙моль -1 c -1 | 10 9 -10 11 л∙моль -1 c -1 |
Анализируя выражение (5.3), мы приходим к выводу, что существует две основные возможности ускорения реакции
a) повышение температуры,
б) понижение энергии активации.
Пример. В скороварке температура кипения воды повышается на 20°C при давлении 2 атмосферы. Сколько раз ускоряется процесс приготовления пищи в скороварке?
Температурный коэффициент реакции. Принцип Ванта-Гоффа
Элементарные акты химических реакций происходят в результате столкновений взаимодействующих молекул. Температура характеризует среднюю кинетическую энергию хаотического движения молекул. Поэтому с увеличением температуры скорость каждого каждой химической реакции должно увеличиваться с повышением температуры. Уже в 1884 году. Вант-Гофф обобщил эмпирический материал и установил правило, названное его именем.
Правило Вант-Гоффа. При не слишком высоких и не слишком низких температурах скорость большинства химических реакций увеличивается в 2-4 раза при повышении температуры на 10 градусов.
Математически этот принцип ( ![]() ) записывается в терминах так называемого у:
) записывается в терминах так называемого у:
![]()
Согласно правилу Ванта-Гоффа, y = 2-^4.
Пример. В скороварке температура кипения воды повышается на 20°C при давлении 2 атмосферы. Сколько раз ускоряется процесс приготовления пищи в скороварке?
Решение. Если предположить, что среднее значение y = 3 для реакции приготовления, то ![]() . Поэтому то, что требовалось приготовить для
. Поэтому то, что требовалось приготовить для
час в кастрюле, будет готов примерно через 5 минут в скороварке!
Читайте далее:- Что такое электродный потенциал; Школа для инженеров-электриков: электротехника и электроника.
- Температура – карта знаний.
- Лекция 2 Реакторы: Введение. Классификация реакторов. Элементы теории химических реакторов.
- Многоликий протон.
- Основные единицы СИ – Тихоокеанский государственный университет.
- Электролит (химия) – это. Что такое электролит (химия)?.
- Какая буква в физике обозначает давление?.