И в руководстве 2017 года, и в руководстве, размещенном на сайте, есть предложение “Не рекомендуется соединять клемму “Вход 0″ и линию заземления” (в руководстве на сайте это предложение приведено в разделе 5.4.1 Подключение датчика).
В новом руководстве действительно есть предложение “Не соединяйте входную клемму с маркировкой “общий” с линией заземления”, но это не имеет никакого отношения к подключению датчиков.
– Что такое кондуктометрические датчики уровня и как они работают?
– Для чего медиакондуктометрия хороша и для чего она не очень хороша.
– Настоящими “спутниками” кондуктометрических датчиков являются сигнализаторы уровня. Регулировка чувствительности своих входов в зависимости от среды
Автор: Алексей Клыков, менеджер по продукции “Датчики уровня”.
- Тонкости проводимости.pdf (669.6 Kb, accessed: 234)
Менеджер по продукции “Датчики температуры”.
- Просмотрщик профиля
- Сообщения форума
- Личное сообщение
- Посмотреть статьи
Кондуктометр ММЗЧ-64. Кондуктометр собран по схеме четырехплечего уравновешенного моста. Он питается переменным током 220 В при 50 Гц через встроенный в устройство генератор. Частота увеличивается до 1150 Гц. Контрольная рука имеет три десятилетия сопротивления. В каждой декаде имеется 9 резисторов, равных 1000, 100, 10 соответственно. Сопротивление опорного плеча можно изменять с шагом 10 Ом от 10 до 10000 Ом. Кондуктометр может измерять сопротивление в диапазоне от 0,01 Ом до 10 кОм. Для компенсации емкостной составляющей используется конденсаторная батарея. Кондуктометр оснащен электрооптическим мостовым индикатором баланса. Погрешность измерения не превышает 1 %.
Кондуктометры
Кондуктометры основаны на проводимости тестируемых растворов.
Электрический ток проходит через растворы электролитов благодаря содержащимся в растворе ионам, которые имеют положительные и отрицательные заряды. Чтобы предотвратить электролиз, для измерения проводимости растворов используется переменный ток.
Проводимость зависит от многих факторов, в частности, от типа вещества, растворителя и концентрации. Измеряя электропроводность, можно определить содержание различных веществ и их соединений в тестовых растворах. Проводимость растворов определяется с помощью кондуктометров различных конструкций путем измерения электрического сопротивления слоя жидкости между двумя электродами, помещенными в исследуемый раствор.
Однако существует возможность непрерывного измерения электропроводности проводящих растворов бесконтактным, индуктивным способом.
Также можно наблюдать изменение проводимости раствора при химическом взаимодействии. В зависимости от принципа измерения эти методы делятся на:
- Прямая электропроводность, основанная на прямом измерении электропроводности раствора одного испытуемого вещества;
- Кондуктометрическое титрование, основанное на измерении электропроводности, которая изменяется при взаимодействии титранта с определяемым веществом в процессе титрования, а содержание вещества оценивается по преломлению кривой титрования, которая строится в следующих координатах: электропроводность – количество добавленного электролита
- Хронокондуктометрическое титрование, которое предполагает определение содержания вещества на основе времени титрования, которое автоматически записывается на графической бумаге регистратора кривой титрования.
В зависимости от метода и области применения существуют различные конструкции измерителей проводимости.
Кондуктометры обеспечивают множество практических применений, включая непрерывный контроль производства. Они используются для мониторинга очистки воды, оценки сточных вод и контроля содержания солей в минеральной, морской и речной воде. Измерение электропроводности является одним из методов контроля качества пищевых продуктов, таких как молоко, вино, напитки и т.д. Часто при анализе смесей электролитов измерение проводимости сочетается с измерением других величин (преломляемость, вязкость, pH, плотность и т.д.).
В некоторых случаях определению электропроводности предшествует химическое взаимодействие. Кондуктометрическое определение различных газов осуществляется таким образом: CO2, CO, O2, NH3, SO2, H2S и т.д. Например, при определении CO2 измеряется проводимость щелочного раствора после поглощения CO2. Этот метод используется при кондуктометрическом определении C, N, O, S и H в органических соединениях, металлах и сплавах.
Принцип работы и конструкция кондуктометра
Проводимость раствора электролита можно определить путем измерения активного сопротивления между погруженными в него электродами. Для измерения сопротивления используется переменный ток, поскольку постоянный ток вызывает электролиз и поляризацию электродов. Источником тока обычно является генератор звуковой частоты.
Сопротивление раствора электролита определяется путем сравнения с эталонным сопротивлением. Для этого используется мост Утстон (рис.1). Сопротивления R1, R2, R3, R4 можно выбрать так, чтобы по диагонали моста не протекал ток, т.е. чтобы сопротивления его ветвей были пропорциональны друг другу. Измеренное сопротивление R4 можно найти по формуле:
R4=R3 R2/R1
Резисторы R1 и R2 выбираются так, чтобы их соотношение было постоянным или поддерживалось неизменным; R3 может варьироваться. Поэтому при балансировке моста отрегулируйте сопротивление R3 и найдите сопротивление R4. В качестве индикаторов нуля используются осциллографы, гальванометры переменного или постоянного тока (после выпрямления) и цифровые вольтметры.
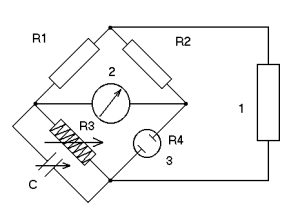
Рис.1. Мост Уитстоуна:
R1, R2, R3, R4- плечи моста; C- переменная емкость; 1- звуковой генератор; 2- индикатор нуля; 3- электролитическая ячейка.
Условия равновесия моста применимы к переменному току, если R1, R2, R3, R4 – активные сопротивления. Однако в мосте переменного тока ток смещения не может быть уменьшен до нуля, поскольку к активному сопротивлению добавляется некоторое реактивное сопротивление, обусловленное емкостью электролитического элемента и цепи.
Электрическая эквивалентная схема электролитической ячейки (рис.2) включает в себя, помимо фактического активного сопротивления раствора R, которое зависит от концентрации ионов и его эквивалентной проводимости, дополнительные активные и пассивные сопротивления, возникающие в ячейке при измерении сопротивления. Электрическая ячейка, т.е. сосуд определенной формы, содержащий электролит с погруженными в него электродами, в принципе может рассматриваться как конденсатор с площадью электродов S, расстоянием между электродами l, заполненный раствором с диэлектрической проницаемостью e. Емкость Cg, которая обратна фактическому сопротивлению электролита в водных растворах, обычно намного выше фактического сопротивления раствора и поэтому не вызывает ошибок в измерениях проводимости. Однако, когда фактическое сопротивление электролита очень велико, эти значения могут быть соизмеримы. Результирующие ошибки уменьшаются с уменьшением частоты тока.
На границе раздела между металлическим электродом и раствором электролита образуется двойной электрический слой. Емкость двойного слоя влияет на сдвиг фаз между током и напряжением, что приводит к ошибкам в измерении фактического сопротивления раствора.
Погрешности измерения могут быть связаны с электрохимическими процессами, происходящими на электродах – ионными разрядами, приводящими к изменению концентрации ионов на поверхности электрода. Вследствие медленной диффузии ионов к электроду возникает концентрационная поляризация, приводящая к поляризационной емкости Cn и поляризационному сопротивлению Rn. Ошибки, связанные с поляризационными явлениями, уменьшаются с увеличением частоты тока и с увеличением концентрации. На частотах выше 1000 Гц влияние поляризации пренебрежимо мало.
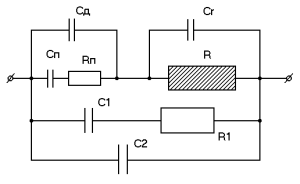
Рисунок 2: Электрическая эквивалентная схема ячейки:
R – сопротивление реального раствора; Cg – геометрическая емкость ячейки; Cd – емкость двойного слоя; Cn и Rn – поляризационная емкость и сопротивление; C1 и R1 – шунтирующая емкость и сопротивление, в зависимости от конструкции ячейки; C2 – емкость провода.
Погрешности измерения также вызваны шунтированием сопротивления R емкостью C1 и сопротивлением R1, что является следствием плохой конструкции ячейки (близкое расположение проводов, выходящих из электродов). Емкость проводников C2 может вызвать емкостную утечку тока.
Кондуктометрические ячейки должны отвечать следующим основным требованиям
- они должны иметь оптимальные геометрические размеры для межэлектродного пространства;
- поляризационные явления на электродах должны быть минимальными;
- утечка тока из-за паразитной емкостной связи должна быть минимальной.
Емкостное сопротивление компенсируется путем подключения конденсатора параллельно резистору R3.
Ошибки из-за поляризационного сопротивления уменьшаются при использовании платиновых электродов, поскольку их увеличенная площадь поверхности снижает плотность тока. Платинированные электроды не следует использовать, если неплатинированная платина влияет на проводимую реакцию или изменяет концентрацию вещества путем поглощения. В некоторых случаях выгодно использовать раскаленные платиновые электроды (серое покрытие). Эти электроды значительно снижают поляризацию, но обладают гораздо худшими поглощающими свойствами.
Прибор для кондуктометрического анализа состоит из электролитической ячейки, звукового генератора, моста Уитстоуна и нулевого индикатора. Для подачи стандартного раствора используется полумикробиурет.
Генераторы ГЗ-1, ГЗ-2, ГЗ-10, ГЗ-33 и т.д. используются для питания системы переменным током. Для работы используется переменный ток частотой 1000 Гц.
В качестве нулевого индикатора можно использовать осциллографический нулевой индикатор. Когда мост будет полностью сбалансирован, эллипс на экране сгладится до горизонтальной линии.
Эти типы устройств характеризуются высокой чувствительностью.
Типы измерителей электропроводности
Проводимость растворов можно измерить с помощью серийно выпускаемых уравновешенных мостов. К таким устройствам относятся P-38, P-556, P-577, P-568 и др. Приведем краткое описание некоторых измерителей электропроводности.
R-38 мостик реохорда. Р-38 широко используется на практике и представляет собой четырехплечий сбалансированный мост со ступенчатой регулировкой плеча сравнения и плавно регулируемым соотношением плеч. Он питается от сети переменного тока 50-500 Гц с напряжением 127 В или 220 В через трансформатор в мостовой схеме. Измеряемое сопротивление может составлять от 0,3 до 30000 Ом. Прибор содержит гальванометр типа M314, который служит в качестве устройства обнуления.
Кондуктометр ММЗЧ-64. Кондуктометр устанавливается в соответствии с четырехплечим сбалансированным мостом. Питание устройства осуществляется переменным током напряжением 220 В и частотой 50 Гц от встроенного в устройство генератора. Это увеличивает частоту до 1150 Гц. Контрольная рука имеет три десятилетия сопротивления. В каждой декаде имеется 9 резисторов, равных 1000, 100, 10 соответственно. Сопротивление опорного плеча можно изменять с шагом 10 Ом от 10 до 10000 Ом. Кондуктометр может измерять сопротивление в диапазоне от 0,01 Ом до 10 кОм. Для компенсации емкостной составляющей используется конденсаторная батарея. Кондуктометр оснащен электрооптическим мостовым индикатором баланса. Погрешность измерения не превышает 1 %.
K-1-4 измеритель электропроводности. Кондуктометр построен по четырехплечей сбалансированной мостовой системе. Он питается переменным током 220 В и частотой 50 Гц от генератора, встроенного в прибор. Частота увеличивается до 1000 Гц. Диапазон измеряемых сопротивлений составляет от 100 до 90 000 Ом. Плечи R1 и R2 представляют собой 100-омные фиксированные сопротивления. Рычаг сравнения представляет собой магазин резисторов типа Р-33. Реактивная составляющая моста сбалансирована. Для балансировки моста используется микроамперметр типа М-495, который через выпрямитель подключается к выходу усилителя. Погрешность измерения находится в пределах 0,5%.
Кондуктометр “Импульс” тип KL-1-2. Кондуктометр “Импульс” предназначен для измерения электропроводности растворов. К прибору прикреплены две ячейки, по которым калибруется шкала прибора. Устройство собрано по мостовой схеме с подачей импульсов переменной полярности и интегрированием синхронно выпрямленного неравновесного сигнала. Точность измерения составляет 0,25 %.
Принцип работы и конструкция бесконтактных измерителей проводимости
Бесконтактные кондуктометры и концентратомеры предназначены для непрерывного измерения электропроводности растворов. Бесконтактные кондуктометры выпускаются в различных исполнениях: погружные, с различной глубиной погружения, и проточные. К таким кондуктометрам, используемым в производстве, относятся БКА-М, КНЧ-1М и другие.
В основе анализатора лежит индуктивный метод измерения проводимости. Анализатор состоит из датчика и измерительного преобразователя. Датчик анализатора обычно изготавливается с такими защитами, как: “искробезопасная электрическая цепь”, “взрывонепроницаемая оболочка” и предназначен для преобразования проводимости в однородный сигнал постоянного тока.
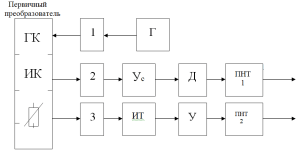
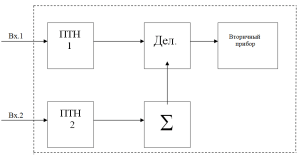
Рис.4. Измерительный преобразователь.
Преобразователь предназначен для преобразования проводимости в однородный сигнал постоянного тока, температурной компенсации и питания постоянным током всех цепей датчика.
Рассмотрим устройство на примере измерителя проводимости потока БКА-М.
Датчик состоит из первичного преобразователя с фланцами для установки на технологическом трубопроводе. Чувствительный элемент и термометр сопротивления, отлитые из пластмассы, расположены в проточной части корпуса первичного преобразователя. На внешней поверхности корпуса находится основание, в котором размещены электронный блок, блок искрозащиты и устройство ввода.
Чувствительный элемент состоит из источника питания (генератора) GC и измерительной тороидальной катушки IR, помещенной в электростатический экран.
Электронный блок анализатора состоит из генератора D, усилителя Us, детектора E и преобразователей напряжение-ток PNT 1 и PNT 2.
Детектор работает следующим образом.
Напряжение переменного тока от генератора через блок искрозащиты 1 подается на силовую катушку GC первичного преобразователя и создает магнитный поток, который наводит ЭДС в контуре гидромуфты, являющейся вторичной обмоткой силовой катушки. Ток в цепи связи пропорционален удельной электропроводности. Изменение тока в цепи связи изменяет ЭДС, наводимую в инфракрасной измерительной катушке. Выходное напряжение первичного преобразователя подается на вход усилителя Us блока искрозащиты. Усиленный сигнал детектируется, фильтруется, подается на вход преобразователя напряжения-тока PNT-1 и по линии связи передается на измерительный преобразователь.
Напряжение с мостовой схемы измерителя температуры IT подается на вход усилителей Y. Усиленное напряжение постоянного тока, пропорциональное температуре анализируемой среды, подается на вход преобразователя напряжения-тока PNT-2 и передается по линии связи на измерительный преобразователь.
Анализатор работает следующим образом.
С одного из выходов преобразователя токовый сигнал, пропорциональный электропроводности, подается на вход преобразователя тока-напряжения ПТН-1, который подключен к одному из входов делителя Деля. Со второго выхода преобразователя токовый сигнал, пропорциональный температуре анализируемой среды, подается на вход преобразователя тока-напряжения ПТН-2, который подключен к входу Σ-а сумматора.
Зависимость удельной электропроводности имеет следующий вид:
Xt = X0 [1 + αt (t – t0)]где
Xt – значение проводимости при текущей температуре, См/м;
X0 – проводимость при начальной температуре, См/м;
αt – температурный коэффициент раствора, град-1;
t0 – начальная температура раствора, град;
t – текущая температура раствора, град.
Для электролитов (солей, кислот и оснований) αt положительна и имеет значение от 0,019 до 0,025.
При повышении температуры раствора его удельная проводимость увеличивается. Чтобы компенсировать это увеличение, выходной сигнал должен быть уменьшен. На входе сумматора устанавливается напряжение, равное
αt (t – t0)
Этот параметр устанавливается на выходе суммирующего устройства
1 + αt (t – t0)
На выходе делителя устанавливается напряжение, пропорциональное
X0 = Xt /[1 + αt (t – t0)]
Которая не зависит от температуры анализируемой среды.
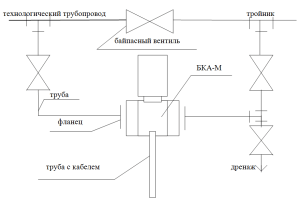
Датчик анализатора устанавливается на обводном трубопроводе технологического трубопровода с помощью фланцевых соединений в горизонтальном положении внутри и снаружи здания. Рекомендуемая схема подключения датчика анализатора показана на рисунке 5.
Кондуктометрическое титрование может быть основано на различных реакциях. Наиболее часто используются кислотно-основные взаимодействия. Например, были разработаны методы определения кислот и оснований в воде с использованием
Главная > Справочное руководство > Химическая энциклопедия:
Кондуктометрия
Кондуктометрия . Кондуктометрия (от conductivity и греческого metreo – измерять), совокупность электрохимических аналитических методов, основанных на измерении электропроводности жидких электролитов, которая пропорциональна их концентрации. Преимущества измерения электропроводности: Высокая чувствительность (нижний предел обнаруживаемой концентрации)
10 -4 -10 -5 М), достаточно высокая точность (относительное отклонение определения 0,1-2%), простые процедуры, легкодоступная аппаратура, возможность тестирования окрашенных и мутных растворов и автоматизация анализа. Кондуктометрические методы могут быть на постоянном или переменном токе, причем последние могут быть как низкочастотными (частота тока 5 Гц), так и высокочастотными (>10 5 Гц). Различают контактную и бесконтактную кондуктометрию, в зависимости от наличия или отсутствия контакта между электролитом и входными цепями измерительного прибора. Наиболее распространенными методами являются низкочастотный контактный метод и высокочастотный бесконтактный метод.
Методы контакта. Измерения проводятся с помощью контактных ячеек (рис. 1, а). Используются электроды из Pt, Ti, нержавеющей стали и т.д. Для измерения растворов с высокой концентрацией электролита (10 -2 -10 -3 М) используются платиновые электроды с развитой поверхностью.
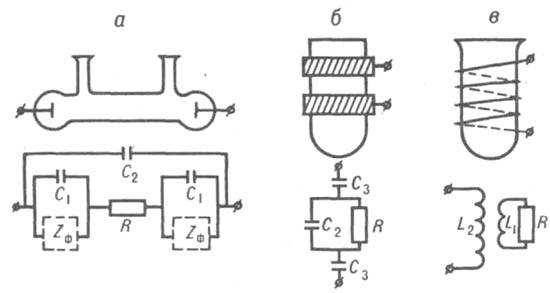
Рис. 1. Кондуктометрические ячейки и эквивалентные электрические схемы: a – контактная ячейка; b – емкостная ячейка; c – индуктивная ячейка; R – сопротивление электролита; С 1 – емкость двойного электрического слоя на границе электрод-электролит; С 2 – емкость раствора; С 3 – емкость конденсатора, образованного раствором, стенкой ячейки и внешним электродом; Z f – импеданс Фарадея, определяемый электрохимической реакцией, происходящей на границе электрод-электролит; L 1 и L 2 – электролит и катушка.
В методе прямой проводимости концентрация электролита определяется непосредственно по значению х его раствора (если между этими величинами существует линейная зависимость). Этот метод в основном используется для анализа разбавленных растворов. В случае концентрированных растворов необходимо построить кривые градиента. Определение веществ в присутствии других электролитов возможно, если концентрация последних постоянна. Метод прямой кондуктометрии является основой для создания солемеров и других кондуктометрических приборов, позволяющих определять содержание олеума и различных солей в минеральной, речной, морской воде, физиологических жидкостях и т.д. Прямая кондуктометрия используется при контроле ионообменных смол, очистке воды, промывке осадка, оценке качества вина, соков и других напитков, чистоты органических растворителей, газов, твердых солей, текстиля, бумаги, зерна, почвы и т.д. Часто образцы для анализа предварительно сжигаются, а выделяющиеся газы поглощаются соответствующими растворами. На основе электропроводности поглотителей определяется количество газов (в частности CO 2 , NO 2 , SO 2 ) и, таким образом, содержание отдельных элементов, например, C, N, S, в металлах, сплавах и органических соединениях.
При косвенном испытании электропроводности смесей электролитов помимо электропроводности растворов измеряют преломляемость, вязкость, pH, плотность и другие величины. Например, при анализе промышленных нитрующих смесей H 2 SO 4 , HNO 3 и H 2 O дополнительно измеряется плотность. На основании всех экспериментальных данных смеси был придан количественный состав.
Кондуктометрическое титрование основано на изменении х-значения раствора в ходе химических реакций, связанных с изменением концентрации ионов различной подвижности. Кондуктометрическое титрование проводится в водной, водно-органической и неводной среде. Кривые титрования, показывающие зависимость x от количества добавленного реагента (титранта), имеют перегиб в точке эквивалентности. При титровании смесей электролитов число преломлений равно числу специфических компонентов, взаимодействующих с титрантом. Форма кривых может быть различной (рис. 2).
Кондуктометрическое титрование может быть основано на различных реакциях. Наиболее часто используются кислотно-основные взаимодействия. Например, были разработаны методы определения кислот и оснований в воде с использованием
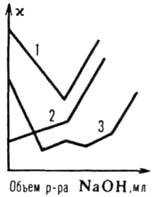
Рис. 2. Кривые кондуктометрического титрования в контактной ячейке с раствором NaOH: 1 – соляная кислота; 2 – CH 3 COOH; 3 – смесь HCl+CH 3 COOH+(C 2 H 5 ) 3 N . HCl + фенол.
pK[10, соли слабых кислот или оснований. При титровании сильных оснований сильными или слабыми кислотами х до эквивалентной точки уменьшается (так что подвижные ионы H+ замещаются менее подвижными катионами титранта) или увеличивается (в результате диссоциации соли), соответственно. С избытком сильного основания после точки эквивалентности (рис. 2, кривые 1 и 2). При титровании солей (до точки эквивалентности изменяется относительно мало, подвижность кондуктометрического титрования замещенных ионов аналогична. Поэтому можно анализировать смеси солей с кислотами или основаниями, содержащие от 2 до 5 компонентов (рис. 2, кривая 3). В кондуктометрических титрованиях, основанных на комплексообразовании, катионы (например, Fe 3+ , Cu 2+ , Pb 2+ , РЗЭ) титруют этилендиаминтетраацетатом Na, а также тартрат-, оксалат-, цитрат-, цианат-ионами и т.д. Реакции осаждения используются для кондуктометрического определения как анионов, так и катионов. Например, растворы СІ- , Вr- , I- , CN- , Ba(ОСОСН 3 ) 2 или ВаСІ 2 -SO 2- , Сr 4 2- , Th(NO 3 ) 3 -F – , SiF 6 2- , Na 2 SeO 3 -Mn 2+ , Co 2+ . Кондуктометрические методы титрования, основанные на окислительно-восстановительных реакциях, используются редко.
В так называемом хронокондуктометрическом титровании раствор титранта вводится в реакционный сосуд (электрохимическую ячейку) с постоянной скоростью, так что время титрования пропорционально количеству добавленного титранта. Концентрация определяется по электропроводности раствора и времени титрования. Кривые обычно записываются автоматически. Все определения, выполненные обычным методом измерения электропроводности, могут быть также выполнены хронокондуктометрически.
Контактные методы очень точны. Они используются не только для химического анализа, но и для изучения кинетики реакций, определения констант диссоциации электролитов, растворимости осадков, коэффициентов диффузии и т.д.
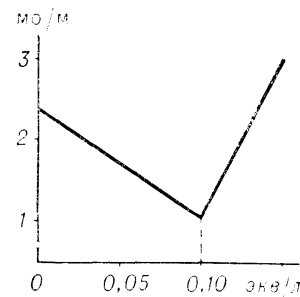
Бесконтактные методы. Используется для измерения относительной проводимости, в основном для высокочастотного титрования. Измерения проводятся с помощью емкостных (C-) или индуктивных (L-) ячеек, которые представляют собой соответственно диэлектрические сосуды с по меньшей мере двумя металлическими электродами снаружи (рис. 1b) или помещенные в магнитное поле индукционной катушки (рис. 1c). Электроды ячейки C или индукционной катушки подключены к генератору высокой частоты. Проводимость электролита под действием высокочастотного тока обусловлена не только действительным движением заряда, но в большей степени потерей электрической энергии в емкостных и индуктивных элементах. Это отражается в реактивной составляющей X импеданса цепи Z 2 = R 2 + X 2 , где R – активный импеданс, X=X L – X C, X L и X C – соответствующие индуктивное и емкостное сопротивления цепи. Индуктивные ячейки обычно используются для измерения относительно высокой проводимости, а емкостные – для измерения низкой проводимости. Чувствительность повышается в C-клетках за счет использования диэлектриков с высокой диэлектрической проницаемостью, уменьшения толщины стенки сосуда и увеличения площади электрода, а в L-клетках – за счет увеличения объема образца. Также используются комбинации LC-элементов, RC-элементов и RL-элементов с повышенной чувствительностью и многоэлементные системы с различным количеством электродов в петлях сдвига фазы генератора. Для высокочастотного титрования условия должны быть предварительно подобраны с учетом характеристик ячейки, т.е. зависимости 1 /X L или 1 /X C от x (рис. 3). Чем больше интервал между (:0 и (. в котором эта зависимость линейна, тем удобнее ячейка для измерений. Кроме того, чувствительность измерений варьируется в различных частях характеристической кривой; например, для кривой 1 чувствительность наименьшая в точке максимума и наибольшая в точках перегиба.
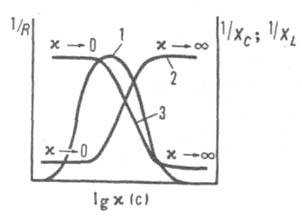
Рисунок 3: Характеристические кривые бесконтактных высокочастотных ячеек: 1,2,3 – зависимость обратных значений соответствующих активных, емкостных и индуктивных составляющих Z от lg(.
Кривые высокочастотного титрования имеют минимум (как кривая 1 на рис. 2) или максимум, а также могут быть М-образными кривыми. Бесконтактные методы уступают контактным методам по точности, но превосходят их по чувствительности. Кроме того, благодаря отсутствию взаимодействия между материалом электрода и тестовой средой, эти методы позволяют проводить измерения при высоких и низких температурах, в агрессивных средах и в замкнутом пространстве. Применяются для кислотно-основного титрования против различных растворителей (СН3 СООН, ацетон, диоксан и т.д.), обнаружения веществ в хроматографии, экспресс-анализа органических соединений, воздуха и промышленных газов, химического анализа. реагентов, контроля качества препаратов в закрытых ампулах, для изучения комплексообразования, гидролиза, сольватации, фазовых переходов.
Лит. по Т.А.Худякова и А.П.Крешков, Теория и практика кондуктометрического и хронокондуктометрического анализа, М., 1976; Б.А.Лопатин, Высокочастотное титрование с многозвенными ячейками, М., 1980; М.С.Грилихес и Б.К.Филановский, Контактная кондуктометрия, Л., 1980. по Т.А. Худякова. Б.К. Филановский. М.С. Грилихес.
С помощью различных методов С. определяется содержание солей в минеральных водах, контролируются процессы водоподготовки и качество воды, определяются вредные примеси в молоке, винах, фруктовых соках и т.д. Кондуктометрическое титрование используется для анализа алкалоидов, барбитуратов и других лекарственных препаратов в химико-фармацевтической промышленности, для наблюдения за ферментными реакциями и для определения концентрации различных соединений и элементарных ионов, которые являются субстратами или кофакторами ферментов. Использование прямого C. Анализ биолитической жидкости используется для определения нарушений водно-солевого баланса (см.) в организме, для контроля за ходом процессов диализа, опреснения белков, адсорбции различных ионов на твердых осадителях (сорбентах) и др. С. является основой для специальных тестов (например, С=N-гидролазный тест при беременности, тест “индекс деградации” для дифференциальной диагностики некоторых заболеваний, гепариновый тест при ревматизме и т.д.). Методы С. могут быть использованы для изучения механизма свертывания крови, гемагглютинации и других процессов, происходящих в тканях, сосудах и различных органах.
КОНДУКТОМЕТРИЯ
Кондуктометрия (Кондуктометрия – это электрохимический метод анализа, основанный на измерении электропроводности жидкостей (включая биологические среды). Электропроводность жидких сред является характеристикой их физического состояния и химических свойств. Проводимость может быть зарегистрирована в автоматическом режиме с высокой точностью (погрешности измерений не превышают сотых долей процента). Таким образом, кондуктометр может быть использован в качественном и количественном анализе различных химических веществ, в гематологических исследованиях, в исследованиях водно-солевого обмена, кислотно-основного баланса в организме и т.д. (см. Электропроводность биологических систем).
При постоянной концентрации и температуре электропроводность (L) слоя жидкости между двумя электродами прямо пропорциональна площади поверхности электродов (S) и обратно пропорциональна расстоянию (d) между ними: L = k (S/d). Коэффициент пропорциональности k называется удельной проводимостью: k = L, если S = 1 и d = 1. В системе СИ проводимость выражается в обратных омах (Мо) или симах (См), единицей проводимости является 1 Ом -1 -м -1 . Молярная (μ), эквивалентная (λ) и ионная (λ-λ+) проводимости часто используются для представления электропроводности р-ров, содержащих 1 г-моль, 1 г-кв вещества и 1 г-ион соответственно: λ = kVN, где VN – объем р-ра, содержащего 1 г-кв электролита; VN = 1/C, где СN – нормальная концентрация.
Впервые (1879) электропроводность серии растворов была измерена Кольраушем (F. Kohlrausch), который предложил использовать для этой цели мост Уитстона, питаемый переменным током, и электролитическую ячейку с плоскопараллельными электродами. Однако широкое использование методов электропроводности началось только в 20 веке в связи с общим прогрессом в электронике, автоматизации, электрохимии и т.д. Современная промышленность выпускает множество типов приборов для измерения электропроводности для различных целей. В зависимости от принципа действия их датчиков, эти приборы можно разделить на две группы: приборы с контактными и бесконтактными датчиками проводимости.
Контактные преобразователи проводимости (R-ячейки, контактные датчики и т.д.), несмотря на различия в конструктивных особенностях, имеют один общий базовый элемент – погруженные в тестируемую жидкость электроды, через которые во время работы протекает электрический ток. Зафиксирован процесс, происходящий на границе раздела электрод-жидкость. Источником рабочего напряжения является низкочастотный генератор (до 1000 Гц). Преимуществом этих методов является возможность измерения с высокой точностью и возможность получения прямого показания измеряемой величины при соответствующей калибровке прибора. Недостатком являются поляризационные явления, которые особенно проявляются в концентрированных растворах.
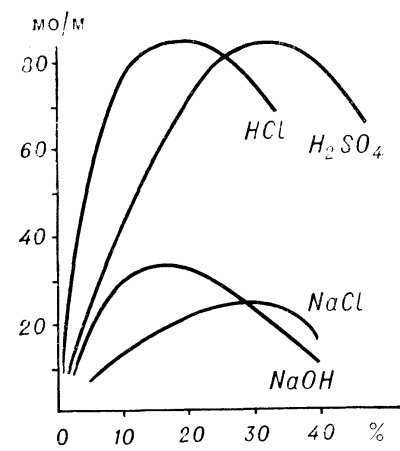
Бесконтактные датчики проводимости регистрируют не процессы, происходящие на границе раздела электрод-жидкость, а электрохимические свойства всей системы, заключенной между электродами. Используются токи низкой (до 20 кгц), высокой (до 100 МГц) и сверхвысокой (>100 МГц) частоты. Поэтому высокочастотные методы используются в качестве косвенных методов, например, в кондуктометрическом титровании. Преимущество этих методов в том, что они могут измерять проводимость концентрированных, агрессивных и летучих жидкостей, и нет взаимодействия между электродами и исследуемым веществом. В высокочастотном титровании используются два типа ячеек (емкостные и индуктивные). В емкостных ячейках тестируемый раствор соединен электрическим полем с опорной цепью прибора. Емкостные ячейки используются для тестирования электролитов с концентрацией до 0,4 М. При более высоких концентрациях используются индуктивные ячейки с магнитной связью. Различают методы прямого и кондуктометрического титрования. При прямом титровании концентрация любого вещества в растворе определяется по значению электропроводности. Концентрация электролита рассчитывается непосредственно с помощью калибровочной кривой, которая строится для каждого из определяемых веществ (рисунок 1). В кондуктометрическом титровании (см. “Кондуктометрическое титрование”). Анализ титрования) количество вещества (титранта), добавленного к исследуемой жидкости, определяется по наклону кривой электропроводности в процессе титрования (рис. 2). Погрешность измерения при кондуктометрическом титровании обычно составляет менее 0,02%. Разновидностью кондуктометрического титрования является хронокондуктометрическое титрование, при котором вещества количественно определяются на основе времени, необходимого при определенных условиях для титрования.
Различные методы C. используются для определения содержания соли в минеральных водах, контроля процессов очистки воды и ее качества, определения вредных примесей в молоке, вине, фруктовых соках и т.д. Кондуктометрическое титрование используется для анализа алкалоидов, барбитуратов и других лекарственных препаратов в химико-фармацевтической промышленности, для наблюдения за ферментативными реакциями и для определения концентрации различных соединений и элементарных ионов, которые являются субстратами или кофакторами ферментов. Биолитические жидкости исследуют при прямой С. с целью определения нарушений водно-солевого баланса (см.) в организме, для контроля за ходом процессов диализа, обессоливания белков, адсорбции различных ионов на твердых осадителях (сорбентах) и др. C. является основой для специальных тестов (например. C=N-гидролазный тест при беременности, тест “индекс деградации” для дифференциальной диагностики некоторых заболеваний, гепариновый тест при ревматизме и др.) Методы С. могут быть использованы для изучения механизма свертывания крови, гемагглютинации и других процессов в тканях, сосудах и различных органах.
Библиография: Андреев В. С. П. Жуков и М. В. Кулаков, Высокочастотная безэлектродная кондуктометрия, Москва, 1968; Лопатин Б.А., Кондуктометрия, Новосибирск, 1964; Худякова Т.А. и Крешков А.П., Теория и практика кондуктометрического и кондуктометрического анализа, Москва, 1976, библиография; Purdy W. C. Электроаналитические методы в биохимии, N. Y., 1965.
Рисунок 2: Сигнализация одного и того же уровня жидкости в разных резервуарах
Кондуктометрический метод измерения уровня
В современных системах автоматизации различают следующие методы измерения уровня: поплавковый, кондуктометрический, гидростатический, ротационный, емкостной, вибрационный и радарный. Каждый из этих методов измерения имеет свои специфические характеристики. В качестве примера классификации датчиков уровня возьмем датчики уровня OVEN.
Текущий ассортимент датчиков уровня, предлагаемых компанией OWEN, обеспечивает следующие методы измерения уровня:

Метод электропроводности

Метод поплавка

Гидростатический метод

Ротационный метод
Функциональная классификация
Датчики уровня можно разделить на две большие группы в соответствии с их функциями:
- Сигнальные устройства.
- Показатели уровня.
Сигнальщики – Это устройства, предназначенные для обнаружения заранее определенного уровня. Датчики подают сигнал, когда уровень достигает заданного значения.
Показатели уровня – это датчики, предназначенные для непрерывного измерения уровня в реальном времени. Они состоят из измерительной части с датчиками.
Данные от измерительной части обрабатываются аналоговой или цифровой электроникой, входящей в состав датчика. Обычно это выходной сигнал 4 … 20 мА или RS-485.
Методы измерения
Множество методов измерения уровня включает как дорогие, так и дешевые датчики. Как правило, каждый датчик имеет свой собственный метод измерения со своими характеристиками.
Наиболее распространенным методом измерения уровня является кондуктометрический метод.
Кондуктометрический метод является самым простым и экономически эффективным способом измерения уровня жидкости. Этот метод актуален только для уровневых показателей.
Датчики проводимости основаны на измерении сопротивления (проводимости) жидкости между общим электродом и сигнальным электродом, которое зависит от уровня контролируемой жидкости. Длина общего электрода должна быть максимальной по отношению к сигнальному электроду, а его рабочая часть должна находиться в постоянном контакте с жидкостью.
Рис. 1 Принцип работы датчиков электропроводности
Кондуктометрический метод измерения подходит только для проводящих жидкостей.
Недостатком этого метода является несовместимость с клеящими и диэлектрическими веществами. Остатки клея, налипшие на электроды, могут вызвать ложные срабатывания. Диэлектрики, с другой стороны, при достижении определенного уровня вообще не проводят электричество.
Кондуктометрические датчики уровня используются для определения уровня жидкости в металлических и неметаллических резервуарах.
Когда датчик проводимости используется для контроля уровня жидкости в неметаллических резервуарах, один электрод является общим, в то время как в металлических резервуарах стенка резервуара выступает в качестве общего электрода.
Рис. 2. Обнаружение уровня жидкости в различных резервуарах
Датчики электропроводности OMEN
Детекторы проводимости используются для контроля одного или нескольких уровней проводящих жидкостей, а также для защиты от переполнения резервуаров и защиты насосов от сухого хода.
К проводящим жидкостям относятся вода, пищевые продукты, соль, растворы кислот и щелочей.
Мы представляем серию датчиков электропроводности OVEN вместе с их основными техническими характеристиками.
Электролиты – это вещества, молекулы или кристаллы которых диссоциируют на ионы либо под действием молекул растворителя, либо под действием тепла (диссоциация).
Кондуктометрический метод анализа
Кондуктометрические измерения начались еще в 18 веке, когда Андреас Баумгартнер заметил, что соль и минеральные воды из Бад Гаштайна в Австрии проводят электричество. Таким образом, использование этого метода определения чистоты воды, который сегодня часто применяется для проверки эффективности систем очистки воды, началось в 1776 году. Так началась история кондуктометрического метода анализа.
Фридрих КольраушОн развил эту науку в 1860 году, когда применил переменный ток к воде, кислотам и другим растворам. Примерно в то же время Уиллис Уитни, изучавший взаимодействие серной кислоты с комплексами сульфата хрома, нашел первую кондуктометрическую конечную точку. Эти открытия привели к потенциометрическому титрованию и созданию первого прибора для объемного анализа Робертом Берендом в 1883 году при титровании хлорида и бромида HgNO.3. Современный кондуктометрический метод анализа был разработан Берендом
Кондуктометрический метод анализа основана на измерении электропроводности растворов и ее зависимости от концентрации.
Его можно использовать для определения концентрации солей, кислот и оснований, а также для проверки концентрации промышленных растворов.
-Низкочастотное кондуктометрическое титрование
-Высокочастотное кондуктометрическое титрование
· Теоретическая основа метода
Проводники электрического тока делятся на:
-Проводники типа 1 – это металлы, обладающие электронной проводимостью
– Проводники второго типа – это электролиты с ионной проводимостью
Электролиты – это вещества, молекулы или кристаллы которых диссоциируют на ионы под воздействием молекул растворителя или тепла (диссоциация).
Проводники второго рода рассматриваются в кондуктометрии.
Закон Ома применим как к электролитам, так и к металлам:
– Ток в проводнике прямо пропорционален напряжению на его концах (разности потенциалов) и обратно пропорционален сопротивлению проводника.
Где: I – ампер тока, A
U- разность потенциалов между электродами
R – сопротивление проводника, Ом.
Электрическое сопротивление – это основная константа, характеризующая электрические свойства вещества
R = p 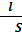 ,
,
l – длина (расстояние между электродами), м
S – площадь поперечного сечения проводника, м 2, см 2
p удельное сопротивление, Ом*см/см 2 Удельное сопротивление – это сопротивление столбика материала длиной 1 см и площадью поперечного сечения 1 см2.
Единицей электропроводности является siemens,cm
1 сиэм – это электропроводность проводника, находящегося под напряжением в
напряжение 1 В при токе 1 А
Электропроводность (W) – это величина, обратная электрическому сопротивлению проводника (R).
W = 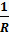
Величина, обратная удельному электрическому сопротивлению, называется проводимостью.
Электропроводностьравна электропроводности 1м3 раствора, помещенного между параллельными электродами площадью 1м2 и расстоянием между ними 1м.

Эквивалентная проводимость используется для качественной и количественной характеристики растворов
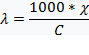
Эквивалентная электропроводность – это электропроводность раствора электролита толщиной 1 м, помещенного между одинаковыми электродами с площадью поверхности такой, что объем жидкости между ними содержит 1 моль химический эквивалент растворенного вещества.
Эквивалентная проводимость измеряется в См ∙ моль -1 ∙ м 2 или Ом -1 ∙ моль-1 ∙ м 2 . В учебниках часто дается эквивалентная проводимость в единицах см ∙ моль -1 ∙ см 2 или Ом -1 ∙ моль -1 ∙ см 2. (Здесь проводимость ϰ выражается в Ом -1 ∙ см -1 или См ∙ см -1 , C – молярная концентрация эквивалента в моль/см 3).
· Закон Кольрауша
В бесконечно разбавленном растворе эквивалентная проводимость достигает предела и не зависит от концентрации. Это объясняется тем, что в растворах слабых электролитов происходит полная диссоциация (α==1), а в растворах сильных электролитов исчезает межионное взаимодействие.

Эквивалентная электропроводность бесконечно разбавленных растворов (λ∞) называется предельной проводимостью
Кольрауш обнаружил, что в таком разбавлении катионы и анионы проводят ток независимо друг от друга, поскольку между ними нет сил взаимодействия. В этом случае эквивалентная электропроводность раствора будет равна сумме электропроводностей катионов (λk) и анионов (λa)
Из этого закона для любого раствора известной концентрации можно вычислить следующее
Значения ионной подвижности приведены в справочной литературе
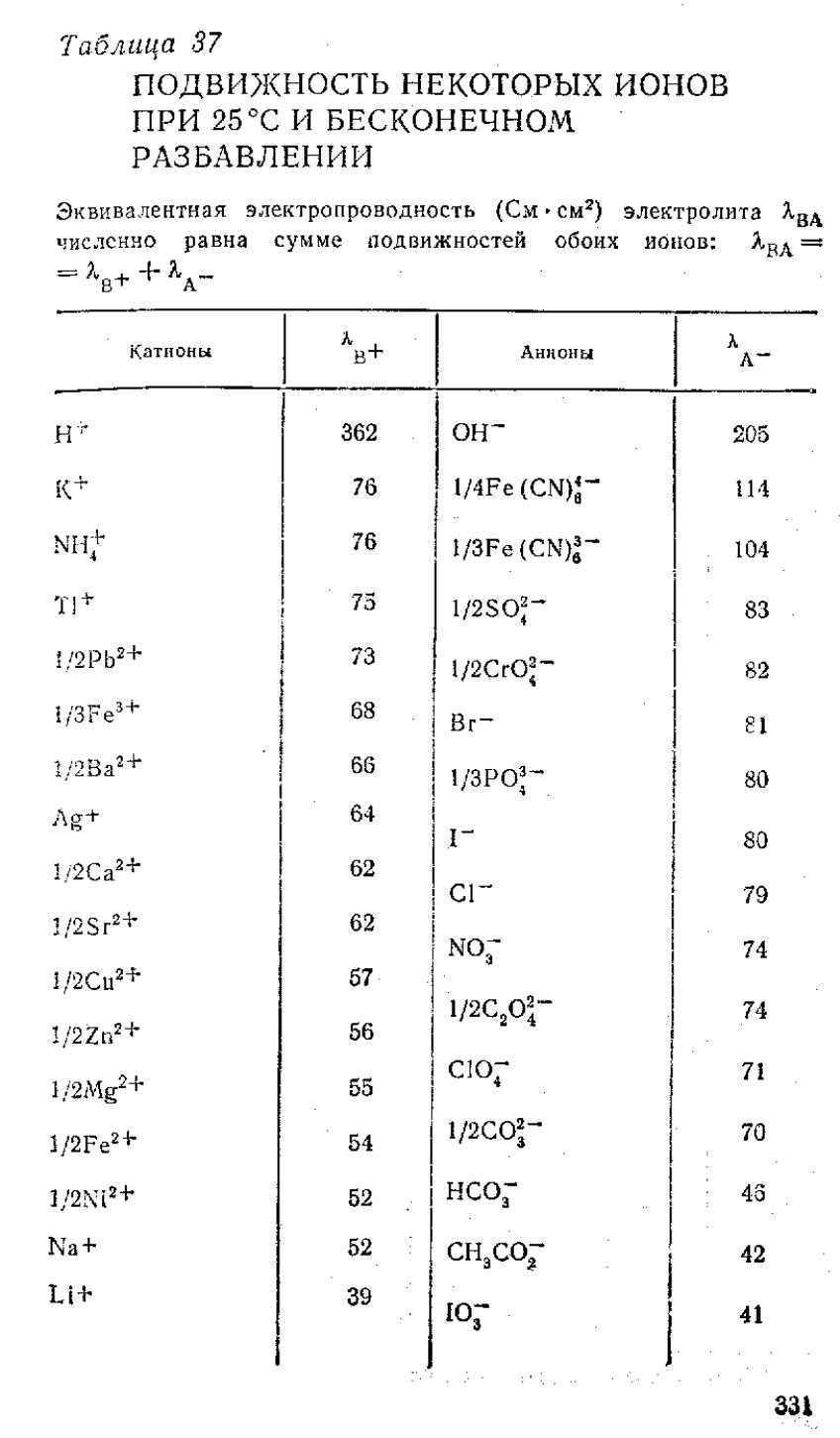
Электропроводность раствора зависит от:
-Природа вещества
Концентрационная зависимость проводимости электролитов
Из эквивалентного значения электропроводности можно рассчитать следующее:
-растворимость веществ и других количеств
· измерение электропроводности
Прибором для измерения сопротивления, а значит и проводимости, является мост Уитстоуна в аппарате Кольрауша.
Измерители проводимости – измерители проводимости
Принцип работы этих приборов основан на проводимости анализируемых растворов, т.е. на кондуктометрическом методе. Используется измерительная ячейка, состоящая из двух электродов, помещенных в анализируемый раствор на определенном расстоянии друг от друга. Сопротивление ячейки зависит только от проводимости раствора. 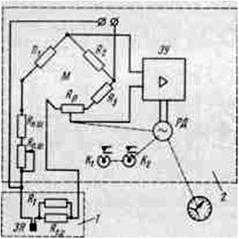
Принципиальная схема кондуктометра
Прибор состоит из двух основных компонентов – преобразователя (1) и измерительного устройства (2).
Преобразователь содержит электрохимическую ячейку EH, термокомпенсирующее сопротивление Rt. s и шунтирующее сопротивление RT для регулирования цепи.
Измерительное устройство, сбалансированный мост переменного тока, содержит мостовую схему M, электронный усилитель EU и реверсивный двигатель RD, воздействующий на реохордный движок Rv.
Резисторы RH.w и Rn.w используются для настройки во время работы. Принцип работы прибора заключается в следующем. Изменение концентрации раствора вызывает изменение сопротивления между электродами измерительной ячейки EJ, что размыкает мост, и на входе усилителя появляется сигнал, пропорциональный изменению концентрации раствора. Усиленный сигнал активирует реверсивный двигатель RD, который перемещает ползунок реохорда для устранения дисбаланса. Контакты K1 и K2 сигнализируют о максимальном и минимальном значениях концентрации раствора.
Читайте далее:- Кондуктометр или EC-метр для анализа питательного раствора.
- Электролит (химия) – это. Что такое электролит (химия)?.
- Как работает pH-электрод.
- Измерительный инструмент – это инструмент для измерения. Что такое измерительный инструмент?.
- Что такое электродный потенциал; Школа для инженеров-электриков: электротехника и электроника.
- Датчики уровня электропроводности – конструкция и принцип работы; Школа электротехники и электроники.
- ROMB-5 – Емкостное устройство защитной сигнализации.