где заряд частицы равен: , потому что i-частица – это ядро атома гелия, которое состоит из двух протонов и двух нейтронов, , потому что мы будем считать, что эксперимент проводится на воздухе.
Заряд ядра атома определяет положение элемента в периодической таблице Менделеева, а следовательно, и химические свойства вещества, состоящего из этих атомов и соединений этих веществ. Величина заряда ядра равна:
![]()
где Z – номер элемента в таблице Менделеева, e – величина заряда электрона или ![]() .
.
Элементы, имеющие одинаковый номер Z, но разные атомные массы, называются изотопами. Если элементы имеют одинаковые Z-числа, их ядра имеют одинаковое количество протонов, но если их атомные массы различны, количество нейтронов в ядрах атомов различно. Например, водород имеет два изотопа – дейтерий и тритий.
Ядра атомов имеют положительный заряд, поскольку состоят из протонов и нейтронов. Протон – это стабильная частица, принадлежащая к классу адронов, которая является ядром атома водорода. Протон – это положительно заряженная частица. Его заряд равен по модулю элементарному заряду, который является величиной заряда электрона. Заряд протона часто обозначается через ![]() можно написать, что:
можно написать, что:
![]()
Масса покоя протона (![]() ) приблизительно равна:
) приблизительно равна:
![]()
Подробнее о протоне см. в разделе “Заряд протона”.
∆Дельта M(Z, A) = Zm_p + (A-Z)m_n – M(Z, A)” width=”” height=”” />,
Содержание
В 1911 году Резерфорд в своем докладе “Рассеяние α- и β-лучей и структура атома” в Философском обществе Манчестера заявил [4] :
Рассеяние заряженных частиц можно объяснить, если предположить такой атом, который состоит из центрального электрического заряда, сосредоточенного в точке и окруженного равномерным сферическим распределением противоположных электрических зарядов одинакового размера. При такой структуре атома α- и β-частицы, проходящие на небольшом расстоянии от центра атома, испытывают большое отклонение, хотя вероятность такого отклонения мала.
Таким образом Резерфорд открыл атомное ядро, что положило начало ядерной физике, то есть изучению структуры и свойств атомных ядер.
После открытия стабильных изотопов элементов ядру самого легкого атома была отведена роль структурной частицы всех ядер. С 1920 года ядро атома водорода носит официальное название протон. После промежуточной протонно-электронной теории строения ядра, которая имела много очевидных недостатков, в частности, противоречила экспериментальным результатам измерений спинов и магнитных моментов ядер [5], в 1932 году Джеймс Чедвик открыл новую электрически нейтральную частицу, названную нейтроном. В том же году Иваненко [6] и независимо Гейзенберг выдвинули гипотезу о протон-нейтронной структуре ядра. Эта гипотеза была полностью подтверждена всем последующим развитием ядерной физики и ее приложений [7] .
Число нейтронов в ядре равно N = A – Z . Для обозначения ядер используется символ X Z A, где X определяется как химический символ элемента.
Энергия связывания. Дефект массы ядер
Величина ∆ m , определяющая разность масс между массой нуклонов, образующих ядро, и массой ядра, называется дефект массы ядра..
Важная информация о свойствах ядра может быть получена даже в отсутствие знания деталей взаимодействий между нуклонами ядра, исходя из закона сохранения энергии и закона пропорциональности массы и энергии. Поскольку каждое изменение массы ∆ m вызывает соответствующее изменение энергии ∆ E ( ∆ E = ∆ m c 2 ), при создании ядра выделяется определенное количество энергии. Из закона сохранения энергии можно сделать вывод, что точно такое же количество энергии необходимо для разделения ядра на составные части, другими словами, для отделения нуклонов друг от друга на такое расстояние, чтобы между ними не происходило никакого взаимодействия. Эта энергия называется энергией связи ядра.
Следует отметить, что эта формула довольно неудобна в применении, так как в таблицах приводятся массы, относящиеся к массам нейтральных атомов, а не к массам ядер. По этой причине для удобства расчетов формула преобразуется так, чтобы в нее входили массы ядер, а не массы атомов. Для этого мы будем складывать и вычитать массу Z электронов ( m e ) в правой части формулы. В этом случае E c in = Z m p + m e + A – Z m n – m a + Z m e c 2 = Z m H 1 1 + A – Z m n – m a c 2 – масса атома водорода, m a – масса атома.
В ядерной физике энергия часто выражается в мегаэлектронвольтах (М эВ). Когда речь идет о практическом применении ядерной энергии, она измеряется в джоулях. Если сравнивается энергия двух ядер, то используется единица массы энергии – отношение массы к энергии (E = m c 2 ). Единица массы энергии ( l e ) равна энергии, которая соответствует массе одного а . м . Это равно 931,502 М е В .
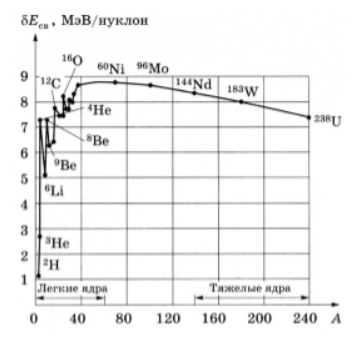
Помимо энергии, важны следующие факторы удельная энергия связи ядра – энергия связи на нуклон: ω = E c в / A . Оно изменяется относительно медленно по сравнению с изменением массового числа A , принимая почти постоянное значение 8. 6 M e B в центральной части периодической таблицы и уменьшается к ее краям.
Все упомянутые в подзаголовке свойства, вместе с E c , усиливаются в периоде с увеличением атомного заряда, в группе с увеличением атомного заряда они ослабевают. Таким образом, самым электроотрицательным элементом в правом верхнем углу таблицы Д.И. Менделеева является фтор.
Периодический закон
Периодический закон был изобретен Д.И. Менделеевым в 1868 году. Его современная формулировка: свойства химических элементов и образуемых ими соединений (простых и сложных) находятся в периодической зависимости от величины заряда атомного ядра.
Периодический закон лежит в основе современного учения о строении материи. Периодическая таблица Д. Менделеева – это наглядное представление периодического закона.
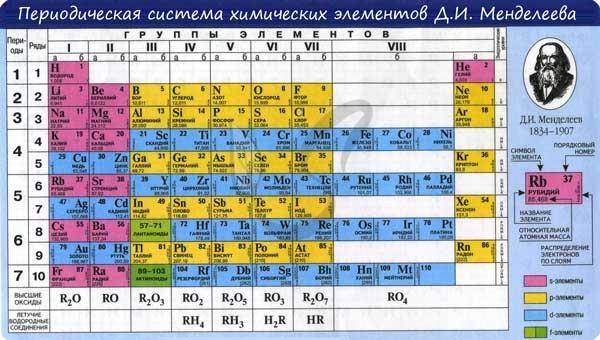
В периодической таблице элементы расположены в порядке возрастания атомного заряда, сгруппированы в “ряды и столбцы” – периоды и группы.
Период – это ряд химических элементов, расположенных горизонтально. Периоды 1, 2 и 3 называются минорными периодами, они состоят из одного ряда элементов. Периоды 4, 5, 6 называются основными периодами, они состоят из двух рядов химических элементов.
Группа – это вертикальный ряд химических элементов в периодической таблице. Элементы расположены по группам в зависимости от степени их окисления в высшем оксиде. Каждая из восьми групп состоит из главной подгруппы (a) и побочной подгруппы (b).
Периодическая таблица Д. Менделеева дает огромное количество ответов на различные вопросы. При умелом использовании вы сможете угадывать строение и свойства веществ, успешно записывать химические реакции и решать задачи.
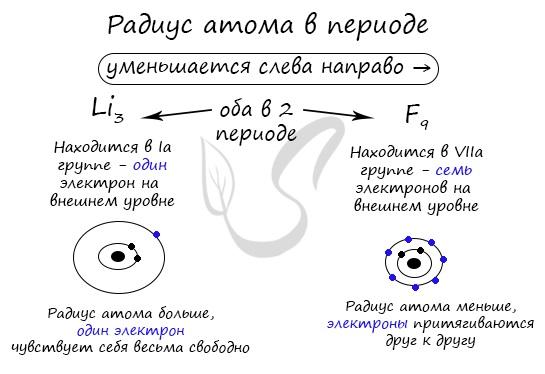
Атомный радиус
Радиус атома – это расстояние между атомным ядром и самой удаленной электронной орбиталью. Это не явная, а концептуальная граница, которая указывает на наиболее вероятное положение электрона.
В периоде радиус атома уменьшается по мере увеличения номера группы элементов (‘→’ слева направо). Это происходит потому, что с увеличением номера группы увеличивается число электронов на внешнем уровне. Помните, что для элементов главных подгрупп номер группы равен числу электронов на внешнем уровне.
По мере увеличения числа электронов они становятся более тесными, так как сильнее притягиваются друг к другу: в этом причина малого радиуса атома.
Чем меньше электронов, тем больше у них свободы и тем больше радиус атома, поэтому радиус увеличивается в периоде “←” справа налево.
В группе радиус атома увеличивается с ростом заряда атомных ядер – сверху вниз “↓”. Чем больше период, тем больше электронных орбиталей вокруг атома, и, следовательно, тем больше радиус.
По мере уменьшения заряда атома в группе уменьшается и его радиус – снизу вверх “↑”. Это связано с уменьшением числа электронных орбиталей вокруг атома. Возьмем для примера атомы бора и алюминия, элементов, относящихся к одной группе.
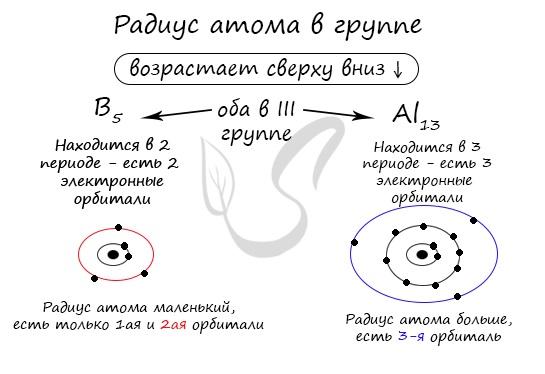
Период, группа и электронная конфигурация
Отметим еще раз важную деталь: элементы одной группы (главной подгруппы!) имеют схожую конфигурацию внешнего уровня. Так, бор имеет 3 электрона на внешнем уровне, и алюминий также имеет 3 электрона на внешнем уровне. Они оба относятся к группе III.
Такая формула иногда может сильно облегчить жизнь, но ее не существует для элементов вторичных подгрупп – там приходится считать электроны “вручную”, размещая их на электронных орбиталях.
- B5 – 1с 2 2с 2п 1
- Аль13 – 1s 2 2s 2 2p 6 3s 2 3p 1
Общая электронная конфигурация для элементов III группы главной подгруппы может быть записана как ns 2 np 1 . Это работает для бора, внешний уровень которого 2s 2 2p 1 , алюминия – 3s 2 3p 1 , галлия – 4s 2 4p 1 , индия – 5s 2 5p 1 и таллия – 6s 2 6p 1 . Мы принимаем “n” за номер периода.
Правило электронной конфигурации, которое вы только что видели, является универсальным. Если вы имеете дело с элементом из главной подгруппы, то, посмотрев на номер группы, вы узнаете, сколько электронов у него на внешнем уровне. Посмотрев на период, вы узнаете номер его внешнего уровня.
Просто разделите известное число электронов на s- и p-элементы, затем подставьте номер периода – и вот вы быстро получите конфигурацию внешнего уровня. Я предлагаю вам посмотреть на пример ниже 
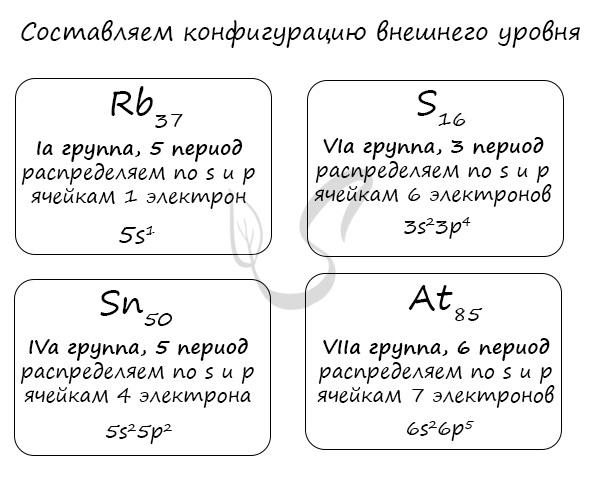
Я очень надеюсь, что теперь вы знаете: просто взглянув на положение элемента в периодической таблице, на группу и период, в которых он находится, уже можно составить конфигурацию его внешнего уровня. Разумеется, это относится к элементам основных подгрупп. Повторяю: для мелких – только “вручную”.
длина связи
Длина связи – это расстояние между атомами химически связанных элементов. Очевидно, что понятия длины связи и атомного радиуса напрямую связаны. Чем больше атомный радиус, тем больше длина связи.
Мы увидим это, сравнив длины связей в четырех веществах: HF, HCl, HBr, HI.
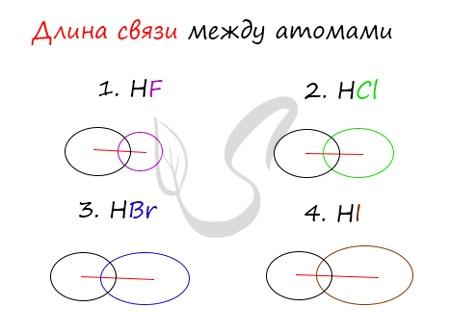
Чем больше радиусы атомов, образующих химическую связь, тем больше длина связи между ними. Радиус атома водорода постоянен во всех трех веществах, а в ряду F → Cl → Br → I происходит увеличение радиуса атома. Йод имеет самый большой радиус, поэтому у него самая длинная связь в молекуле HI.
Металлические и неметаллические свойства
В периоде с увеличением заряда атома металлические свойства становятся слабее, а неметаллические – сильнее (слева направо “→”). В группе с увеличением атомного заряда металлические свойства становятся сильнее, а неметаллические – слабее (сверху вниз “↓”).
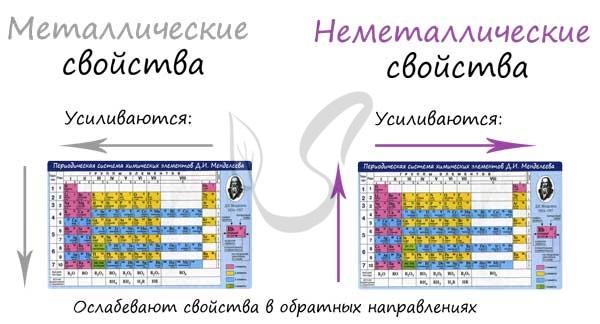
Давайте сравним металлические и неметаллические свойства Rb, Na, Al, S. Натрий, алюминий и сера находятся в одном периоде. Металлические свойства увеличиваются S → Al → Na. Натрий и рубидий находятся в одной группе, металлические свойства увеличиваются Na → Rb.
Таким образом, рубидий обладает самыми сильными металлическими свойствами, но, с другой стороны, имеет самые слабые неметаллические свойства. Сера обладает самыми слабыми металлическими свойствами, но если посмотреть на это с другой стороны, то сера – самый сильный неметалл.
Распределение металлов и неметаллов в периодической таблице также является четким отражением этого принципа. Если провести условную линию, идущую от бора к астатину, то справа окажутся неметаллы, а слева – металлы.
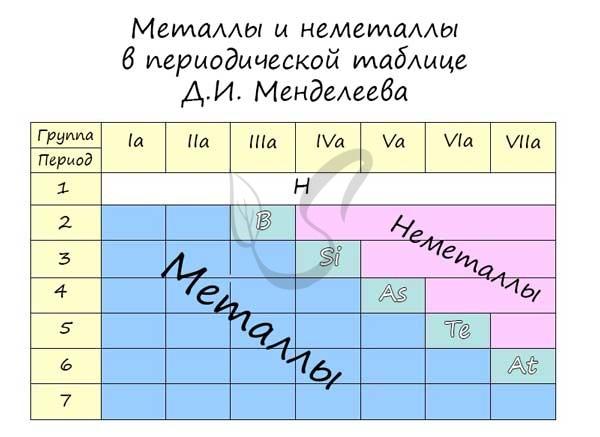
Щелочные и кислотные свойства
Щелочные свойства уменьшаются с увеличением заряда атома в данном периоде, кислотные свойства увеличиваются с увеличением заряда атома. В группе основные свойства увеличиваются с ростом заряда атома, а кислотные свойства уменьшаются с ростом заряда атома.
Кислотные и основные свойства противоположны друг другу, так же как металлические и неметаллические свойства противоположны друг другу. Там, где первые усиливаются, вторые уменьшаются. Все они похожи, поэтому не стесняйтесь ассоциировать одно с другим, так легче запомнить.
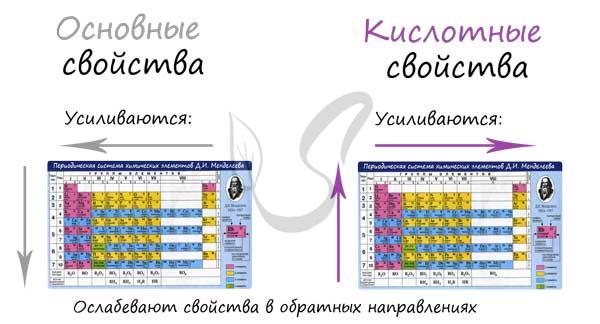
Есть одно важное исключение. Как и в общем случае: исключения только подтверждают правила. В ряду HF → HCl → HBr → HI кислотные свойства усиливаются (а не ослабляются, как должно следовать из логики нашего правила).
Это можно объяснить в теме диссоциации и химической связи. Когда мы перейдем к настоящей теме, я напомню вам о HF и водородных связях между молекулами, которые делают эту кислоту самой слабой. Пока давайте примем это как исключение: HF – самая слабая из этих кислот, а HI – самая сильная.
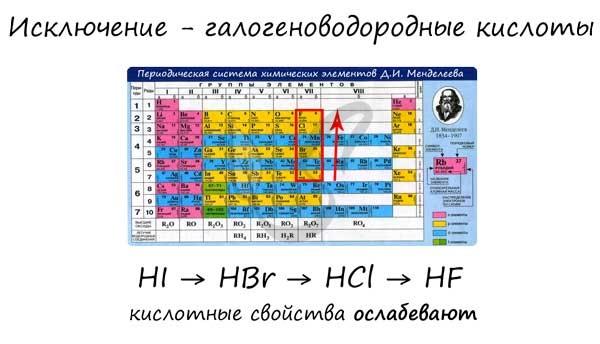
Окислительно-восстановительные свойства
Восстановительные свойства периода ослабевают по мере увеличения атомного заряда, а окислительные свойства усиливаются. В группе, по мере увеличения атомного заряда, восстановительные свойства становятся сильнее, а окислительные – слабее.
Связывать восстановительные свойства с металлическими и основными свойствами, а окислительные свойства с неметаллическими и кислотными свойствами. Это гораздо легче запомнить 
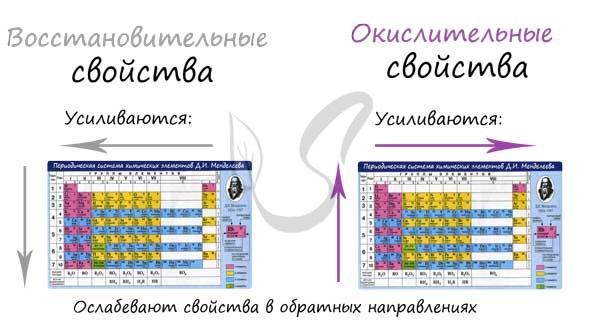
Электроотрицательность (EN), связь, ионизация и энергия сродства к электрону
Электронегативность – это способность связанного атома приобретать отрицательный заряд (притягивать к себе электроны). Мы уже затрагивали эту тему в статье о степенях окисления. Это важное свойство, поскольку более LO-атом притягивает электроны и переходит в отрицательную степень окисления со знаком минус “-“.
Все свойства, упомянутые в подзаголовке, наряду с EO, увеличиваются в периоде с увеличением заряда атома, в то время как в группе они ослабевают с увеличением заряда атома. Таким образом, самым электроотрицательным элементом в правом верхнем углу таблицы Д.И. Менделеева является фтор.
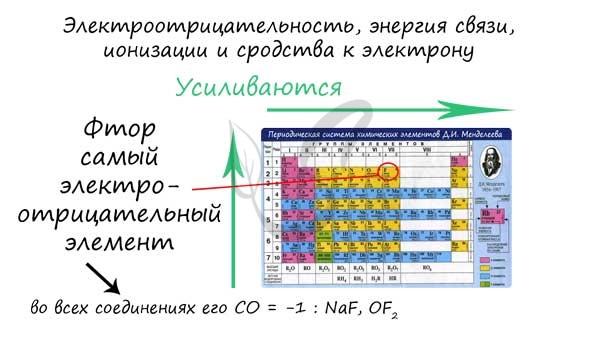
Например, сравните электросопротивления атомов Te, In, Al, P. Ind находится в той же группе, что и алюминий, электросопротивления In → Al увеличиваются (снизу вверх). Алюминий находится в том же периоде, что и сера, значение EO увеличивается Al → S (слева направо). Сравнивая серу и теллур, мы видим, что сера находится в группе выше теллура, что означает, что ее электроотрицательность также выше.
Энергия связи (как и ее прочность) возрастает с увеличением электроотрицательности атомов, образующих связь. Чем больше атом притягивает к себе электроны (чем более он электроотрицателен), тем более прочную связь он образует.
Понятие EO-ness также является “синонимом” понятий сродства к электрону – энергии, выделяемой при присоединении электрона к атому, и энергии ионизации – количества энергии, необходимого для отрыва электрона от атома. Оба увеличиваются с ростом электроотрицательности.
Я продемонстрирую это на примере. Давайте сравним энергии связи трех молекул: H2O, H2S, H2Se.

Высшие оксиды и летучие водородные соединения (ЛВС)
В периодической таблице Д.И. Для элементов периода Менделеева ниже периода 7 находится линия с соответствующими высшими оксидами для каждой группы, ниже линия с летучими водородными соединениями.

Для элементов основных подгрупп, начиная с IV группы (в большинстве случаев), максимальная степень окисления (CO) определяется номером группы. Например, для серы (в группе VI) максимум CO = +6, что она и показывает в соединениях: H2SO4, SO3.
В таблице видно, что для группы VIa формула высшего оксида – RO3и, например, в группе IIIa это R2O3. Запишем наибольшие значения оксидов для вещества VIa: SO3SeO3, TeO3 и группа IIIa: B2O3, Ал2O3, Ga2O3.
На экзамене вы можете пропустить строки с готовыми “высшими” оксидами, как в таблице выше. Я считаю важным подготовить вас к этому. Предположим, что эта строка внезапно исчезла из таблицы, а вам нужно записать высшие оксиды фосфора и углерода.
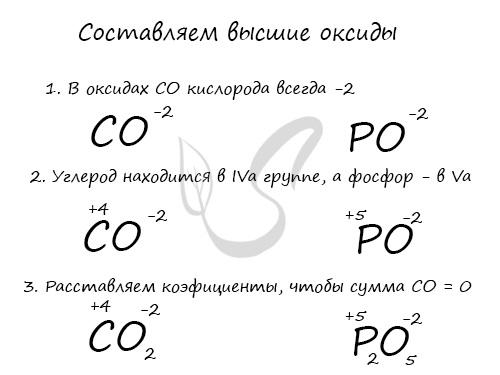
То же самое касается летучих водородных соединений (ЛВС): их может не быть в периодической таблице Д.И. Менделеева, которая появится на экзамене. Позвольте мне рассказать вам, как легко их запомнить.
LBC характерны для групп IV, V, VI и VII. Элементы в этих группах более электроотрицательны, чем водород, поэтому они переходят в “-” отрицательную СО. Минимальная степень окисления для элементов основных подгрупп, начиная с группы IV, может быть рассчитана следующим образом: номер группы – 8.
Например, для углерода минимум CO = 4-8 = -4; для азота 5-8 = -3; для кислорода 6-8 = -2; для фтора 7-8 = -1. Чтобы запомнить LBC, вы должны ассоциировать группы IV, V, VI и VII с хорошо знакомыми вам веществами: метаном, аммиаком, водой и фтористым водородом.
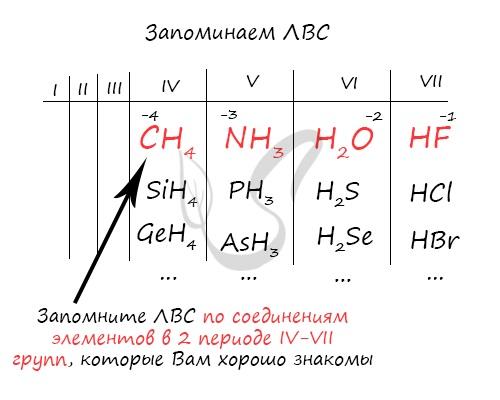
Поскольку общая структура LBC в пределах группы схожа, вспомним, например.2O для кислорода в VI группе, вы легко найдете формулы для других ОСНОВНЫХ веществ VI группы: сера – H2S, H2Se, H2Te, H2По.
© Юрий Сергеевич Беллевич 2018-2021
Эта статья написана Юрием Сергеевичем Беллевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе копирование на другие сайты и ресурсы в Интернете) или любое другое использование информации и объектов без предварительного разрешения владельца авторских прав преследуется по закону. Для получения разрешения на использование данного материала и получения разрешения, пожалуйста, свяжитесь с Юрий Беллевич..
Дробь может быть выражена в виде обыкновенной или десятичной дроби, или, например, в процентах:
Каков заряд ядра атома?
4.1 Состав атомов
Слово “атом” переводится с древнегреческого как “неделимый”. Так считалось почти до конца 19 века. В 1911 году Е. Резерфорд открыл, что в атоме есть положительно заряженное ядро. ядро. Позже выяснилось, что он был окружен электронной оболочкой..
| Электронная оболочка – Совокупность электронов, движущихся вокруг ядра. |
Таким образом, атом – это материальная система, состоящая из ядра и электронной оболочки.
Атомы очень малы – так, сотни тысяч атомов располагаются на толщине листа бумаги. Размер атомных ядер все еще в сто тысяч раз меньше, чем размер атомов.
Атомные ядра заряжены положительно, но они состоят не только из протонов. Ядра также содержат нейтральные частицы, открытые в 1932 году и названные нейтроны. Протоны и нейтроны вместе называются нуклоны – которые являются ядерными частицами.
| Нуклоны – общее название протонов и нейтронов. |
Каждый атом электрически нейтрален, что означает, что число электронов в электронной оболочке атома равно числу протонов в его ядре.
- Название “электрон” происходит от греческого слова, означающего “янтарь”.
- Название “протон” происходит от греческого слова, означающего “первый”.
- Название “нейтрон” происходит от латинского слова, означающего “ни”. (имеется в виду его электрический заряд).
- Символы ” – “, ” + ” и ” 0 ” в символах частиц занимают место правого верхнего индекса.
- Размер электрона настолько мал, что в физике (в рамках современной теории) принято считать некорректным говорить об измерении этого размера.
ЭЛЕКТРОН, ПРОТОН, НЕЙТРОН, НУКЛОН, ЭЛЕКТРОННАЯ ОБОЛОЧКА.
1.Определите, на сколько процентов масса протона меньше массы нейтрона. Какую долю от массы протона составляет эта разница (выразите в виде десятичной дроби и в процентах)?
2.Во сколько раз (приблизительно) масса любого нуклона больше массы электрона?
3.Определите, какую долю массы атома составляет масса его электронов, если атом состоит из 8 протонов и 8 нейтронов. 4.Как вы думаете, удобно ли использовать единицы Международной системы единиц (СИ) для измерения масс атомов?
Между всеми заряженными частицами атома действуют электрические (электростатические) силы: электроны атома притягиваются к ядру и одновременно отталкиваются друг от друга. Взаимодействие заряженных частиц друг с другом передается электрическим полем..
Вы уже знаете одно поле – гравитационное. Более подробно о том, что такое поля и каковы их свойства, вы узнаете на уроках физики.
Все протоны в ядре заряжены положительно и отталкиваются друг от друга под действием электрических сил. Но ядра существуют! Поэтому в ядре, помимо электростатических отталкивающих сил, между нуклонами существует еще одно взаимодействие, с помощью которого они притягиваются друг к другу, причем это взаимодействие гораздо сильнее электростатического. Эти силы называются ядерные силы.и взаимодействие… сильное взаимодействиеи поле, несущее это взаимодействие сильное поле.
В отличие от электростатического взаимодействия, сильное взаимодействие ощущается только на малых расстояниях, порядка размеров атомных ядер. Но сила притяжения, вызванная этим взаимодействием (Fя). во много раз превышает электростатическую (Fэ). Следовательно, “сила” ядер во много раз больше, чем “сила” атомов. Поэтому в химические явления, меняется только электронная оболочка, а атомные ядра остаются неизменными.
Общее число нуклонов в ядре называется массовое число и обозначается буквой А. Количество нейтронов в ядре обозначается N, а количество протонов – обозначается Z . Эти числа связаны между собой простым соотношением:
Плотность материи в ядрах огромна: она составляет около 100 миллионов тонн на кубический сантиметр, что несоизмеримо с плотностью любого химического вещества.
ЭЛЕКТРОННАЯ ОБОЛОЧКА, АТОМНОЕ ЯДРО, МАССОВОЕ ЧИСЛО, ЧИСЛО ПРОТОНОВ, ЧИСЛО НЕЙТРОНОВ.
В химических реакциях атомы могут терять некоторые из своих электронов или добавлять дополнительные. В этом процессе нейтральные атомы образуют заряженные частицы – ионы. Химическая природа атомов не меняется, т.е. атом хлора, например, не превращается в атом азота или в атом какого-либо другого элемента. Физические воздействия достаточно высокой энергии могут вообще “оторвать” от атома всю электронную оболочку. Не изменится и химическая природа атома – забрав электроны у какого-либо другого атома, ядро снова станет атомом или ионом того же элемента. Атомы, ионы и ядра в совокупности называются нуклиды.
| Нуклиды – Общее название для атомов, простых ионов и атомных ядер. |
Символы элементов используются для обозначения нуклидов (помните, что они также могут обозначать один атом) с левосторонними индексами: верхний равен массовому числу, нижний – числу протонов. Примеры обозначений нуклидов:
Теперь мы можем сформулировать окончательное определение химического элемента.
| Химический элемент – Совокупность нуклидов с одинаковым зарядом в ядре. |
Поскольку заряд ядра определяется числом протонов, мы можем назвать химическим элементом совокупность нуклидов с одинаковым числом протонов. Вспомнив то, что мы говорили в начале параграфа, мы можем объяснить один из самых важных химических законов.
В химических реакциях (и в физических взаимодействиях, в которых не участвуют ядра) нуклиды не возникают, не исчезают и не превращаются друг в друга.
Таким образом, массовое число равно сумме числа протонов и числа нейтронов: А = Z + N. Для нуклидов одного и того же элемента заряд ядра одинаков (Z = const) и количество нейтронов N? Число нейтронов в нуклидах одного и того же элемента может быть одинаковым, а может отличаться. Поэтому массовые числа нуклидов одного и того же элемента также могут быть разными. Примером нуклидов одного и того же элемента с разными массовыми числами являются различные стабильные нуклиды олова, характеристики которых приведены в таблице 12. Нуклиды с одинаковыми массовыми числами имеют одинаковую массу, а нуклиды с разными массовыми числами имеют разные массы. Из этого следует, что атомы одного элемента могут отличаться по массе.
Следовательно, нуклиды одного изотопа имеют одинаковое количество протонов (потому что это один элемент), одинаковое количество нейтронов (потому что это один изотоп) и, конечно, одинаковую массу. Такие нуклиды совершенно одинаковы и поэтому по существу неразличимы. (В физике слово “изотоп” иногда также означает один нуклид данного изотопа).
Нуклиды разных изотопов одного и того же элемента отличаются массовыми числами
нейтронов и массы.
| Изотопы элементы водород |
Изотопы элемент Кислород |
Изотопы элементы хлор |
Общее число известных ученым нуклидов приближается к 2000. Из них около 300 являются стабильными, т.е. встречаются в природе. В настоящее время известно 110 элементов, включая искусственные (среди нуклидов физики выделяют изобары– нуклиды с одинаковой массой (независимо от заряда).
Многие элементы имеют по одному природному изотопу, например, Be, F, Na, Al, P, Mn, Co, I, Au и другие. Но большинство элементов имеют по два, три или более стабильных изотопов.
Для описания состава атомных ядер иногда необходимо вычислить фракции протонов или нейтронов в этих ядрах.
| фракция – это отношение количества объектов, долю которых мы определяем, к общему количеству объектов. |
где Di – это дробь интересующих характеристик (например, семерки),
N1 – это количество первых объектов,
N2 – количество вторых объектов,
N3 – количество третьих объектов,
Ni – количество интересующих объектов (например, семь объектов),
Nn – это номер последнего объекта.
Чтобы сделать формулы в математике короче, знак обозначает сумму всех чисел Niот первого (i = 1) до последнего (i = n). В нашей формуле это означает, что номера всех объектов, начиная с первого (N1) до последнего (Nn).
Пример. В коробке 5 зеленых, 3 красных и 2 синих груш; определите, какова доля красных груш.
Дробь может быть выражена в виде обыкновенной или десятичной дроби, или в процентах, например:
НУКЛИД, ИЗОТОП, ФРАКЦИЯ
1.Определить долю протонов в ядре атома. .Определите долю нейтронов в этом ядре.
2.Какова доля нейтронов в ядре нуклида
3.Массовое число этого нуклида равно 27. Доля протонов в нем составляет 48,2%. К какому элементу относится этот нуклид?
4.Нуклид имеет долю нейтронов 0,582. Определите Z.
5.Во сколько раз больше масса атома тяжелого изотопа урана 92U, содержащего 148 нейтронов в ядре, больше, чем масса легкого изотопа урана, содержащего 135 нейтронов в ядре?
Из количественных свойств атома вам уже известны массовое число, число нейтронов в ядре, число протонов в ядре и заряд ядра.
Поскольку заряд протона равен элементарному положительному заряду, число протонов в ядре (Z) и заряд ядра (qя), выраженные в элементарных электрических зарядах, численно равны. Поэтому, как и число протонов, заряд ядра обычно обозначается через Z.
Число протонов одинаково для всех нуклидов элемента, поэтому его можно использовать в качестве характеристики этого элемента. В этом случае он называется атомный номер.
| Атомный номер свойство химического элемента, равное числу протонов в ядре любого нуклида этого элемента. |
Поскольку электрон “легче” каждого нуклона почти в 2000 раз, масса атома (mo) концентрируется в основном в ядре. Его можно измерять в килограммах, но это очень неудобно.
Например, масса самого легкого атома, атома водорода, составляет 1,674 . 10 – 27 кг, и даже самый тяжелый атом на Земле, атом урана, имеет массу всего 3,952 . 10 – 25 кг. Даже используя наименьшую десятую долю грамма, атограмм (ag), мы получим массу атома водорода mo(H) = = 1,674 . 10 – 9 аг. Действительно, это неудобно.
Поэтому в качестве единицы измерения атомных масс используется специальная атомная единица массы, для которой известный американский химик Лайнус Полинг (1901 – 1994) предложил название “Дальтон”.
Атомная единица массы, с достаточной точностью применяемая в химии, равна массе любого нуклона и близка к массе атома водорода, ядро которого состоит из одного протона. В курсе физики 11 класса вы узнаете, почему она немного меньше массы каждой из этих частиц. Для удобства измерения атомная единица массы определяется как масса нуклида наиболее распространенного изотопа углерода.
| Дальтон (атомная единица массы) – 1/12 массы нуклида 12 C. |
Атомной единицей массы является а.е.м. или дн.
1Dn = 1,6605655 . 10- 27 кг 1.66 . 10 – 27 кг.
Если масса атома измеряется в дальтонах, ее традиционно называют не “атомной массой”, а , а атомная масса. Атомная масса и атомная масса – это одна и та же физическая величина. Поскольку это масса одного атома (нуклида), ее называют атомной массой нуклида.
| Атомная масса нуклида – Атомная масса нуклида, выраженная в дальтонах. |
Атомный вес нуклида обозначается буквами Аr за которым следует символ нуклида, например:
Аr( 16 O ) – атомная масса нуклида 16 O,
Ar( 35 Cl) – атомная масса нуклида 35 Cl,
Ar( 27 Al) – атомная масса нуклида 27 Al.
Если элемент имеет более одного изотопа, он состоит из нуклидов с разными массами. В природе изотопный состав элементов обычно постоянен, поэтому для каждого элемента можно рассчитать средняя масса атомов этого элемента может быть рассчитана ():
где D1, D2, . Di – Пропорции 1. и 2, . , i-изотоп;
m0(1), m0(2), . m0(i) – масса нуклида первого, второго, . i-го изотопа;
n – общее число изотопов соответствующего элемента.
Если средняя масса атомов данного элемента измеряется в дальтонах, то она называется атомный вес элемента.
Атомная масса элемента обозначается теми же буквами, что и атомная масса нуклида Аrно в скобках указывается символ соответствующего элемента, а не символ нуклида, например:
Аr(O) – атомная масса кислорода,
Аr(Cl) – атомный вес хлора,
Аr(Al) – атомная масса алюминия.
Поскольку атомная масса элемента и средняя масса атомов этого элемента являются одной и той же физической величиной, выраженной в разных единицах измерения, формула для расчета атомной массы элемента аналогична формуле для расчета средней массы атомов этого элемента
где D1, D2, . Dn – дробь 1, 2, . i-изотоп 6;
Аr(1), Аr(2), . Ar(i) – атомная масса элемента 1, 2, … i-изотоп 6;
п – общее число изотопов элемента.
АТОМНЫЙ НОМЕР ЭЛЕМЕНТА, МАССА АТОМА (НУКЛИДА), АТОМНАЯ МАССА НУКЛИДА, АТОМНАЯ МАССА ЕДИНИЦЫ МАССЫ, АТОМНАЯ МАССА ЭЛЕМЕНТА
1) найти число нейтронов N и количество электронов N(е- ) в следующих атомах: .
Какова доля протонов в ядре каждого из этих атомов?
2) Какие элементы являются изотопами нуклидов, содержащих
| нейтроны | 5 | 16 | 4 | 1 | 60 | 2 | 146 | 0 |
| протоны | 5 | 15 | 3 | 1 | 47 | 1 | 92 | 1 |
Запишите символы этих нуклидов.
3)Какова доля атомов водорода в молекуле воды? Используйте этот пример, чтобы доказать, что “дробь не зависит от части”. Это означает, что доля атомов водорода в любой порции воды равна доле атомов водорода в одной молекуле этого вещества.
4) Какова доля (a) атомов кислорода в оксиде азота N2O5O; б) атомов серы в серной кислоте? 5)Принимая атомную массу нуклида численно равной его массовому числу, рассчитайте атомную массу бора, если природная смесь изотопов бора содержит 19% изотопа 10 B и 81% изотопа 11 B.
6) Учитывая нуклид, атомная масса которого равна его массовому числу, рассчитайте атомные массы следующих элементов, если их изотопные доли в природной смеси (изотопный состав) составляют: a) 24 Mg – 0,796 25 Mg – 0,091 26 Mg – 0,113
(b) 28 Si – 92,2 % 29 Si – 4,7 % 30 Si – 3,1 %
c) 63 Cu – 0,691 65 Cu – 0,309
7)Определите изотопный состав природного таллия (в долях соответствующих изотопов), если в природе присутствуют изотопы таллий-207 и таллий-203, а атомная масса таллия равна 204,37 Dn.
8)Природный аргон состоит из трех изотопов. Доля нуклида 36 Ag составляет 0,34%. Атомный вес аргона равен 39,948 г. Определите соотношение 38 Ag и 40 Ag, встречающихся в природе.
9)Природный магний состоит из трех изотопов. Атомный вес магния составляет 24,305 Dn. Доля изотопа 25 Mg составляет 9,1%. Определите доли двух других изотопов магния с массовыми числами 24 и 26.
10)В земной коре (атмосфере, гидросфере и литосфере) атомы лития-7 встречаются примерно в 12,5 раз чаще, чем атомы лития-6. Определите атомную массу лития.
11)Атомная масса рубидия равна 85,468 г. В природе встречаются 85 Rb и 87 Rb. Определите, во сколько раз больше легких изотопов рубидия, чем тяжелых.
Этот сервер создан при поддержке Российского фонда фундаментальных исследований.
Не разрешается копировать материалы и размещать их на других сайтах.
Авторское право (C) I. Миняйлова и В. Миняйлов
Авторское право (C) Химический факультет Московского государственного университета
Написать письмо редактору
Чтобы продемонстрировать на практике, как найти атомный заряд данного элемента (в нашем случае брома), полезно обратиться к Периодической таблице химических элементов и найти там бром. Это означает, что бром имеет заряд ядра 35, так как он зависит от числа протонов в ядре. Число протонов представляет собой номер, под которым химический элемент значится в знаменитой книге Менделеева.
Заряд атомного ядра
Многие могут возразить, что химия – сложная наука, которую не каждый может понять. Но если вы возьмете серьезный ноутбук и начнете с нуля, все далеко не так мрачно. Первое, с чего следует начать, – это атом и его основные характеристики.
Атом – это самая маленькая молекула из всего, что нас окружает, которая несет всю необходимую информацию, молекула, определяющая характеристики и заряды. Долгое время ученые считали его неделимым, единым, но в течение долгих часов, дней, месяцев и лет исследования, изыскания и эксперименты доказали, что атом тоже имеет структуру. Другими словами, этот микроскопический шарик состоит из множества более мелких элементов, которые влияют на размер его ядра, его свойства и заряд. Структура этих частиц следующая:
- электроны;
- атомные ядра.
Последние также можно разделить на элементарные части, которые в науке называются протонами и нейронами, которых в каждом случае определенное количество.
Количество протонов в ядре указывает на структуру оболочки, которая состоит из электронов. Эта оболочка, в свою очередь, содержит все необходимые свойства данного материала, вещества или объекта. Расчет суммы протонов очень прост – достаточно знать порядковый номер наименьшей части вещества (атома) в известной таблице Менделеева. Эта величина также называется атомным номером и обозначается латинской буквой “Z”. Обратите внимание, что протоны имеют положительный заряд, и эта величина определяется как +1.
Нейроны являются вторым компонентом атомного ядра. Это элементарная субатомная частица, не имеющая заряда, в отличие от электронов и протонов. Нейроны были открыты в 1932 году Дж. Чедвиком, за что через 3 года он получил Нобелевскую премию. В учебниках и научных трудах они обозначаются латинским символом “n”.
Третьим компонентом атома является электрон, который монотонно движется вокруг ядра, образуя облако. Эта частица является самой легкой из всех известных современной науке, что означает, что она также имеет наименьший заряд.
Именно%20сочетание%20положительных%20и%20отрицательных%20частиц%20в%20структуре%20делает%20атом%20незаряженной%20или%20нейтрально%20заряженной%20частицей.%20Ядро,%20по%20сравнению%20с%20общим%20размером%20атома,%20очень%20маленькое,%20но%20именно%20в%20нем%20сосредоточена%20вся%20масса,%20что%20указывает%20на%20его%20высокую%20плотность.
Как%20можно%20определить%20заряд%20на%20ядре%20атома?
Чтобы%20определить%20ядерный%20заряд%20атома,%20необходимо%20хорошо%20понимать%20строение%20атома%20и%20его%20ядра,%20понимать%20основные%20законы%20физики%20и%20химии,%20а%20также%20иметь%20под%20рукой%20периодическую%20таблицу%20Менделеева%20для%20определения%20атомного%20номера%20химического%20элемента.
Чтобы%20найти%20и%20рассчитать%20заряд%20ядра%20атома,%20необходимо:
-
- %20%20
- Знание%20того,%20что%20микроскопическая%20частица%20любого%20вещества%20имеет%20в%20своей%20структуре%20ядро%20и%20электроны,%20которые%20образуют%20вокруг%20нее%20оболочку,%20похожую%20на%20облако.%20Ядро,%20в%20свою%20очередь,%20содержит%20два%20типа%20элементарных%20неделимых%20частиц:%20протоны%20и%20нейроны,%20каждый%20из%20которых%20обладает%20своими%20свойствами%20и%20характеристиками.%20Нейроны%20не%20имеют%20в%20своем%20арсенале%20электронного%20заряда.%20Это%20означает,%20что%20их%20заряд%20неодинаков%20и%20не%20больше%20и%20не%20меньше%20нуля.%20Протоны,%20в%20отличие%20от%20своих%20собратьев,%20имеют%20положительный%20заряд.%20Другими%20словами,%20их%20электрический%20заряд%20можно%20обозначить%20как%20+1.
%20%20
-
- Электроны,%20которые%20являются%20неотъемлемой%20частью%20каждого%20атома,%20также%20имеют%20определенный%20электрический%20заряд.%20Это%20отрицательно%20заряженные%20элементарные%20частицы,%20которые%20обозначаются%20как%20-1.
%20%20
-
- Чтобы%20рассчитать%20заряд%20атома,%20нам%20необходимо%20знать%20его%20структуру%20(мы%20только%20что%20вспомнили%20необходимую%20информацию),%20количество%20элементарных%20частиц%20в%20его%20составе.%20Чтобы%20узнать%20величину%20заряда%20атома,%20мы%20должны%20математически%20сложить%20количество%20одних%20частиц%20(протонов)%20с%20другими%20частицами%20(электронами).%20Обычная%20характеристика%20атома%20заключается%20в%20том,%20что%20он%20является%20электронно-нейтральным.%20Другими%20словами,%20количество%20электронов%20равно%20количеству%20протонов.%20В%20результате%20значение%20заряда%20такого%20атома%20равно%20нулю.
%20%20
- Важный%20нюанс:%20существуют%20ситуации,%20когда%20количество%20положительно%20и%20отрицательно%20заряженных%20элементарных%20частиц%20в%20ядре%20может%20быть%20не%20одинаковым.%20Это%20говорит%20о%20том,%20что%20атом%20становится%20ионом%20с%20положительным%20или%20отрицательным%20зарядом.
Это%20были%20основные%20рекомендации%20и%20указания%20для%20тех,%20кто%20пытался%20постичь%20основы%20естественных%20наук.%20А%20затем%20несколько%20формул.
Обозначение%20атомного%20ядра%20в%20научной%20сфере%20выглядит%20как%20Ze.%20Это%20довольно%20просто%20расшифровать:%20Z%20-%20это%20номер,%20присвоенный%20элементу%20в%20известной%20таблице%20Менделеева,%20также%20называемый%20порядковым%20номером%20или%20зарядовым%20числом.%20Он%20обозначает%20число%20протонов%20в%20ядре%20атома%20и%20является%20просто%20зарядом%20протона.
Современная%20наука%20различает%20ядра%20с%20различными%20значениями%20заряда,%20от%201%20до%20118.
Еще%20одно%20важное%20понятие,%20которое%20должны%20знать%20юные%20химики,%20-%20это%20массовое%20число.%20Этот%20термин%20относится%20к%20общему%20количеству%20зарядов%20нуклонов%20(мельчайших%20частей%20атомного%20ядра%20химического%20элемента).%20Это%20число%20можно%20найти%20по%20формуле:%20A%20=%20Z%20+%20Nгде%20А%20-%20искомое%20массовое%20число,%20Z%20-%20число%20протонов%20и%20AN%20-%20число%20нейтронов%20в%20ядре.
Каков%20заряд%20ядра%20атома%20брома?
Чтобы%20продемонстрировать%20на%20практике,%20как%20найти%20атомный%20заряд%20нужного%20вам%20элемента%20(в%20нашем%20случае%20брома),%20загляните%20в%20периодическую%20таблицу%20химических%20элементов%20и%20найдите%20там%20бром.%20Это%20означает,%20что%20он%20имеет%20заряд%20ядра%2035,%20поскольку%20этот%20заряд%20зависит%20от%20числа%20протонов%20в%20ядре.%20Количество%20протонов%20указывает%20на%20номер,%20под%20которым%20химический%20элемент%20значится%20в%20знаменитой%20книге%20Менделеева.
%20
Приведено еще несколько примеров, чтобы будущим химикам было легче рассчитать необходимые данные:
- заряд ядра атома натрия (na) равен 11, так как его можно найти под этим номером в таблице химических элементов.
- Заряд ядра фосфора (с символическим обозначением P) равен 15, потому что таково число протонов в ядре;
- Сера (с графическим символомS) является соседом в таблице предыдущего элемента, поэтому она имеет заряд ядра 16;
- Железо (мы можем найти его под номером Fe) имеет номер 26, что говорит нам о таком же количестве протонов в ядре, а значит, и о заряде атома;
- Углерод (он же C) находится под номером 6 в периодической таблице, что дает нам необходимую информацию;
- Магний имеет атомный номер 12 и известен в мире как Mg;
- Хлор в периодической таблице, записанный как Cl, имеет атомный номер 17, поэтому его атомный номер также равен 17 (что нам и нужно);
- Кальций (Ca), который так полезен для молодых организмов, имеет номер 20;
- Атом азота имеет ядерный заряд (письменное число N) 7, именно в таком порядке он представлен в периодической таблице;
- Барий имеет номер 56, который равен его атомному весу;
- химический элемент селен (Se) имеет 34 протона в своем ядре, что означает, что он имеет тот же ядерный заряд, что и его атом;
- Серебро (или Ag в его письменном обозначении) имеет порядковый номер и атомную массу 47;
- Если вы хотите узнать заряд ядра атома лития (Li), вы должны вернуться к началу великого труда Менделеева, где он равен 3;
- Аурум или наше любимое золото (Au) имеет атомную массу 79;
- и имеет атомную массу 18;
- Рубидий имеет атомную массу 37; австроний имеет атомную массу 38.
Можно долго перечислять все компоненты периодической таблицы Менделеева, потому что их очень много. Самое главное, что суть явления понятна, и если нам нужно рассчитать атомный номер калия, кислорода, кремния, цинка, алюминия, водорода, бериллия, бора, фтора, меди, фтора, мышьяка, ртути, неона, марганца, титана, то достаточно обратиться к таблице химических элементов и знать порядковый номер того или иного вещества.
Читайте далее: